预计市场规模将达到 到2030年4.69亿美元,从2023年的8.824亿美元增加到9.7% 在预测期间。 生物工艺验证,是指证明和保证生物药品制造工艺持续可靠地生产符合预先确定的质量标准和监管要求的产品的过程. 它涉及验证关键过程参数、设备、分析测试方法、清洁程序、计算机系统和设施。 生物工艺验证对确保药物安全、功效和质量至关重要。 推动生物工艺验证市场增长的主要驱动力包括增加对制药和生物技术工业的研发投资, 生物类似物和生物记录学 市场和有利的政府规章等等。
生物工艺验证市场按测试类型,工艺类型和最终用户及区域划分. 按检验类型,市场分为可提取检验服务,微生物检验服务,生化检验服务,完整性检验服务等. 2022年试验型机段占最大份额. 这是因为生物反应器等生物工艺仪器和 色谱 (b) 生物制药公司验证其制造过程的系统。
分析视图 :
- 生物工艺验证市场在未来几年内将大幅增长。 由于对生物过程验证的严格监管要求,北美和欧洲目前占据市场主导地位. 然而,随着中国、印度和韩国等国家的生物相似性和生物性制造能力的扩大,亚太的增长预计将最快。
- 市场主要靠越来越多地采用单克隆抗体和重组蛋白来治疗各种慢性病. 随着生物过程越来越先进和复杂,对这些过程进行彻底验证的必要性将继续增加。 此外,管理机构为确保产品质量和安全提供的持续支持也将推动采用生物工艺验证解决方案。
- 然而,市场也面临与审定程序有关的高昂成本的限制。 既定的验证协议加上缺乏训练有素的专业人员,构成进一步的挑战。
- 尽管如此,细胞疗法和基因疗法的出现为市场带来了巨大的增长机会。 合同服务供应商正集中力量整合数字工具,以进行持续流程监测和实时发布测试。 采用先进的分析和建模技术有助于优化生物加工,促进产品的及时批准。 总体而言,随着生物制药研发开支的上升以及确保一致的工艺性能的需要的不断增长,预计未来对生物工艺验证解决方案的需求将大大增加。
生物工艺验证市场区域透视:
- 北美 预计在预测期内将是最大的生物工艺验证市场,因为 2022年市场份额的2%。 。 。 北美市场的增长归因于主要生物制药公司的存在,研发投资高,以及该区域生物工艺验证的严格监管要求.
- 欧洲 预计是生物工艺验证的第二大市场,因为 2022年市场份额的5%。 。 。 本区域市场的增长归因于生物生产活动的增加、对生命科学研究的日益重视以及政府在欧洲的有利资助。
- 亚太 预计将成为增长最快的生物工艺验证市场,表明 预测期间CAGR超过19.3%,。 。 。 亚太区域市场的增长归因于生物制药部门不断扩大,研发基础设施投资增加,以及本区域外包服务迅速增长。
图 1. 2023年按区域分列的全球生物加工验证市场份额(%)
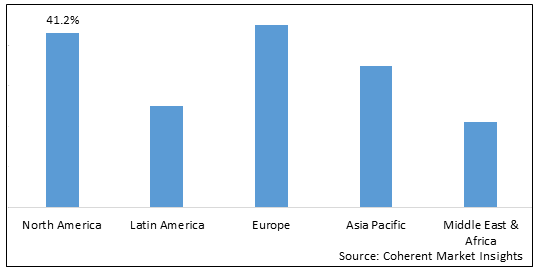
To learn more about this report, request sample copy
生物工艺验证市场驱动器:
- 增加生物药品研发投资: 过去十年来,生物制药业的研发支出大幅增加。 几家生物制药公司拥有很强的临床管道,越来越注重开发新颖的生物学和生物类似物. 生物药物研制的这种上升,后来助长了临床前和临床制造过程中广泛进行过程特征鉴定和验证的需要. 此外,细胞和基因疗法等新方式的生物过程复杂,需要更严格的验证,以确保药物安全和功效。
- 生物学和生物类似市场的增长: 生物药物和生物类似物市场迅速扩大,是推动生物过程验证活动的主要因素。 癌症和自体免疫疾病高价值生物学的审批,使全行业的生物生产量进一步升级. 这就产生了对经过验证的制造工艺和分析的巨大需求,以确保无缝的推广和产品质量合规。
- 增加生物制药公司的外包: 许多生物制药公司正在战略性地外包各种生物加工活动,包括向合同公司提供验证服务。 合同制造组织(CMO)正在加强其服务提供,为其赞助商的工艺和产品提供端到端验证支持. 此外,首席管理官在设计和实施符合监管期望的验证协议方面提供的专门知识正在鼓励赞助者越来越多地利用外包。
- 不断增加的生物工艺基础设施投资: 生物制药公司正在作出大量投资,以建设先进的生物加工设施并提高其生产能力。 扩大API和生物学的生产能力需要大量的验证要求。 此外,更新遗留设施以提高流程效率还需要重新鉴定设备、方法和基础设施。 这大大促进了生物过程验证需求。 此外,市场参与者一直在投资启动新的资源中心,预计这将推动全球生物进程验证市场在预测期间的增长。 例如,2022年,医疗和制药行业的OEM单用途组件全球供应商Qosina启动了新的生物工艺资源中心,这是生物工艺行业的信息来源。
| 报告范围 | 细节 |
|---|
| 基准年 : | 2022 (英语). | 2023年市场规模: | (单位:千美元) |
|---|
| 历史数据: | 2018年至2022年 互联网档案馆的存檔,存档日期2018-09-02. | 预测周期 : | 2023 - 2030 (英语). |
|---|
| 2023至2030年CAGR预测期: | 9.7% (单位:千美元) | 2030 (英语). 数值预测 : | 882.4亿nn美元 |
|---|
| 覆盖的地理: | - 北美: 美国和加拿大
- 拉丁美洲: 巴西、阿根廷、墨西哥和拉丁美洲其他地区
- 欧洲: 德国、英国、西班牙、法国、意大利、俄罗斯和欧洲其他地区
- 亚太: 中国、印度、日本、澳大利亚、韩国、东盟和亚太其他地区
- 中东和非洲: 海湾合作委员会国家、以色列、南非、北非、中非和中东其他地区
|
| 所涵盖的部分: | - 按测试类型 : 可提取测试服务、微生物测试服务、物理化学测试服务、诚信测试服务等(兼容测试服务等)
- 按进程构成部分: 过滤元件、媒体容器和袋、冷冻和 Thewing 工艺袋、生物反应器、传输系统及其他(混合系统及其他)
- 按终端用户 : 医药和生物技术 公司、合同发展和制造组织、学术和研究机构及其他(临床研究组织及其他)
|
| 涵盖的公司: | Sartorius Stedim生物技术公司、Merck KGaA公司、Pall公司、Cobetter过滤设备公司、Toxikon公司、DOC S.r.l.、MEISSNER FILTRION ProDUCTS、Themo Fisher Scientific、SGS SA、Eurofins Science、Lonza集团、ProBioGen公司、Charles River实验室、太平洋生物实验室、直布罗陀实验室、Nelson实验室、生物加工技术顾问公司、CMIC HOLDINGS公司、有限公司、Cytovance Biologics公司和Woxi Biologics公司。 |
| 增长动力: | - 增加生物药品研发投资
- 生物学和生物类似市场的增长
- 增加生物制药公司的外包
- 不断增长的生物工艺基础设施投资
|
| 限制和挑战: | |
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
生物加工验证市场 机会:
- 自动化和数据分析: 机器人和互联互通的IOT系统等自动化技术为优化和加快生物过程验证活动提供了巨大的机遇. 与自动化相结合的高级分析可以加强监测,便利持续核查,并允许在验证过程中快速数据驱动决策. 区块链等数据管理技术也促进了外包伙伴之间的数据安全和透明度。
- 单用途系统集成: 由于灵活性、降低成本和加快实施速度等优势,生物加工中单一用途技术的采用越来越多。 将单一用途组件纳入关键流程步骤,为更快和更有效的验证提供了途径。 此外,单一用途系统的模块化性质允许在将新的可支配部件引入现有验证程序时进行额外验证。
- 虚拟化和硅建模: 在硅建模工具中,允许对生物过程进行数字模拟,用于优化和排除故障. 利用机械模型和人工智能进行虚拟验证有可能减少对广泛实时物理试验的依赖。 通过数字模拟制造工艺,生物药品玩家可以完善验证协议,并将物理运行的焦点集中在边缘病例上. 这可大大提高生产力和速度。
- 合作伙伴关系: 生物加工公司正在与技术供应商、CMO、实验室和研究机构结成战略伙伴关系,以加强其验证能力和测试能力。 合作框架允许利用合作伙伴的专门知识和基础设施开发方法、特征分析、自动化一体化和其他验证需要。
生物加工验证市场 趋势:
- 数字化和无纸化验证: 一个显著的趋势是,向利用自动化、电子日志和专门的信息技术基础设施进行无纸化验证迈进。 数字工具允许以安全和合规的方式集中管理验证生命周期数据。 它们还加强了对历史记录的获取和跨职能小组之间的实时信息共享,以支持持续核查。
- 按设计原则采用质量: 生物制药公司正在通过设计方法增加质量的利用。 QbD有助于更深入地了解制定控制战略和确定设计空间,以确保一致的质量。 这种以科学为基础的实时发布方法允许将验证从证明遵守转为持续的进程核查。
- 加强分析测试: 高级分析工具,如高分辨率质谱仪,在验证过程中对生化特性、杂质和降解产物进行特征分析。 此外,正在开发分析化验包,专门量化宿主细胞DNA和残留蛋白质等关键质量属性。
- 将监管遵守情况结合起来: 生物制药公司正在对其生产过程采取更加综合的质量和验证战略,以便与多个监管部门相结合。 正在利用质量风险管理原则设计统一验证协议,以满足林业发展局、EMA和ICH准则的要求。
生物加工验证市场限制:
- 资本投资要求高: 全面的生物工艺验证需要大量投资,为设施配备先进的仪器、自动化系统和信息技术基础设施。 规模较小的生物制药商和初创企业可能没有足够的资本来支付大量审定支出。 这可能使它们无法实施经过验证的程序,从而限制了增长机会。
- 产品审批时限: 生物过程的端到端验证以及技术转让活动可以将生物学的监管批准时限延长几个月。 所涉及的广泛审判也使修改工作变得非常繁琐。 由此产生的产品发射时限很长,会限制制造商的增长潜力。
- 未界定的新兴市场条例: 中国、巴西和韩国等高增长的新兴市场对生物过程验证的监管预期的不确定性对制造商构成挑战。 不明确的验证规范迫使公司承担额外成本,以便在扩大进入这些市场时重新验证符合当地要求的程序。
最近的事态发展:
新产品发射:
- 2019年1月,参加中国足协杯. 萨托里乌斯·斯蒂丁生物技术国际制药和实验室设备供应商为生物制药业和实验室提供了解决方案,推出了AMBr 250模块,这是一个用于细胞线筛选、流程优化和扩大模型等生物进程开发应用的自动化小型生物反应器系统
采购和伙伴关系:
- 2021年1月,生物药学研究与工业的国际伙伴萨托里乌斯·AG(Sartorius AG)获得了GMP级细胞培养成分全球领先供应商CellGenix的多数股权,以扩大其细胞培养媒体组合.
- 2020年6月时, 瑟莫·费舍尔科学一家生物技术公司收购了Henogen(病毒载体CDMO),以扩大细胞和基因治疗的开发和制造能力。
图 2. 全球生物加工验证市场份额(%),按试验类型分列,2023年
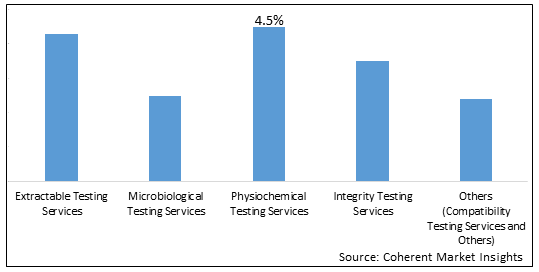
To learn more about this report, request sample copy
生物加工验证市场上的顶级公司:
- 萨托里乌斯·斯蒂丁生物技术
- 默科克 KGaA
- 保龄球公司
- 更好的过滤设备
- 托克斯孔公司
- DOC S.r.l. (英语).
- 制造业制造产品
- 瑟莫·费舍尔科学
- SGS SA (英语).
- 欧洲鳍科学
- 隆扎集团
- ProBioGen公司
- 查尔斯河实验室
- 太平洋生物实验室
- 直布罗陀实验室
- 纳尔逊实验室
- 生物加工技术顾问
- CMIC 控股有限公司
- 循环生物学
- 武西生物学
* 定义: 生物工艺验证是指生物制药工艺持续可靠地生产符合预定规格和质量标准的产品的有文件证据和保证. 它涉及根据良好制造做法和监管准则验证生物生产的所有关键方面,包括设备、设施、公用事业、工艺、分析测试方法和自动化系统。 生物工艺验证是生物制品制造的重要组成部分,对确保产品质量、功效和安全至关重要。 它使人们相信,制造过程消除了差异,并始终提供高质量的产出。
生物技术领域其他有希望的报告很少 工业:
生物外包市场
生物市场
生物药品 市场
生物类似物市场


