Предполагается, что биоаналоги продолжают оказывать значительное влияние на фармацевтическую промышленность. Многие регулирующие органы установили клинические рекомендации для поддержки разработки биоаналогов, устанавливая требования к демонстрации сопоставимой фармакокинетики, фармакодинамики, безопасности и эффективности от фазы I до контролируемых рандомизированных испытаний фазы III.
Хотя биоаналоги Для их утверждения не требуется проходить интенсивные клинические испытания, необходимы данные, демонстрирующие их сходство с оригинальным биологическим с точки зрения клинической эффективности и безопасности. Принятие биоаналогов варьируется от страны к стране, что неизменно связано с вопросами регулирования и доступа к рынкам. Ожидается, что на рынке биоаналогов будет наблюдаться значительный рост из-за истечения срока действия и прекращения существующих лекарств и наличия богатых людей. трубопровод биоаналог продукции, особенно на стадии III.
Размер мирового рынка биоаналогов был оценен в $ 5,0 bион В 2017 году ожидается CAGR 35,2.% за прогнозный период (2018-2026).
глобальный Биоаналоги Анализ рыночной доли (%), по типу продукта, 2017
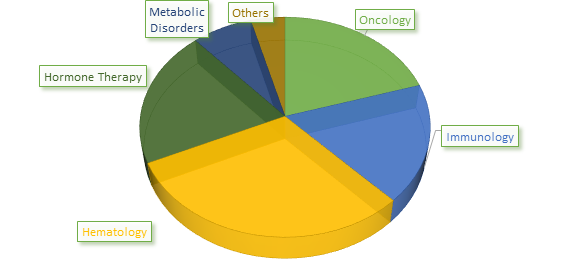
Чтобы узнать больше об этом отчете, запросить образец копии
Когерентный анализ рыночных представлений (2019)
Ожидается, что увеличение числа одобрений биоаналогов будет стимулировать рост рынка биоаналогов.
Увеличение числа утвержденных биоаналоги Ожидается, что из-за большей ясности в процессе обзора Управления по контролю за продуктами и лекарствами США (FDA), кроме процесса производства и разработки, будет стимулировать рост рынка биоаналогов. Например, в июле 2018 года Управление по контролю за продуктами и лекарствами США (FDA) представило план действий по биосимилярам для поощрения разработки биосимиляров. Этот процесс утверждения побуждает заявителей разрешать патентные споры до запуска биоаналогов.
Кроме того, число поданных заявок на биоаналоги увеличилось, поскольку производители стали более комфортно относиться к сложным нормативным и судебным схемам, связанным с подачей биоаналоговой заявки. Например, с 2015 года FDA одобрило 16 биоаналогов, и ожидается, что их число увеличится в течение прогнозируемого периода. Несколько других правительственных учреждений также следуют аналогичным тенденциям для одобрения продукции. Например, в ноябре 2017 года Samsung Bioepis получила два одобрения на свой биоаналог адалимумаба, Hadlima (SB5) и его биоаналог трастузумаба, Samfenet (SB3), от Министерства безопасности пищевых продуктов и лекарств Кореи (Южная Корея).
Рынок биоаналогов – ограничения
Ожидается, что строгие нормативные руководящие принципы для разработки и производства биоаналогов в США будут сдерживать рост мирового рынка биоаналогов. Например, в 2018 году FDA США отклонило четыре биоаналогичных заявки. В апреле 2018 года FDA США отклонило кандидата Pfizer в биоаналог трастузумаба и кандидата Сандоз в биоаналог ритуксимаба в мае 2018 года.
Кроме того, ожидается, что несколько производственных проблем для биоаналогов, которые в первую очередь возникают из-за того, что биологические препараты гораздо более сложны структурно и их сложнее охарактеризовать, производить и воспроизводить, чем большинство мелкомолекулярных препаратов, также будут сдерживать рост рынка. Небольшие изменения в производственном процессе могут потенциально изменить безопасность и эффективность препарата.
Рынок биосимиляров - региональные исследования
На основе региона глобальный рынок биоаналогов сегментирован на Северную Америку, Латинскую Америку, Европу, Азиатско-Тихоокеанский регион, Ближний Восток и Африку. Ожидается, что Европа станет самым прибыльным рынком для биоаналогов за прогнозируемый период. Ожидается, что усиление внимания регулирующих органов к разработке новых биоаналогов будет стимулировать рост рынка в Европе. Например, в июле 2016 года Европейское агентство по лекарственным средствам (EMA) санкционировало введение и маркетинг торинана и инхикса, биоаналогов гепарина с низким молекулярным весом (LMWH), эноксапарина.
Ожидается, что объем рынка биоаналогов в Азиатско-Тихоокеанском регионе будет быстро расти из-за значительного увеличения числа одобрений биоаналогов. Например, в 2017 году Celltrion получил одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов Китая (CFDA) на начало клинических испытаний инфликсимаба Remsima (CT-P13) в Китае. Это делает Celltrion первой иностранной компанией, которая начала клинические испытания биоаналога антител в Китае.
Глобальная рыночная стоимость биоаналогов (US$ Bn) и рост Y-o-Y (%), 2016-2026
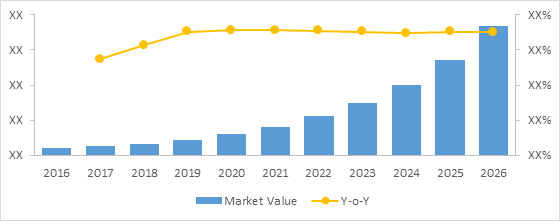
Чтобы узнать больше об этом отчете, запросить образец копии
Когерентный анализ рыночных представлений (2019)
Рынок биоаналогов - конкурентный ландшафт
Ключевые игроки, работающие на мировом рынке биоаналогов, включают Novartis AG, Pfizer, Inc., Teva Pharmaceutical Industries Ltd., Celltrion Healthcare Co., Ltd., Biocon Limited, Amgen, Inc., Dr. Reddy's Laboratories и Sanofi S.A.
Поделиться
Об авторе
Abhijeet Kale
Абхиджит Кейл — ориентированный на результат консультант по управлению с пятилетним опытом работы в сфере биотехнологий и клинической диагностики. Обладая обширным опытом в области научных исследований и бизнес-стратегии, Абхиджит помогает организациям определять потенциальные источники дохода и, в свою очередь, помогать клиентам со стратегиями выхода на рынок. Он помогает клиентам разрабатывать надежные стратегии для соответствия требованиям FDA и EMA.
Не хватает удобства чтения отчетов на местном языке? Найдите нужный вам язык:
Измените свою стратегию с помощью эксклюзивные отчеты о тенденциях :
Часто задаваемые вопросы
Присоединяйтесь к тысячам компаний по всему миру, стремящихся к making the Excellent Business Solutions.
Просмотреть всех наших клиентов