Ожидается, что объем рынка валидации биопроцессов достигнет 460,9 млн долларов США к 2030 году с 882,4 млн долларов США в 2023 году, увеличившись на 9,7% в течение прогнозируемого периода. Проверка биопроцессов относится к процессу демонстрации и обеспечения того, чтобы биофармацевтический производственный процесс последовательно и надежно производил продукты, которые соответствуют заранее определенным стандартам качества и нормативным требованиям. Он включает в себя проверку критических параметров процесса, оборудования, методов аналитического тестирования, процедур очистки, компьютерных систем и объектов. Валидация биопроцессов имеет решающее значение для обеспечения безопасности, эффективности и качества лекарств. Ключевыми факторами, стимулирующими рост рынка валидации биопроцессов, являются увеличение инвестиций в НИОКР в фармацевтической и биотехнологической отраслях, рост производства. биоаналоги и биологические рынка и благоприятного государственного регулирования.
Рынок валидации биопроцессов сегментирован по типу тестирования, типу процесса и конечному пользователю и региону. По типу теста рынок подразделяется на извлекаемые услуги тестирования, услуги микробиологического тестирования, услуги физиохимического тестирования, услуги тестирования целостности и другие. Наибольшую долю в 2022 году составил сегмент тестового типа. Это связано с высоким внедрением инструментов биопроцесса, таких как биореакторы и биореакторы. хроматография системы биофармацевтических компаний для проверки их производственных процессов.
Мнение аналитика:
- Рынок валидации биопроцессов в ближайшие годы значительно вырастет. Северная Америка и Европа в настоящее время доминируют на рынке из-за строгих нормативных требований для проверки биопроцессов. Ожидается, что Азиатско-Тихоокеанский регион продемонстрирует самый быстрый рост с расширением возможностей производства биоаналогов и биологических препаратов в таких странах, как Китай, Индия и Южная Корея.
- Рынок в первую очередь обусловлен растущим внедрением моноклональных антител и рекомбинантных белков для лечения различных хронических заболеваний. По мере того, как биопроцессы становятся все более совершенными и сложными, потребность в тщательной проверке этих процессов будет продолжать расти. Кроме того, постоянная поддержка со стороны регулирующих органов для обеспечения качества и безопасности продукции также будет способствовать принятию решений по валидации биопроцессов.
- Однако рынок также сталкивается с ограничениями из-за высоких затрат, связанных с процедурами проверки. Установленные протоколы проверки в сочетании с отсутствием подготовленных специалистов создают дополнительные проблемы.
- Тем не менее, появление клеточной терапии и генной терапии открывает большие возможности для роста на рынке. Поставщики контрактных услуг сосредоточены на интеграции цифровых инструментов для непрерывного мониторинга процессов и тестирования выпуска в режиме реального времени. Принятие передовых методов анализа и моделирования может помочь оптимизировать биопроцессы и облегчить своевременное утверждение продукции. В целом, с ростом расходов на биофармацевтические исследования и разработки и растущей потребностью в обеспечении последовательной производительности процесса, ожидается, что спрос на решения для валидации биопроцессов значительно возрастет в будущем.
Региональные исследования рынка валидации биопроцессов:
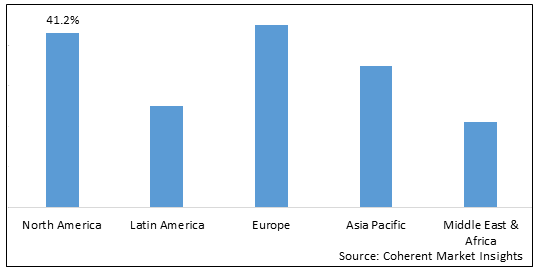
- Северная Америка Ожидается, что он станет крупнейшим рынком для валидации биопроцессов в течение прогнозируемого периода. 2% доли рынка в 2022 году. Рост рынка в Северной Америке объясняется присутствием в регионе ведущих биофармацевтических компаний, высокими инвестициями в НИОКР и строгими нормативными требованиями к валидации биопроцессов.
- Европа Ожидается, что он станет вторым по величине рынком для валидации биопроцессов. 5% доли рынка в 2022 году. Рост рынка в регионе объясняется увеличением биопроизводства, увеличением внимания к исследованиям в области наук о жизни и благоприятным государственным финансированием в Европе.
- Азиатско-Тихоокеанский регион Ожидается, что это будет самый быстрорастущий рынок для валидации биопроцессов, демонстрирующий CAGR более 19,3% в течение прогнозируемого периода. Рост рынка в Азиатско-Тихоокеанском регионе объясняется расширением сектора биофармацевтического производства, увеличением инвестиций в инфраструктуру НИОКР и быстрым ростом услуг аутсорсинга в регионе.
Фигура 1. Доля мирового рынка валидации биопроцессов (%), по регионам, 2023 год
To learn more about this report, request sample copy
Рыночные драйверы валидации биопроцессов:
- Увеличение инвестиций в НИОКР в биофармацевтические препараты: За последнее десятилетие биофармацевтическая промышленность стала свидетелем значительного роста расходов на НИОКР. Несколько компаний, занимающихся биофармой, имеют надежные клинические конвейеры, уделяя все больше внимания разработке новых биологических препаратов и биоаналогов. Этот рост разработки биологических препаратов впоследствии подпитывал потребность в обширной характеристике и валидации процессов в доклиническом и клиническом производстве. Кроме того, сложность биопроцессов для новых методов, таких как клеточная и генная терапия, требует большей строгости проверки для обеспечения безопасности и эффективности лекарств.
- Рост рынка биопрепаратов и биоаналогов: Быстро растущий рынок биологических препаратов и биоаналогов является основным фактором, стимулирующим деятельность по валидации биопроцессов. Одобрение ценных биопрепаратов для лечения рака и аутоиммунных заболеваний еще больше увеличило объемы биопроизводства в отрасли. Это создает значительный спрос на проверенные производственные процессы и аналитику для обеспечения бесшовного масштабирования и соответствия качеству продукции.
- Увеличение аутсорсинга биофармацевтическими фирмами: Многие фирмы, занимающиеся биофармой, стратегически аутсорсингуют различные виды деятельности по биообработке, включая услуги по валидации для контрактных компаний. Контрактные производственные организации (КМО) расширяют свои предложения по обслуживанию, чтобы обеспечить сквозную поддержку процессов и продуктов своих спонсоров. Кроме того, опыт, предоставляемый КМО в разработке и внедрении протоколов проверки в соответствии с нормативными ожиданиями, побуждает спонсоров все чаще использовать аутсорсинг.
- Рост инвестиций в инфраструктуру биопроцессов: Значительные инвестиции в биофармацевтические компании делаются для создания передовых биоперерабатывающих мощностей и увеличения их производственных мощностей. Расширение производственных мощностей для API и биопрепаратов требует значительных требований к валидации. Кроме того, модернизация устаревших объектов для повышения эффективности процессов также требует обновления оборудования, методов и инфраструктуры. Это вносит значительный вклад в спрос на проверку биопроцессов. Кроме того, участники рынка инвестируют в запуск новых ресурсных центров, что, как ожидается, будет стимулировать рост мирового рынка валидации биопроцессов в течение прогнозируемого периода. Например, в 2022 году Qosina, глобальный поставщик OEM-компонентов для медицинской и фармацевтической промышленности, запустила свой новый Центр биопроцессных ресурсов.
Отчет рынка валидации биопроцессов
| Отчетное покрытие | Подробности |
|---|
| Базовый год: | 2022 год | Размер рынка в 2023 году: | $460,9 млн. |
|---|
| Исторические данные для: | 2018-2022 годы | Прогнозный период: | 2023 - 2030 |
|---|
| Прогнозный период с 2023 по 2030 год CAGR: | 9,7% | 2030 год Прогноз ценности: | US$ 882,4 млн. |
|---|
| География охватывает: | - Северная Америка: США и Канада
- Латинская Америка: Бразилия, Аргентина, Мексика и остальная часть Латинской Америки
- Европа: Германия, Великобритания, Испания, Франция, Италия, Россия и остальная Европа
- Азиатско-Тихоокеанский регион: Китай, Индия, Япония, Австралия, Южная Корея, АСЕАН и остальная часть Азиатско-Тихоокеанского региона
- Ближний Восток и Африка: Страны ССАГПЗ, Израиль, Южная Африка, Северная Африка и Центральная Африка и остальная часть Ближнего Востока
|
| Сегменты охватываются: | - Тип испытания: Услуги по экстракционному тестированию, услуги по микробиологическому тестированию, услуги по физиохимическому тестированию, услуги по тестированию целостности и другие (услуги по тестированию совместимости и другие)
- По компоненту процесса: Элементы фильтров, медиаконтейнеры и пакеты, пакеты процессов замораживания и оттаивания, биореакторы, системы передачи и другие (системы смешивания и другие)
- Конечный пользователь: Фармацевтика и биотехнология Компании, организации по разработке контрактов и производству, академические и исследовательские институты и другие (организации по клиническим исследованиям и другие)
|
| Компании охвачены: | Sartorius Stedim Biotech, Merck KGaA, Pall Corporation, Cobetter Filtration Equipment, Toxikon Corporation, DOC S.r.l., MEISSNER FILTRATION PRODUCTS, Thermo Fisher Scientific, SGS SA, Eurofins Scientific, Lonza Group, ProBioGen AG, Charles River Laboratories, Pacific BioLabs, Gibraltar Laboratories, Nelson Laboratories, BioProcess Technology Consultants, CMIC HOLDINGS Co., Ltd, Cytovance Biologics и Wuxi Biologics. |
| Драйверы роста: | - Увеличение инвестиций в НИОКР в биофармацевтические препараты
- Рост рынка биопрепаратов и биоаналогов
- Увеличение аутсорсинга биофармацевтическими фирмами
- Растущие инвестиции в инфраструктуру биопроцессов
|
| Ограничения и вызовы: | - Высокие требования к капиталовложениям
- Длительные сроки утверждения продукции
- Неопределенные правила для развивающихся рынков
|
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
Рынок валидации биопроцессов Возможности:
- Автоматизация и анализ данных: Технологии автоматизации, такие как робототехника и взаимосвязанные системы IoT, предоставляют огромные возможности для оптимизации и ускорения валидации биопроцессов. Продвинутая аналитика в сочетании с автоматизацией может улучшить мониторинг, облегчить непрерывную проверку и обеспечить быстрое принятие решений на основе данных во время проверки. Технологии управления данными, такие как блокчейн, также способствуют безопасности данных и прозрачности между партнерами-аутсорсинговыми компаниями.
- Интеграция одноразовых систем: Технологии одноразового использования становятся все более популярными в биообработке благодаря таким преимуществам, как гибкость, снижение затрат и более быстрое внедрение. Интеграция одноразовых компонентов в критические этапы процесса обеспечивает возможности для более быстрой и эффективной проверки. Кроме того, модульный характер одноразовых систем позволяет проводить дополнительную валидацию при внедрении новых одноразовых компонентов в существующие валидированные процессы.
- Виртуализация и моделирование in silico: Инструменты моделирования in silico позволяют моделировать биопроцессы в цифровом виде для оптимизации и устранения неполадок. Виртуальная проверка с использованием механистических моделей и искусственного интеллекта может потенциально снизить зависимость от обширных физических испытаний в реальном времени. С помощью цифровой эмуляции производственных процессов игроки биофармы могут совершенствовать протоколы проверки и фокусировать физические запуски на крайних случаях. Это может значительно повысить производительность и скорость.
- Совместные партнерства: Биоперерабатывающие компании вступают в стратегические партнерские отношения с поставщиками технологий, КМО, лабораториями и исследовательскими институтами для повышения их валидационных компетенций и возможностей тестирования. Совместные рамки позволяют использовать специализированный опыт и инфраструктуру партнеров для разработки методов, анализа характеристик, интеграции автоматизации и других потребностей валидации.
Рынок валидации биопроцессов Тренды:
- Оцифровка и безбумажная проверка: Существенной тенденцией является переход к безбумажной валидации с использованием автоматизации, электронных журналов и специализированной ИТ-инфраструктуры. Цифровые инструменты позволяют централизованно управлять данными жизненного цикла проверки безопасным и совместимым образом. Они также расширяют доступ к историческим записям и обмену информацией в режиме реального времени между кросс-функциональными группами для поддержки непрерывной проверки.
- Принципы качества по дизайну (QbD): Фирмы Biopharma расширяют использование качественного дизайна для проверки. QbD облегчает более глубокое понимание процессов для разработки стратегий управления и определения пространств проектирования для обеспечения постоянного качества. Эта научно-обоснованная методология с выпуском в режиме реального времени позволяет перейти от демонстрации соответствия к непрерывной проверке процесса.
- Усовершенствованное аналитическое тестирование: Передовые аналитические инструменты, такие как масс-спектрометрия с высоким разрешением, набирают обороты для характеристики биохимических свойств, примесей и продуктов деградации во время проверки. Кроме того, разрабатываются аналитические наборы для специализированной количественной оценки критических качественных атрибутов, таких как ДНК клеток-хозяев и остаточные белки.
- Сочетание нормативного соответствия: Биофармацевтические компании внедряют более интегрированные стратегии качества и валидации для своих процессов, чтобы обеспечить совместное соблюдение требований нескольких регулирующих органов. Унифицированные протоколы валидации разрабатываются с использованием принципов управления рисками для соответствия требованиям FDA, EMA и ICH.
Рынок валидации биопроцессов:
- Высокие требования к капиталовложениям: Комплексная валидация биопроцессов требует значительных инвестиций в оснащение объектов передовыми инструментами, системами автоматизации и ИТ-инфраструктурой. Меньшие игроки и стартапы могут не иметь достаточного капитала для больших расходов на проверку. Это может помешать им внедрять проверенные процессы, ограничивая возможности роста.
- Длительные сроки утверждения продукции: Сквозная валидация биопроцессов наряду с передачей технологий может продлить сроки одобрения биопрепаратов на несколько месяцев. Обширные испытания также делают введение изменений для оптимизации процессов очень громоздким. Длительные сроки запуска продукта могут ограничить потенциал роста для производителей.
- Неопределенные правила для развивающихся рынков: Неопределенности в отношении нормативных ожиданий по валидации биопроцессов на быстрорастущих развивающихся рынках, таких как Китай, Бразилия и Южная Корея, создают проблемы для производителей. Неопределенные нормы валидации вынуждают компании нести дополнительные расходы для проверки процессов на соответствие местным требованиям при выходе на эти рынки.
Последние события:
Запуск нового продукта:
- В январе 2019 года, Sartorius Stedim BiotechМеждународный поставщик фармацевтического и лабораторного оборудования, который предлагает решения для биофармацевтической промышленности и лабораторий, запустил модульную систему Ambr 250, автоматизированную мини-биореакторную систему для приложений разработки биопроцессов, таких как скрининг клеточных линий, оптимизация процессов и моделирование масштабирования.
Приобретение и партнерство:
- В январе 2021 года Sartorius AG, международный партнер в области биофармацевтических исследований и промышленности, приобрела контрольный пакет акций CellGenix, ведущего мирового поставщика компонентов для культивирования клеток GMP-класса, для расширения своего портфеля носителей клеточной культуры.
- В июне 2020 года, Научный Термо ФишерБиотехнологическая компания приобрела Henogen, вирусный вектор CDMO, чтобы расширить возможности для разработки и производства клеточной и генной терапии.
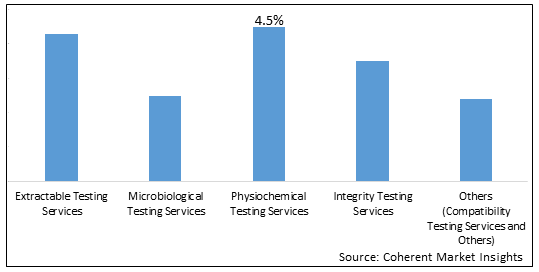
Фигура 2. Доля рынка валидации биопроцессов (%) по типу испытаний, 2023 год
To learn more about this report, request sample copy
Лучшие компании на рынке валидации биопроцессов:
- Sartorius Stedim Biotech
- Merck KGaA
- Корпорация Pall
- Фильтрационное оборудование Cobetter
- Корпорация Toxikon
- DOC S.r.l.
- ФИЛЬТРАЦИОННЫЕ ПРОДУКТЫ МЕЙСНЕР
- Научный Термо Фишер
- SGS SA
- Компания Eurofins Scientific
- Группа компаний LONZA
- ProBioGen AG
- Лаборатории реки Чарльз
- Тихоокеанские биолаборатории
- Гибралтарские лаборатории
- Лаборатории Нельсона
- Технологические консультанты BioProcess
- CMIC HOLDINGS Co., Ltd.
- Cytovance Biologics
- Wuxi Biologics
* Определение: Валидация биопроцессов относится к документально подтвержденным доказательствам и гарантии того, что биофармацевтический процесс последовательно и надежно производит продукты, которые соответствуют заданным спецификациям и стандартам качества. Он включает в себя проверку всех критических аспектов биопроизводства, включая оборудование, объекты, коммунальные услуги, процессы, методы аналитического тестирования и системы автоматизации в соответствии с надлежащей производственной практикой и нормативными руководящими принципами. Валидация биопроцессов является неотъемлемой частью производства биологических препаратов и имеет решающее значение для обеспечения качества, эффективности и безопасности продукции. Это создает уверенность в том, что производственный процесс устраняет дисперсию и последовательно обеспечивает высокое качество продукции.
Несколько других многообещающих отчетов в области биотехнологий Промышленность:
Рынок аутсорсинга биологических препаратов
Биологический рынок
Биофармацевтические препараты рынок
Рынок биоаналогов


