Os produtos biosimilar são suspeitos de continuar a ter um impacto significativo na indústria farmacêutica. Muitos órgãos reguladores estabeleceram diretrizes clínicas para apoiar o desenvolvimento de biosimilars, estabelecendo os requisitos para demonstrar farmacocinética comparável, farmacodinâmica, segurança e eficácia de testes de fase I para testes controlados e randomizados de fase III.
Embora biosimilars não são obrigados a submeter-se a ensaios clínicos intensos para sua aprovação, os dados que demonstram sua semelhança com um biológico original em termos de eficácia clínica e segurança é necessária. A adoção de biosimilars varia de país para país, o que está invariavelmente ligado a questões regulatórias e de acesso ao mercado. Espera-se que o mercado de biosimilars testemunhe um crescimento significativo, devido ao vencimento e à cessação das drogas existentes e à presença de ricos gasoduto de biosimilar produtos especialmente aqueles em fase de fase III.
O tamanho global do mercado de biosimilars foi avaliado em US$ 5.0 bbiliões em 2017, e é esperado para testemunhar um CAGR de 35,2% durante o período de previsão (2018 – 2026).
Global Biosimilars Market Share (%) Análise, por tipo de produto, 2017
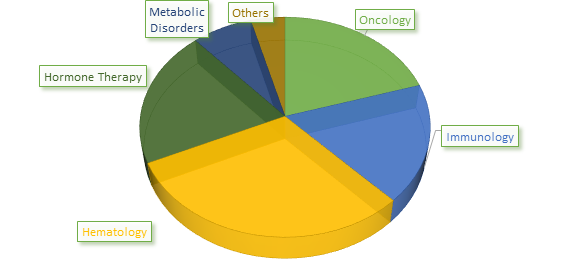
To learn more about this report, request sample copy
Fonte: Análise de Insights de Mercado Coerente (2019)
Espera-se que o aumento do número de aprovações biosimilar impulsione o crescimento do mercado de biosimilars
Aumento do número de aprovado biosimilars devido a maior clareza no processo de revisão da Administração de Alimentos e Medicamentos dos EUA (FDA) além do processo de fabricação e desenvolvimento são esperados para impulsionar o crescimento do mercado de biosimilars. Por exemplo, em julho de 2018, a FDA dos EUA introduziu um Plano de Ação Biosimilars para incentivar o desenvolvimento de biosimilars. Este processo de aprovação incentiva os candidatos a resolver disputas de patentes antes do lançamento de biosimilars.
Além disso, o número de aplicações de biosimilar arquivados aumentou à medida que os fabricantes se tornaram mais confortáveis com os complexos esquemas de regulação e contencioso associados à apresentação de uma aplicação biosimilar. Por exemplo, desde 2015, o FDA dos EUA aprovou 16 biosimilars e o número é esperado para aumentar ao longo do período de previsão. Várias outras agências governamentais também estão seguindo tendências semelhantes para aprovações de produtos. Por exemplo, em novembro de 2017, a Samsung Bioepis recebeu duas aprovações para seu biosimilar adalimumab, Hadlima (SB5) e para seu biosimilar trastuzumab, Samfenet (SB3), do Ministério da Segurança Alimentar e Droga da Coreia (Coreia do Sul).
Mercado de Biosimilars – Restrições
As diretrizes regulamentares rígidas para o desenvolvimento e fabricação de biosimilars nos EUA devem restringir o crescimento do mercado global de biosimilars. Por exemplo, a FDA dos EUA rejeitou quatro aplicações biosimilar durante 2018. Em abril de 2018, a FDA dos Estados Unidos rejeitou o candidato da Pfizer trastuzumab biosimilar e o biosimilar do candidato da Sandoz em maio de 2018.
Além disso, vários desafios de fabricação para biosimilares que surgem principalmente devido à biolÃ3gica ser muito mais estruturalmente complexa e mais difícil de caracterizar, produzir e reproduzir do que a maioria das drogas pequenas-moléculas também são esperados para restringir o crescimento do mercado. Uma pequena variação no processo de fabricação pode potencialmente alterar a segurança e a eficácia do medicamento.
Mercado de Biosimilars - Insights Regionais
Com base na região, o mercado global de biosimilars é segmentado para a América do Norte, América Latina, Europa, Ásia Pacífico, Oriente Médio e África. Espera-se que a Europa seja o mercado mais lucrativo dos biosimilares durante o período de previsão. Espera-se que o aumento do foco dos órgãos reguladores no desenvolvimento de novos biosimilars aumente o crescimento do mercado na Europa. Por exemplo, em julho de 2016, a Agência Europeia de Medicamentos (EMA) autorizou a introdução e comercialização de Thorinane e Inhixa, biosimilares da Heparina de Peso Molecular Baixo (LMWH), enoxaparina.
Espera-se que o tamanho do mercado de biosimilars da Ásia Pacific preveja um crescimento rápido, devido ao aumento significativo do número de aprovações biosimilar. Por exemplo, em 2017, Celltrion recebeu aprovação da China Food and Drug Administration (CFDA) para iniciar ensaios clínicos para sua biosimilar infliximab, Remsima (CT-P13), na China. Isso faz da Celltrion a primeira empresa estrangeira a iniciar ensaios clínicos de um anticorpo biosimilar na China.
Valor Global de Mercado de Biosimilars (US$ Bn) & Y-o-Y Crescimento (%), 2016-2026
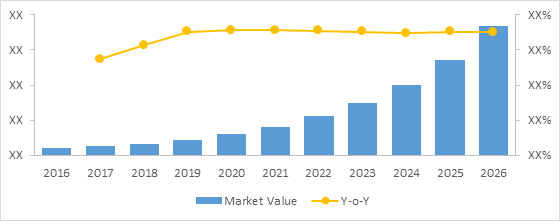
To learn more about this report, request sample copy
Fonte: Análise de Insights de Mercado Coerente (2019)
Mercado Biosimilars - Paisagem Competitiva
Os principais players que operam no mercado global de biosimilars incluem, Novartis AG, Pfizer, Inc., Teva Pharmaceutical Industries Ltd., Celltrion Healthcare Co., Ltd., Biocon Limited, Amgen, Inc., Dr. Reddy's Laboratories e Sanofi S.A.
Share
About Author
Abhijeet Kale
Abhijeet Kale is a results-driven management consultant with five years of specialized experience in the biotech and clinical diagnostics sectors. With a strong background in scientific research and business strategy, Abhijeet helps organizations identify potential revenue pockets, and in turn helping clients with market entry strategies. He assists clients in developing robust strategies for navigating FDA and EMA requirements.
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients