On soupçonne que les produits biosimilaires continuent d'avoir un impact important sur l'industrie pharmaceutique. De nombreux organismes de réglementation ont établi des lignes directrices cliniques pour appuyer le développement de biosimilaires, en établissant les exigences pour démontrer la pharmacocinétique, la pharmacodynamique, l'innocuité et l'efficacité comparables de la phase I aux essais de phase III randomisés contrôlés.
Bien que biosimilaires ne sont pas tenus de subir des essais cliniques intenses pour leur approbation, les données démontrant leur similitude avec un produit biologique original en termes d'efficacité clinique et d'innocuité sont nécessaires. L'adoption de biosimilaires varie d'un pays à l'autre, ce qui est invariablement lié aux questions de réglementation et d'accès aux marchés. Le marché des biosimilaires devrait connaître une croissance importante, en raison de l'expiration et de la cessation des médicaments existants et de la présence de pipeline de biosimilaires produits en particulier ceux de la phase III.
La taille du marché mondial des biosimilaires a été évaluée à 5,0 b dollars des États-UnisIllion en 2017, et devrait être témoin d'un TCAC de 35,2% au cours de la période de prévision (2018-2026).
Mondial Biosimilaires Part de marché (%) Analyse, par type de produit, 2017
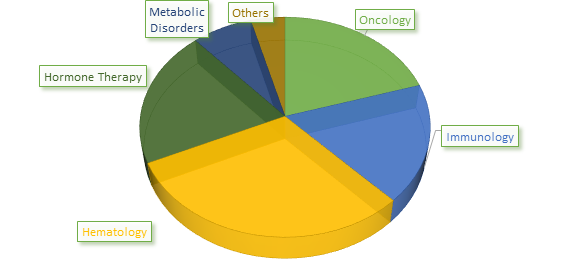
To learn more about this report, request sample copy
Source: Analyse cohérente des perspectives du marché (2019)
Le nombre croissant d'approbations biosimilaires devrait stimuler la croissance du marché des biosimilaires
Augmentation du nombre de projets approuvés biosimilaires En raison d'une plus grande clarté dans le processus d'examen de la Food and Drug Administration (FDA) des États-Unis autres que le processus de fabrication et de développement, on s'attend à ce que les biosimilaires stimulent la croissance du marché. Par exemple, en juillet 2018, la FDA américaine a présenté un plan d'action pour les biosimilaires afin d'encourager le développement de biosimilaires. Ce processus d'approbation encourage les demandeurs à régler les différends relatifs aux brevets avant le lancement des biosimilaires.
De plus, le nombre de demandes de biosimilaires déposées a augmenté à mesure que les fabricants sont devenus plus à l'aise avec les systèmes complexes de réglementation et de litiges associés au dépôt d'une demande de biosimilaires. Par exemple, depuis 2015, la FDA américaine a approuvé 16 biosimilaires et le nombre devrait augmenter au cours de la période de prévision. Plusieurs autres organismes gouvernementaux suivent également des tendances similaires pour l'approbation des produits. Par exemple, en novembre 2017, Samsung Bioepis a reçu deux approbations du Ministère coréen de la sécurité alimentaire et des médicaments (Corée du Sud) pour son adalimumab biosimilar, Hadlima (SB5) et Samfenet (SB3).
Marché des biosimilaires – Restrictions
Aux États-Unis, on s'attend à ce que des lignes directrices réglementaires rigoureuses pour le développement et la fabrication de biosimilaires limitent la croissance du marché mondial des biosimilaires. Par exemple, la FDA américaine a rejeté quatre demandes biosimilaires en 2018. En avril 2018, la FDA des États-Unis a rejeté la candidature de Pfizers trastuzumab biosimilar et de Sandozs rituximab biosimilar en mai 2018.
De plus, plusieurs défis de fabrication pour les biosimilaires qui surviennent principalement parce que les produits biologiques sont beaucoup plus complexes sur le plan structurel et plus difficiles à caractériser, à produire et à reproduire que la plupart des médicaments à petites molécules devraient aussi freiner la croissance du marché. Une petite variation du processus de fabrication peut potentiellement modifier l'innocuité et l'efficacité du médicament.
Marché des biosimilaires - Perspectives régionales
Sur la base de la région, le marché mondial des biosimilaires est segmenté en Amérique du Nord, Amérique latine, Europe, Asie-Pacifique, Moyen-Orient et Afrique. L'Europe devrait être le marché le plus lucratif des biosimilaires au cours de la période de prévision. On s'attend à ce que les organismes de réglementation se concentrent de plus en plus sur le développement de nouveaux biosimilaires pour stimuler la croissance du marché en Europe. Par exemple, en juillet 2016, l'Agence européenne des médicaments (EMA) a autorisé l'introduction et la commercialisation de la thorinane et de l'inhixa, biosimilaires de l'héparine à faible poids moléculaire (LMWH), l'enoxaparine.
On s'attend à ce que la taille du marché des biosimilaires de l'Asie-Pacifique augmente rapidement, en raison du nombre croissant d'approbations de biosimilaires. Par exemple, en 2017, Celltrion a reçu l'autorisation de la China Food and Drug Administration (CFDA) de commencer des essais cliniques pour son infliximab biosimilaire, Remsima (CT-P13) en Chine. Cela fait de Celltrion la première entreprise étrangère à entreprendre des essais cliniques d'un anticorps biosimilaire en Chine.
Biosimilaires mondiaux Valeur de marché (en milliards de dollars É.-U.) et croissance de l'année civile (%), 2016-2026
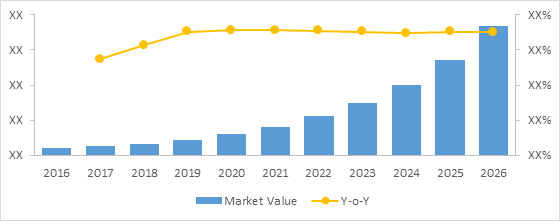
To learn more about this report, request sample copy
Source: Analyse cohérente des perspectives du marché (2019)
Marché des biosimilaires - Paysage concurrentiel
Les principaux acteurs du marché mondial des biosimilaires sont Novartis AG, Pfizer, Inc., Teva Pharmaceutical Industries Ltd., Celltrion Healthcare Co., Ltd., Biocon Limited, Amgen, Inc., Dr Reddy's Laboratories et Sanofi S.A.
Share
About Author
Abhijeet Kale
Abhijeet Kale is a results-driven management consultant with five years of specialized experience in the biotech and clinical diagnostics sectors. With a strong background in scientific research and business strategy, Abhijeet helps organizations identify potential revenue pockets, and in turn helping clients with market entry strategies. He assists clients in developing robust strategies for navigating FDA and EMA requirements.
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients