Die Größe des Bioprozess Validation Market wird voraussichtlich erreichen 460,9 Mio. US$ bis 2030, von 882,4 Mio. US$ im Jahr 2023, wächst mit einem CAGR von 9,7% während des Prognosezeitraums. Bioprozessvalidierung bezieht sich auf den Prozess der Demonstration und Sicherstellung, dass ein biopharmazeutischer Herstellungsprozess Produkte, die vorbestimmte Qualitätsstandards und regulatorische Anforderungen erfüllen, konsequent und zuverlässig produziert. Es umfasst die Validierung kritischer Prozessparameter, Ausrüstung, analytische Prüfmethoden, Reinigungsverfahren, Computersysteme und Einrichtungen. Die Validierung von Bioprozessen ist entscheidend für die Sicherstellung von Drogensicherheit, Wirksamkeit und Qualität. Zu den wichtigsten Faktoren, die das Wachstum der Bioprozessvalidierung fördern, gehören zunehmende FuE-Investitionen in die Pharma- und Biotechnologieindustrie, Wachstum der Biosimilars und Biologik Markt, und günstige Regierungsvorschriften, unter anderem.
Der Bioprozess-Validierungsmarkt wird nach Testtyp, Prozesstyp und Endbenutzer und Region segmentiert. Der Markt wird nach Testtyp in extrahierbare Testdienste, mikrobiologische Testdienste, physikalisch-chemische Testdienste, Integritätstests und andere segmentiert. Das Segment Testtyp entfiel 2022 auf den größten Anteil. Dies ist auf die hohe Annahme von Bioprozessinstrumenten wie Bioreaktoren und Chrom Systeme von biopharmazeutischen Unternehmen zur Validierung ihrer Herstellungsverfahren.
Analyst Ansicht:
- Der Bioprozess-Validierungsmarkt wird in den kommenden Jahren deutlich wachsen. Nordamerika und Europa beherrschen derzeit den Markt aufgrund strenger regulatorischer Anforderungen an die Bioprozessvalidierung. Asien-Pazifik wird jedoch mit dem Ausbau der Produktionskapazitäten für Biosimilar und Biologik in Ländern wie China, Indien und Südkorea am schnellsten Wachstum zeigen.
- Der Markt wird in erster Linie durch die zunehmende Annahme von monoklonalen Antikörpern und rekombinanten Proteinen zur Behandlung verschiedener chronischer Erkrankungen angetrieben. Da Bioprozesse weiter fortgeschritten und komplex werden, wird die Notwendigkeit einer gründlichen Validierung dieser Prozesse weiter steigen. Darüber hinaus wird die kontinuierliche Unterstützung von Regulierungsstellen zur Gewährleistung der Produktqualität und -sicherheit auch die Einführung von Bioprozessvalidierungslösungen vorantreiben.
- Der Markt steht jedoch auch vor Einschränkungen von den hohen Kosten, die mit Validierungsverfahren verbunden sind. Gegründete Validierungsprotokolle und mangelnde ausgebildete Fachkräfte stellen weitere Herausforderungen.
- Dennoch zeigt die Entstehung von Zelltherapie und Gentherapie große Wachstumschancen auf dem Markt. Vertragsdienstleister konzentrieren sich auf die Integration digitaler Werkzeuge zur kontinuierlichen Prozessüberwachung und Echtzeit-Releaseprüfung. Die Einführung fortschrittlicher Analyse- und Modellierungstechniken könnte dazu beitragen, Bioprozesse zu optimieren und zeitnahe Produktzulassungen zu erleichtern. Insgesamt wird mit steigenden biopharmazeutischen FuE-Ausgaben und wachsender Notwendigkeit, eine konsequente Prozessleistung zu gewährleisten, die Nachfrage nach Bioprozessvalidierungslösungen voraussichtlich im kommenden Jahr enorm ansteigen.
Bioprozess Validation Market Regionale Einblicke:
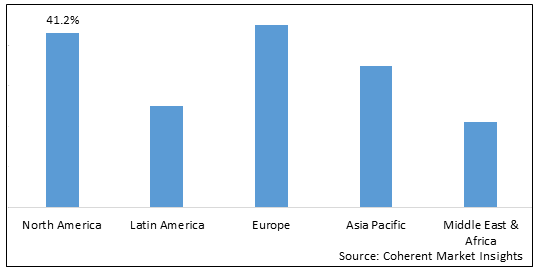
- Nordamerika wird voraussichtlich der größte Markt für Bioprozessvalidierung während des Prognosezeitraums sein, der über 2 % des Marktanteils in 2022. Das Wachstum des Marktes in Nordamerika wird auf das Vorhandensein führender biopharmazeutischer Unternehmen, hoher FuE-Investitionen und strenge regulatorische Anforderungen an die Bioprozessvalidierung in der Region zurückgeführt.
- Europa erwartet wird, dass der zweitgrößte Markt für Bioprozessvalidierung ist, 5 % des Marktanteils 2022. Das Wachstum des Marktes in der Region wird auf die zunehmende Bioproduktion, den steigenden Fokus auf Life Sciences Research und die günstige Regierungsförderung in Europa zurückgeführt.
- Asien-Pazifik wird voraussichtlich der am schnellsten wachsende Markt für Bioprozessvalidierung sein, der eine CAGR von über 19,3% während des Prognosezeitraums. Das Wachstum des Marktes in Asien-Pazifik wird auf den expandierenden biopharmazeutischen Produktionssektor zurückgeführt, die Investitionen in FuE-Infrastruktur und das rasche Wachstum der Outsourcing-Dienstleistungen in der Region erhöht.
Abbildung 1. Globale Bioprozess-Validierungsmarktanteil (%), nach Region, 2023
To learn more about this report, request sample copy
Bioprozess Validation Market Drivers:
- Erhöhung der FuE-Investitionen in Biopharmazeutika: Die biopharmazeutische Industrie verzeichnete in den letzten zehn Jahren ein beträchtliches Wachstum der FuE-Ausgaben. Mehrere Biopharma-Unternehmen haben robuste klinische Pipelines mit zunehmendem Fokus auf die Entwicklung neuartiger Biologen und Biosimilars. Dieser Anstieg der biologen Arzneimittelentwicklung hat anschließend die Notwendigkeit einer umfangreichen Prozesscharakterisierung und Validierung während der präklinischen und klinischen Fertigung gefördert. Darüber hinaus verlangen die Komplexität von Bioprozessen für neuartige Modalitäten wie Zell- und Gentherapien eine höhere Validierungsstrenz, um die Sicherheit und Wirksamkeit von Arzneimitteln zu gewährleisten.
- Wachstum von Biologik und Biosimilars Markt: Der rasch expandierende Markt für Biologika und Biosimilars ist ein wichtiger Faktor für die Validierung von Bioprozessen. Die Zulassung von hochwertigen Biologen für Krebs- und Autoimmunerkrankungen hat weitere eskalierte Bioproduktionsvolumina in der gesamten Branche. Dies schafft eine erhebliche Nachfrage nach validierten Fertigungsprozessen und Analysen, um eine nahtlose Scale-up- und Produktqualitätskonformität zu gewährleisten.
- Erhöhung der Auslagerung durch biopharmazeutische Firmen: Viele Biopharma-Firmen sind strategisch Outsourcing verschiedener bioverarbeitender Tätigkeiten, einschließlich Validierungsdienstleistungen für Vertragsunternehmen. Vertragsfertigungsorganisationen (CMOs) verbessern ihre Serviceangebote, um die Prozesse und Produkte ihrer Sponsoren nachhaltig zu unterstützen. Darüber hinaus ist das Know-how der CMOs bei der Konzeption und Umsetzung von Validierungsprotokollen, die auf regulatorische Erwartungen ausgerichtet sind, ermutigend, Sponsoren zunehmend zu nutzen Outsourcing.
- Investitionen in die Bioprozessinfrastruktur: Wesentliche Investitionen werden von Biopharma-Unternehmen getätigt, um fortgeschrittene Bioverarbeitende Anlagen aufzubauen und ihre Produktionskapazitäten zu verbessern. Die Erweiterung der Produktionskapazitäten für APIs und Biologik erfordert erhebliche Validierungsanforderungen. Darüber hinaus erfordert die Modernisierung von Altanlagen zur Verbesserung der Prozesseffizienz auch eine Revalidierung von Ausrüstung, Methoden und Infrastruktur. Dies trägt wesentlich zur Bioprozessvalidierungsnachfrage bei. Darüber hinaus investieren Marktteilnehmer für die Einführung neuer Ressourcenzentren und dies wird erwartet, dass das Wachstum des globalen Bioprozess-Validierungsmarktes über den Prognosezeitraum vorangetrieben wird. So hat Qosina 2022, ein globaler Lieferant von OEM-Einsatzkomponenten für die medizinische und pharmazeutische Industrie, sein neues Bioprozess Resource Center, eine Informationsquelle für die Bioprozessindustrie, ins Leben gerufen.
Bioprozess Validierung Marktbericht Abdeckung
| Bericht Deckung | Details |
|---|
| Basisjahr: | 2022 | Marktgröße 2023: | US$ 460.9 Mn |
|---|
| Historische Daten für: | 2018 bis 2022 | Vorausschätzungszeitraum: | 2023 - 2030 |
|---|
| Vorausschätzungszeitraum 2023 bis 2030 CAGR: | 9.7% | 2030 Wertprojektion: | US$ 882.4 Mn |
|---|
| Geographien: | - Nordamerika: USA und Kanada
- Lateinamerika: Brasilien, Argentinien, Mexiko und Rest Lateinamerikas
- Europa: Deutschland, U.K., Spanien, Frankreich, Italien, Russland und Rest Europas
- Asia Pacific: China, Indien, Japan, Australien, Südkorea, ASEAN und Rest Asien-Pazifik
- Naher Osten und Afrika: GCC-Länder, Israel, Südafrika, Nordafrika und Zentralafrika und Rest des Nahen Ostens
|
| Segmente: | - Nach Prüftyp: Ausziehbare Testing Services, mikrobiologische Testing Services, Physiochemische Testing Services, Integrity Testing Services und andere (Kompatibilitätstesting Services und andere)
- Durch Prozesskomponenten: Filterelemente, Medienbehälter und Beutel, Gefrier- und Tauvorgangsäcke, Bioreaktoren, Transfersysteme und andere (Mixing Systems and Others)
- Von Endbenutzer: Pharma und Biotechnologie Unternehmen, Organisationen für die Entwicklung und Fertigung, akademische und Forschungsinstitute und andere (Klinische Forschungsorganisationen und andere)
|
| Unternehmen: | Sartorius Stedim Biotech, Merck KGaA, Pall Corporation, Cobetter Filtration Equipment, Toxikon Corporation, DOC S.r.l., MEISSNER FILTRATION PRODUCTs, Thermo Fisher Scientific, SGS SA, Eurofins Scientific, Lonza Group, ProBioGen AG, Charles River Laboratories, Pacific BioLabs, Gibraltar Laboratories, Nelson Laboratories, BioProcess Consultants Technology Ltd. |
| Wachstumstreiber: | - Erhöhung der FuE-Investitionen in Biopharmazeutika
- Wachstum von Biologik und Biosimilars Markt
- Erhöhung der Auslagerung durch biopharmazeutische Firmen
- Investitionen in die Bioprozessinfrastruktur
|
| Zurückhaltungen & Herausforderungen: | - Hohe Investitionsanforderungen
- Dauerhafte Produktzulassungszeiträume
- Undefinierte Regelungen für Schwellenländer
|
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
Bioprozess Validierung Markt Möglichkeiten:
- Automatisierung und Datenanalyse: Automatisierungstechnologien wie Robotik und vernetzte IoT-Systeme bieten enorme Möglichkeiten, die Bioprozessvalidierung zu optimieren und zu beschleunigen. Erweiterte Analytik kombiniert mit Automatisierung kann die Überwachung verbessern, die kontinuierliche Überprüfung erleichtern und schnelle datengesteuerte Entscheidungsfindung während der Validierung ermöglichen. Datenmanagementtechnologien wie Blockchain fördern auch die Datensicherheit und Transparenz zwischen Outsourcing-Partnern.
- Integration von Einwegsystemen: Single-Use-Technologien zeugen von einer verstärkten Akzeptanz bei der Bioverarbeitung aufgrund von Vorteilen wie Flexibilität, reduzierten Kosten und schnellerer Umsetzung. Die Integration von Einwegkomponenten in kritische Prozessschritte ermöglicht eine schnellere und effizientere Validierung. Darüber hinaus ermöglicht der modulare Charakter von Einwegsystemen eine zusätzliche Validierung, wenn neue Einwegkomponenten in bestehende validierte Prozesse eingeführt werden.
- Virtualisierung und in silico Modellierung: In silico Modellierungswerkzeugen ermöglichen die Simulation von Bioprozessen digital zur Optimierung und Fehlerbehebung. Virtuelle Validierung mit mechanistischen Modellen und künstlicher Intelligenz kann möglicherweise die Abhängigkeit von umfangreichen Echtzeit-Erprobungen reduzieren. Durch die digitale Emulation von Fertigungsprozessen können Biopharma-Spieler Validierungsprotokolle verfeinern und physische Abläufe auf Randfällen fokussieren. Dies kann Produktivität und Geschwindigkeit deutlich verbessern.
- Kooperationen: Bioverarbeitende Unternehmen setzen strategische Partnerschaften mit Technologieanbietern, CMOs, Labors und Forschungsinstituten ein, um ihre Validierungskompetenzen und Testkapazitäten zu verbessern. Verbundene Rahmenbedingungen ermöglichen es, das Fachwissen und die Infrastruktur der Partner für die Methodenentwicklung, die Charakterisierungsanalyse, die Automatisierungsintegration und andere Validierungsanforderungen zu nutzen.
Bioprozess Validierung Markt Trends:
- Digitalisierung und papierlose Validierung: Ein wesentlicher Trend ist der Schritt hin zu einer papierlosen Validierung, die Automatisierung, elektronische Logbücher und spezialisierte IT-Infrastruktur nutzt. Digitale Tools ermöglichen eine zentrale Verwaltung von Validierungs-Lebenszyklusdaten sicher und konform. Sie verbessern auch die Zugänglichkeit historischer Aufzeichnungen und den Echtzeit-Informationsaustausch zwischen funktionsübergreifenden Teams, um eine kontinuierliche Überprüfung zu unterstützen.
- Qualität durch Design (QbD) zu optimieren: Biopharma-Unternehmen erhöhen die Verwendung von Qualität durch Design-Ansätze zur Validierung. QbD erleichtert ein tieferes Prozessverständnis zur Festlegung von Steuerungsstrategien und zur Definition von Designräumen, um gleichbleibende Qualität zu gewährleisten. Diese wissenschaftlich fundierte Methodik mit Echtzeit-Release ermöglicht eine Änderung der Validierung von der Nachweis der Compliance bis zur kontinuierlichen Prozessprüfung.
- Verbesserte analytische Tests: Fortgeschrittene analytische Werkzeuge wie hochauflösende Massenspektrometrie gewinnen Traktion zur Charakterisierung biochemischer Eigenschaften, Verunreinigungen und Abbauprodukte während der Validierung. Zusätzlich werden analytische Assaykits zur spezialisierten Quantifizierung kritischer Qualitätsattribute wie Wirtszellen-DNA und Restproteine entwickelt.
- Kombination der regulatorischen Compliance: Biopharmazeutische Unternehmen übernehmen mehr integrierte Qualitäts- und Validierungsstrategien für ihre Prozesse, um die Einhaltung mehrerer Regulierungsbehörden zu ermöglichen. Einheitliche Validierungsprotokolle werden mit Qualitäts-Risikomanagement-Prinzipien entwickelt, um Anforderungen von FDA, EMA und ICH-Richtlinien zu erfüllen.
Bioprozess Validation Market Restraints:
- Hohe Investitionsanforderungen: Umfassende Bioprozessvalidierung erfordert erhebliche Investitionen in Anlagen mit fortschrittlichen Instrumenten, Automatisierungssystemen und IT-Infrastruktur. Kleinere Biopharma-Spieler und Startups haben möglicherweise kein ausreichendes Kapital für große Validierungsausgaben. Dies kann sie von der Umsetzung validierter Prozesse zurückhalten und die Wachstumschancen begrenzen.
- Längere Produktzulassungszeiten: Die End-to-End-Validierung von Bioprozessen sowie Technologietransfer-Aktivitäten können die regulatorischen Genehmigungsfristen der Biologik um mehrere Monate verlängern. Die umfangreichen Studien macht die Einführung von Modifikationen zur Optimierung von Prozessen auch sehr umständlich. Die daraus resultierenden langen Produktstartzeitlinien können das Wachstumspotenzial für die Hersteller einschränken.
- Undefinierte Regelungen für Schwellenländer: Ungewissheiten rund um regulatorische Erwartungen an die Bioprozessvalidierung in aufstrebenden Märkten wie China, Brasilien und Südkorea stellen Herausforderungen für Hersteller. Undefinierte Validierungsnormen zwingen Unternehmen, zusätzliche Kosten zu tragen, um Prozesse zu revalidieren, um den lokalen Anforderungen bei der Expansion in diese Märkte gerecht zu werden.
Aktuelle Entwicklungen:
Neue Produkte:
- Im Januar 2019, Sartorius Stedim Biotech, ein internationaler Anbieter von pharmazeutischen und Laborgeräten, der Lösungen für die biopharmazeutische Industrie und Labore anbietet, ambr 250 modular, ein automatisiertes Mini-Bioreaktorsystem für Bioprozessentwicklungsanwendungen wie Zelllinien-Screening, Prozessoptimierung und Scale-up-Modellierung
Erwerb und Partnerschaften:
- Im Januar 2021 erwarb die Sartorius AG, ein internationaler Partner für biopharmazeutische Forschung und Industrie, eine Mehrheitsbeteiligung an CellGenix, einem weltweit führenden Anbieter von Zellkulturkomponenten der GMP-Klasse, um ihr Zellkultur-Medienportfolio zu erweitern
- Im Juni 2020 Thermo Fisher Scientific, ein Biotechnologie-Unternehmen, erworben Henogen, ein viraler Vektor CDMO, um Fähigkeiten für Zell- und Gentherapie Entwicklung und Herstellung zu erweitern
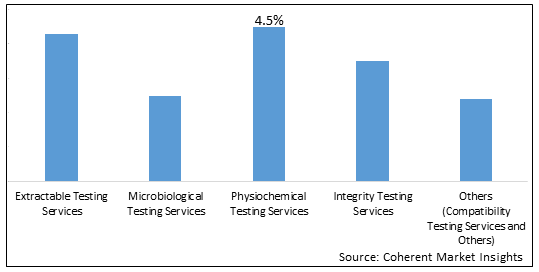
Abbildung 2. Globale Bioprozess-Validierungsmarktanteil (%), nach Testtyp, 2023
To learn more about this report, request sample copy
Top-Unternehmen im Bioprozess Validation Market:
- Sartorius Stedim Biotech
- Warenbezeichnung
- Pall Corporation
- Cobetter Filtrationsanlagen
- Toxikon Corporation
- DOC S.r.l.
- MEISSNER FILTRATIONSPRODUKTE
- Thermo Fisher Scientific
- SGS SA
- Eurofins Wissenschaftlich
- Lonza Group
- ProBioGen AG
- Charles River Laboratories
- Pazifik BioLabs
- Gibraltar Laboratories
- Nelson Laboratories
- BioProcess Technology Consultants
- CMIC HOLDINGS Co., Ltd.
- Cytovance Biologics
- Wuxi Biologistik
*Definition: Bioprozessvalidierung bezieht sich auf den dokumentierten Nachweis und die Gewissheit, dass ein biopharmazeutischer Prozess Produkte, die vorgegebenen Spezifikationen und Qualitätsstandards entsprechen, konsequent und zuverlässig produziert. Es umfasst die Validierung aller kritischen Aspekte der Bioproduktion, einschließlich Ausrüstung, Einrichtungen, Versorgungsunternehmen, Prozesse, analytische Testmethoden und Automatisierungssysteme nach bewährten Fertigungsmethoden und regulatorischen Richtlinien. Bioprozessvalidierung ist ein wesentlicher Bestandteil der Biologikherstellung und ist entscheidend für die Gewährleistung von Produktqualität, Wirksamkeit und Sicherheit. Es baut Vertrauen, dass der Herstellungsprozess die Varianz eliminiert und konstant hohe Qualitätsausgänge liefert.
Nur wenige weitere Promising-Berichte in der Biotechnologie Industrie:
Biologics Outsourcing Markt
Biologistik Markt
Biopharmazeutika Markt
Biosimilars Markt


