Généothérapie pour le marché des maladies rares - Insights
La thérapie génique implique l'insertion de matériel génétique dans les cellules des patients pour fournir une nouvelle fonction ou pour restaurer le fonctionnement manquant ou inapproprié des cellules en raison du cancer ou des mutations génétiques. Selon le Centre national pour l'avancement des sciences de la traduction, bien qu'environ 7 000 maladies rares soient identifiées, quelques centaines seulement ont des traitements approuvés. De plus, le développement de la thérapie génique pour les maladies rares gagne en traction significative, car plus de 80% des maladies rares ont une cause monogénique connue (single-gene). Les médicaments à petites molécules ne traitent souvent que les symptômes plutôt que de guérir la cause sous-jacente de la maladie. Cela nécessite l'administration fréquente des médicaments pour gérer l'état. La thérapie génique peut corriger les défauts génétiques sous-jacents. De plus, un son clinique et un succès thérapie génique peut seulement nécessiter une dose unique pour guérir une maladie plutôt qu'un traitement à vie. Les thérapies géniques approuvées commercialement comprennent Kymriah (Novartis AG), Yescarta (Gilad Sciences, Inc.), Luxturna (Spark Therapeutics) et Strimvelis (Orchard Therapeutics).
L'augmentation de l'approbation des médicaments et le lancement de nouvelles thérapies génétiques pour le traitement de diverses maladies rares devraient stimuler la croissance du marché des maladies rares au cours de la période de prévision.
Récemment, les principaux acteurs du marché ont obtenu des approbations réglementaires et lancé leurs thérapies sur le marché. On s'attend à ce que les approbations fréquentes de nouvelles thérapies génétiques et de leur lancement dans les régions développées stimulent de façon significative la croissance du marché des maladies rares au cours de la période de prévision. Par exemple, en décembre 2017, Spark Therapeutics, Inc. a reçu l'approbation de la Food and Drug Administration (FDA) des États-Unis pour son LUXTURNA (voretigène néparvovec-rzyl), un produit de thérapie génique unique indiqué pour le traitement de patients présentant une dystrophie rétinienne associée à une mutation de la RPE65 confirmée. En outre, en août 2018, Novartis International AG a reçu l'approbation de la Commission européenne (CE) pour le kymriah (tisagenlecleucel, anciennement CTL019) indiqué pour le traitement des patients jusqu'à 25 ans atteints de leucémie aiguë lymphoblastique (LAL) à rechute ou réfractaire et pour le traitement des patients adultes atteints de lymphome à grandes cellules B (DLBCL) à rechute ou réfractaire (r/r) après deux ou plusieurs lignes de traitement systémique. De plus, en août 2018, Kite Pharma, Inc., une société de Galaad, a reçu l'approbation de la Commission européenne (CE) pour la commercialisation de son nouveau Yescarta (axicabtagene ciloléucel), en tant que traitement pour les patients adultes atteints d'un lymphome à grandes cellules B rechute ou réfractaire diffuse (DLBCL) et d'un lymphome à grandes cellules B (PMBCL) à médiation primaire, après deux lignes de traitement systémique ou plus.
La thérapie génique globale pour la taille du marché des maladies rares a été évaluée à 16,3 millions de dollars des États-Unis en 2017, et devrait être témoin d'un TCAC robuste de 35,0% au cours de la période de prévision (2018-2026).
Figure no 1 : Généothérapie mondiale pour la part de marché des maladies rares, selon le médicament (%), 2018 -2026 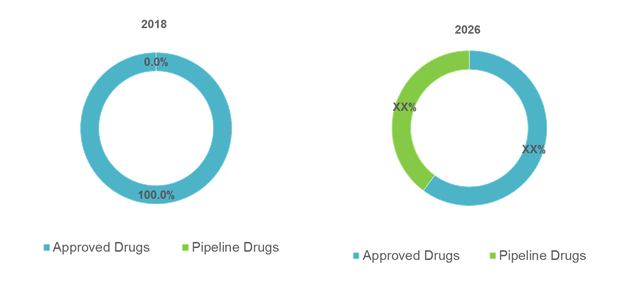
To learn more about this report, request sample copy
Source: Analyse cohérente des perspectives du marché (2018)
La recherche et le développement en cours dans le domaine des thérapies génétiques pour les maladies rares devraient stimuler la croissance du marché mondial de la thérapie génique pour les maladies rares
La présence de plusieurs thérapies géniques nouvelles pour divers traitements des maladies rares en cours d'élaboration, qui devraient être approuvées, devrait stimuler la croissance du marché au cours de la période de prévision. Par exemple, Spark Therapeutics, Inc. est en train de développer une thérapie génique, à savoir Fidanacogene Elaparvovec, une nouvelle thérapie génique expérimentale indiquée pour le traitement des patients souffrant d'hémophilie B. Actuellement, le traitement fait l'objet d'un essai clinique de phase 3 et devrait être approuvé prochainement. En août 2018, UniQure N.V. a traité le premier patient Étude de phase IIb de confirmation de la dose d'AMT-061, une thérapie génique à base d'AAV5 expérimentale intégrant la variante FIX-Padua pour le traitement de patients atteints d'hémophilie B sévère et modérément sévère.En mai 2018, Orchard Therapeutics Plc. a reçu la désignation de maladie pédiatrique rare de la Food and Drug Administration (FDA) des États-Unis pour son candidat à la thérapie génique OTL-200, indiqué pour le traitement de patients atteints de leucodystrophie métachromatique (LMD). PTC Thérapeutique, In. a GT-AADC dans la phase 3 essais cliniques et est indiqué pour la carence en L-Amino Acid Décarboxylase (AADC).
Tableau 1 : Généothérapie pour les maladies rares
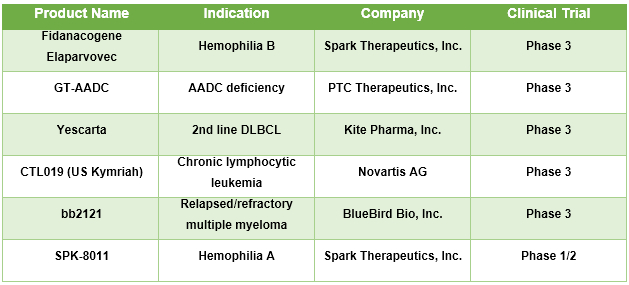
To learn more about this report, request sample copy
Source: Site Web de l'entreprise, Clinicaltrials.gov
Toutefois, le manque de sensibilisation de la population au sujet des maladies rares et de leur traitement devrait avoir une incidence négative sur la croissance de la thérapie génique sur le marché des maladies rares. Par exemple, en 2017, UniQure N.V. a abandonné sa plante pour poursuivre le renouvellement de sa thérapie génique Glybera, qui a été approuvée en 2012, pour le traitement d'un petit sous-ensemble de patients atteints d'un déficit familial en lipoprotéine lipase (PLLD). La société a abandonné son plan en raison de la très faible demande de thérapie sur le marché
Parmi les principaux acteurs du marché mondial de la thérapie génique pour les maladies rares, citons Kite Pharma, Inc. (Gilead Sciences, Inc.), Novartis International AG, Juno Therapeutics Inc. (Celgene Corporation), Bluebird Bio, Inc., Spark Therapeutics, Inc., uniQure N.V, Orchard Therapeutics Plc., PTC Therapeutics, Inc. et BioMarin Pharmaceutical Inc.
Share
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients