Die Bioburden-Tests Marktgröße wird bei US$ 1.40 Bn in 2024 und wird voraussichtlich erreichen US$ 2.59 Bn von 2031Wachstumsrate (CAGR) von 9,2% von 2024 bis 2031. Bioburden-Tests sind ein wichtiger Bestandteil der Gewährleistung der Sicherheit von pharmazeutischen und medizinischen Produkten. Es geht um die Detektion und Quantifizierung von Mikroorganismen, die als Verunreinigungen vorliegen können. Es gibt zwei Haupttypen von Bioburden-Tests: mikrobielle Aufzählung und Identifizierung. Mikroben Aufzählungstests sollen die Anzahl der in oder auf einem Produkt, einem Behälter oder einer Oberfläche vorhandenen lebensfähigen Mikroorganismen zählen. Dies geschieht typischerweise durch Inkubation einer Probe und Zählung aller Kolonien, die wachsen. Identifizierungstests helfen dabei, die vorhandenen spezifischen Mikroorganismen zu bestimmen.
Diese Tests sind kritisch, da übermäßige Bioburden die Sterilität von Arzneimitteln und medizinischen Geräten beeinträchtigen können, die steril sein sollen. Die mikrobielle Kontamination stellt Risiken wie Toxizität, Veränderung von Medikamenteneigenschaften, Infektionen bei Patienten und Ablehnung von gesamten Fertigungsansätzen dar. Die Vorteile von Bioburden-Tests umfassen die Gewährleistung der Produktqualität und -sicherheit Unterschiedliche Testmethoden werden je nach Produkttyp und potenziellen Mikroben von Belang eingesetzt. Automatisierte schnelle Methoden haben die Prüfung effizienter und kostengünstiger im Vergleich zu herkömmlichen mikrobiologischen Plattenzählungen. Solche Verfahren können jedoch den Empfindlichkeits- und Differenzierungsfähigkeiten herkömmlicher Techniken fehlen. Die Auswahl des Prüfverfahrens hängt von der Abgleichgeschwindigkeit, Genauigkeit und Empfindlichkeitsanforderungen in der jeweiligen Anwendung ab.
Bioburden Testing Market Regional Insights:
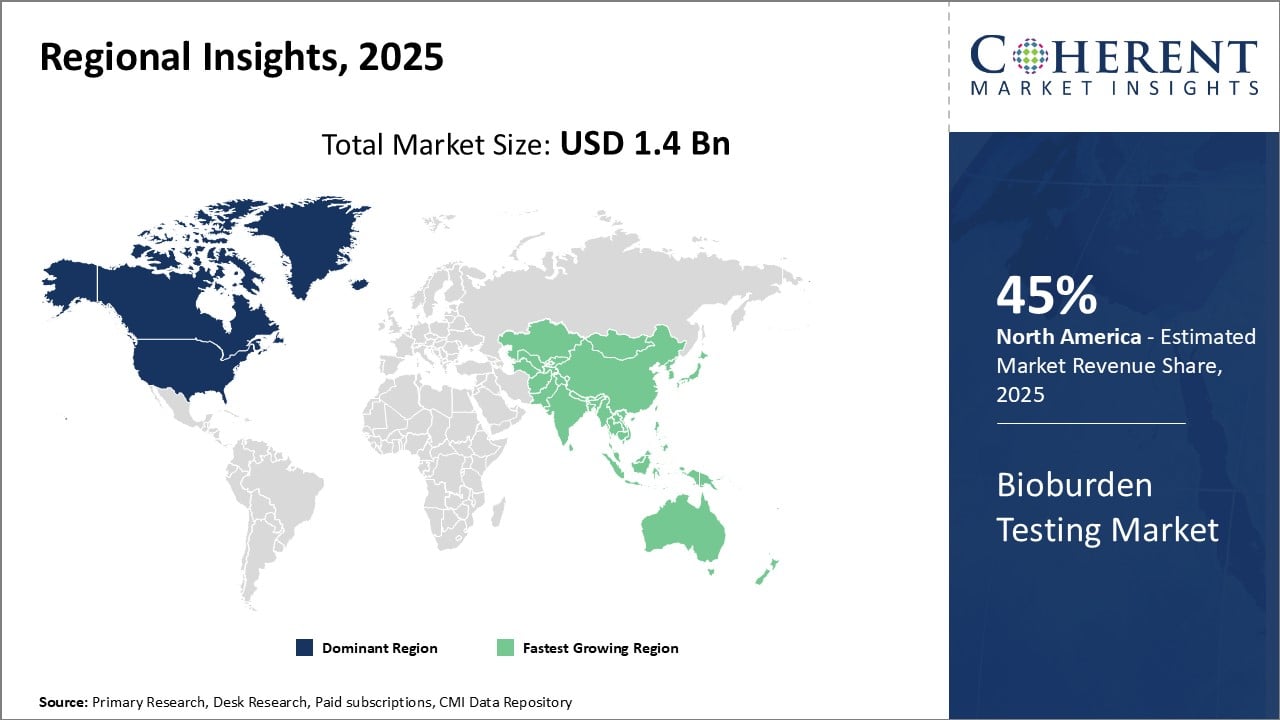
- Nordamerika: Nordamerika hat den globalen Bioburden-Testmarkt mit einer Präsenz von 45 % dominiert und erwartet, dass er seine führende Position in den kommenden Jahren fortsetzen wird. Dies kann auf die starke Präsenz von Pharma- und Biotech-Unternehmen in Ländern wie den USA zurückzuführen sein. Die Region ist die Heimat von Top-Unternehmen in der Pharmaindustrie, die sich kontinuierlich auf neue Arzneimittelentwicklung und strenge Qualitätsstandards konzentrieren. Dies hat die Nachfrage nach Bioburden-Tests, um die Sicherheit und Wirksamkeit von Medikamenten zu gewährleisten. Darüber hinaus haben etablierte Regelungen zur Qualitätskontrolle und Standardisierung durch Regulierungsbehörden wie die FDA Bioburden-Tests für verschiedene medizinische Produkte beauftragt, die das Marktwachstum weiter unterstützen.
- Europa hält die zweite Position in Bezug auf Marktanteil aufgrund der Anwesenheit von großen Drogenherstellern. Auch strenge medizinische Vorschriften, die von der Europäischen Medizinischen Agentur festgelegt werden, treiben die Umsetzung von Bioburdentests auf verschiedenen Fertigungsstufen voran.
- Asien-Pazifik wird durch den Ausbau der Pharmaindustrie in Ländern wie China, Indien und Südkorea als der am schnellsten wachsende regionale Markt anerkannt. Anbau Generelles Medikament Die Produktion sowie das Vorhandensein von Kontraktherstellungsorganisationen in diesen Ländern bieten vielfältige Möglichkeiten für Bioburden-Testanbieter. Asien-Pazifik-Länder betonen auch Qualitätsstandards, um den Zugang zu globalen Märkten zu gewährleisten. Dies hat die Einführung von Bioburden-Testlösungen weiter katalysiert. Die Steigerung der Gesundheitsausgaben und die Sensibilisierung der Gesundheitsversorgung haben auch eine entscheidende Rolle in der Marktentwicklung gespielt. Viele internationale Akteure setzen Fertigungsanlagen ein und arbeiten mit regionalen Unternehmen zusammen, um Wachstumschancen zu nutzen. Dies hilft beim Technologietransfer und der Entwicklung von Testinfrastrukturen, um die steigende Nachfrage zu decken.
Abbildung 1. Bioburden Testing Market Share (%), nach Region, 2024
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Analyst Viewpoint:
Der Bioburden-Testmarkt wird in den kommenden Jahren deutlich wachsen. Die steigenden regulatorischen Standards für biopharmazeutische und medizinische Gerätehersteller zur Beurteilung mikrobieller Verunreinigungen in Rohstoffen und Fertigprodukten haben eine erhöhte Nachfrage nach Bioburden-Tests. Darüber hinaus wird die rasche Expansion der biopharmazeutischen Industrie und des wachsenden Generika-Markts die Anforderungen an die Compliance-Tests erhöhen. Nordamerika dominiert derzeit den Markt aufgrund etablierter regulatorischer Rahmenbedingungen und einer beträchtlichen Biomanufakturindustrie in der Region. Asien-Pazifik wird aufgrund positiver wirtschaftlicher und regulatorischer Bedingungen, die die Produktion von Biosimilars in Ländern wie China, Indien und Südkorea beschleunigen, der am schnellsten wachsende Markt sein.
Allerdings können hohe Investitionsanforderungen an strenge Pathogentestinstrumente wie PCR-Maschinen und automatisierte Schnellerkennungssysteme das Marktwachstumspotenzial teilweise zurückhalten, insbesondere bei kleinen und mittleren Unternehmen in preissensitiven Entwicklungsmärkten. Eine zunehmende Einführung von kontinuierlichen Überwachungssystemen anstelle von diskontinuierlichen Tests könnte den Lieferanten die Möglichkeit bieten, wiederkehrende Einnahmenströme zu gewinnen. Die Entwicklung schneller Bioburden-Tests vor Ort kann Herstellern, die schnellere Ergebnisse suchen, ansprechen, ohne die Genauigkeit zu gefährden. Die Outsourcing von Testdiensten wird voraussichtlich steigen, da sie die Hersteller von erstklassigen Ressourcen- und Gerätekosten entlastet.
Bioburden Testing Market Drivers:
Strict Regulations for Bioburden Testing
Die Regierungsverordnungen spielen eine große Rolle beim Fahren der Notwendigkeit einer bioburden Prüfung von pharmazeutischen und medizinischen Geräten. Regulatorische Körper weltweit haben strenge Normen und Richtlinien umgesetzt, um die Produktsicherheit und Qualität zu gewährleisten. So hat die US-FDA klare Spezifikationen für mikrobielle Grenzwerte für parenterale und andere medizinische Produkte festgelegt. Auch in den EU- und anderen entwickelten Märkten müssen Vorschriften für mikrobielle Verunreinigungen in Fertigungsumgebungen, Rohstoffen und fertigen medizinischen Gütern geprüft werden.
Die Einhaltung solcher Regulierungsstandards ist für Unternehmen unerlässlich geworden. Selbst ein einziger Bericht der Infektion durch Kontamination kann den Ruf einer Marke beschädigen und schwere Kosten verursachen. So verbringen Hersteller erhebliche Zeit und Ressourcen für die Umwelt- und Personalüberwachung sowie Produkttests. Geförderte Bioburden-Tests werden in verschiedenen Phasen durchgeführt, von der Rohmaterialaufnahme bis zur Sterilisationsvalidierung. Fortgeschrittene automatisierte Geräte und schnelle Methoden werden verwendet, um auch die minimalen mikrobiellen Ebenen innerhalb von festgelegten Zeitlinien zu erkennen. Jede Nichteinhaltung kann schwere Strafen anziehen und zukünftige Clearancen beeinträchtigen. Dies hat es für Qualitätskontrollteams wichtig gemacht, sich auf zuverlässige und validierte Bioburdentests zu verlassen, um globale Qualitätsnormen zu erfüllen.
Starke Regulierungsaufsicht in Verbindung mit den Risiken von Nichteinhaltungsantrieben setzte Investitionen in den Bioburden-Testmarkt fort. Da die Vorschriften mit wechselnden Paradigmen strenger werden, werden innovative Testlösungen, die einen höheren Durchsatz und eine höhere Genauigkeit ermöglichen, mehr Nachfrage sehen. Unternehmen müssen die Sicherheit ihrer Betriebe und Produkte durch sorgfältige Dokumentation von Bioburden-Testdaten konsequent nachweisen. Dies hilft, das Vertrauen der Kunden zu erhalten und bleibt für die Aufrechterhaltung ihrer Marktposition kritisch. So sorgt das sich entwickelnde regulatorische Umfeld für ein stetiges Wachstum der globalen Bioburden-Testindustrie.
wachsende Nachfrage nach Outsourcing von Testing Services
Bioburden-Tests erfordern spezialisierte mikrobiologische Expertise und erweiterte Laborinfrastruktur. Die Einrichtung eines hauseigenen Mikrobiologielabors und die Aufrechterhaltung auf globalen Standards erfordert jedoch erhebliche Kapital- und wiederkehrende Investitionen. Es umfasst auch ständig Schulungspersonal zur Entwicklung von Testtechniken und Compliance-Praktiken. Für viele mittelständische und kleinere Unternehmen scheint die Einrichtung solcher Anlagen unter Berücksichtigung ihrer Produktionsmengen nicht finanziell tragfähig zu sein.
Gleichzeitig sind die Outsourcing-Testanforderungen mit Qualitäts- und Zeitlinienrisiken erfüllt. Es besteht eine ständige Notwendigkeit, die Fähigkeiten der Dienstleister zu überwachen und eine reibungslose Koordinierung sicherzustellen. Diese Herausforderung wurde jedoch in jüngster Zeit von einer wachsenden Zahl von Good Laboratory Practice (GLP) zertifizierten Full-Service-Vertragsforschungsorganisationen (CROs) mit Bioburden-Tests angesprochen. Sie bieten einen zentralen Laboraufbau und ein Team von gut qualifizierten Wissenschaftlern für alle Arten von mikrobiologischen Testanforderungen. Die CROs helfen, die Rüstkosten zu senken und die Risiken von unvorhersehbaren internen Verzögerungen oder Nichteinhaltungen durch regulierte Labormitarbeiter zu beseitigen.
Die Einhaltung von CROs ermöglicht es Unternehmen auch, Ressourcen auf ihre Kernproduktions- und Marketingkompetenzen zu konzentrieren. Outsourcing entfernt die Notwendigkeit von Investitionen und Ressourcen für den Betrieb und die Aufrechterhaltung der internen Testinfrastruktur. Es bietet Zugang zu den neuesten analytischen Techniken und flexiblen Kapazitäten. Darüber hinaus bieten CRO-Zertifikate und Datenintegritätsprogramme eine höhere Glaubwürdigkeit für Audits und Einreichungen. Da mehr Unternehmen diese operativen und Compliance-Vorteile erkennen, steigt die Nachfrage nach ausgelagerten Bioburden-Tests in der Branche weiter an. Dieser zunehmend einflussreiche Trend sorgt für ein stetiges Wachstum dieses Marktes.
Bioburden Testing Market Möglichkeiten:
- Erweiterung der Pharma- und Biotech-Industrie in Schwellenländern : Die schnell wachsenden Pharma- und Biotechnologie-Industrien in Schwellenländern wie Indien, China, Brasilien und anderen stellen eine große Chance für den Ausbau von Bioburden-Testdienstleistungen dar. Diese Entwicklungsländer sehen ein beträchtliches Wirtschaftswachstum, das größere Investitionen in die Gesundheits- und Drogenentwicklung ermöglicht. So hat sich die Gesamtausgaben der Gesundheitsversorgung in Prozent des BIP in den letzten zehn Jahren in vielen Entwicklungsländern deutlich erhöht. Die Gesundheitsausgaben in Indien sind von nur 3,5 % des BIP im Jahr 2000 auf etwa 5 % im Jahr 2020 gestiegen.
- Wachsende Nachfrage nach nicht-pharmazeutischen Anwendungen von Bioburden-Tests: Die steigende Nachfrage nach Bioburden-Tests in nicht-pharmazeutischen Anwendungen stellt eine bedeutende Wachstumsmöglichkeit in dieser Branche dar. Bioburden-Tests sind nicht mehr nur auf die Herstellung von pharmazeutischen und medizinischen Geräten beschränkt, da Industrien wie Lebensmittel und Getränke, Kosmetik, Luft- und Raumfahrt und Automobil nun die Bedeutung einer strengen Qualitätskontrolle und Sicherheit erkennen. Mit einer wachsenden globalen Bevölkerung und steigenden Einkommen nimmt die Nachfrage nach verarbeiteten und verpackten Lebensmitteln und Getränken rapide zu. Verbraucher sind sich der Produktqualität und Hygiene bewusst und setzen mehr Druck auf Marken, um robuste Sicherheitspraktiken umzusetzen. Jede Verunreinigung könnte zu Krankheitsausbrüchen und dem Verlust von Leben führen. Die UN-Food and Agriculture Organization (FAO) schätzt, dass fast 1 von 10 Menschen jedes Jahr vom Verzehr kontaminierter Lebensmittel krank werden. Um solche Vorkommnisse zu verhindern und das Vertrauen der Verbraucher zu stärken, investieren Unternehmen mehr in die bioburden Prüfung von Inhaltsstoffen, Verpackungsmaterialien und Fertigprodukten. Der Bioburden-Testmarkt wird in den nächsten 5 Jahren in der Lebensmittelindustrie deutlich wachsen. So prognostiziert der globale Bericht der UN-Wirtschaftskommission bis 2030 einen fünffachen Anstieg der biobasierten Produktproduktion.
Bioburden Testing Market Report Coverage
| Bericht Deckung | Details |
|---|
| Basisjahr: | 2023 | Marktgröße 2024: | US$ 1.40 Bn |
|---|
| Historische Daten für: | 2019 bis 2023 | Vorausschätzungszeitraum: | 2024 - 2031 |
|---|
| Vorausschätzungszeitraum 2024 bis 2031 CAGR: | 9.2% | 2031 Wertprojektion: | US$ 2.59 Bn |
|---|
| Geographien: | - Nordamerika: USA und Kanada
- Lateinamerika: Brasilien, Argentinien, Mexiko und Rest Lateinamerikas
- Europa: Deutschland, U.K., Spanien, Frankreich, Italien, Russland und Rest Europas
- Asia Pacific: China, Indien, Japan, Australien, Südkorea, ASEAN und Rest Asien-Pazifik
- Naher Osten: GCC Länder, Israel und Naher Osten
- Afrika: Südafrika, Nordafrika und Zentralafrika
|
| Segmente: | - Nach Produkt: Verbrauchsmaterialien, Kulturmedien, Reagenzien und Kits, Instrumente, Automatisierte mikrobielle Identifikationssysteme, PCR Instrumente
- Nach Prüftyp: Aerobic Count Testing, Anaerobic Count Testing, Fungi/Mold Count Testing, Spore Count Testing
- Durch Anwendung: Rohmaterialprüfung, Medizinische Geräteprüfung, In-Process-Materialprüfung, Sterilisations-Validierung Testing, Ausrüstung Reinigung Validierung
- Von Endbenutzer: Pharma und Biotechnologie Unternehmen, Medizinproduktehersteller, Contract Manufacturing Organizations, Hersteller von Lebensmittel- und Getränke- und Agrarprodukten, Mikrobielle Testlaboratorien
|
| Unternehmen: | Charles River Laboratories International, Inc., SGS SA, Merck KGaA, Becton Dickinson and Company, Wuxi Apptec, North American Science Associates Inc., Nelson Laboratories, LLC, Biomérieux SA, Thermo Fisher Scientific and Pacific Biolabs |
| Wachstumstreiber: | - Strict Regulations for Bioburden Testing
- wachsende Nachfrage nach Outsourcing von Testing Services
|
| Zurückhaltungen & Herausforderungen: | - Hohe Liebe der Fachkräfte
- Kapitalanlage für analytische Instrumente
|
Entdecken Sie Makros und Mikros, die anhand von über 75 Parametern geprüft wurden, Sofortigen Zugriff auf den Bericht erhalten
Bioburden Testing Market Trends:
- steigende Nachfrage nach On-line- und In-Process-Bioburden-Überwachung: Die steigende Nachfrage nach On-line- und In-Process-Bioburden-Überwachung hat einen erheblichen Einfluss auf den Bioburden-Testmarkt. Mit der immer komplexer werdenden Biologik und Zelltherapie-Produktion liegt der Fokus auf der Sicherstellung der Sterilität und der Minimierung von Verunreinigungen durch den gesamten Herstellungsprozess von Zellkultur bis zur endgültigen Medikamentenproduktfüllung. Eine frühzeitige und Echtzeit-Erkennung von mikrobiellen Verunreinigungen ermöglicht es Unternehmen, sofortige Korrekturmaßnahmen zu ergreifen, um wertvolle Produktansätze zu vermeiden. Bioburden-Monitoring-Technologien von On-line und in-Prozess ermöglichen es, innerhalb der Fertigungsstätte Prüfrecht zu testen, ohne Proben in ein externes Labor zu übertragen. Zeitgemäße Bioburden-Daten ermöglichen engere Prozesssteuerungen und helfen, aseptische Bedingungen zu erhalten. Einige Biologen, wie bispezifische Antikörper, sind inhärent anfällig für die Aggregatbildung, die durch eine schnellere Reaktion auf jede mikrobielle Detektion reduziert werden könnte. In der Lage sein, Verunreinigungen innerhalb von 2448 Stunden zu identifizieren, im Vergleich zu den Ergebnissen für über eine Woche zu warten, verbessert die Fähigkeit eines Unternehmens, enge Prozessentwicklung Zeitlinien zu erfüllen. So investierten Biopharmazeutische Firmen in den USA nach Angaben der Pharmaforschung und der Hersteller von Amerika (PhRMA) 2021 in Forschung und Entwicklung (FuE). Diese erheblichen Investitionen wären auf verschiedene FuE-Tätigkeiten ausgerichtet gewesen, einschließlich der Stärkung der Prozessautomatisierung und der Qualitätsprüfinfrastruktur.
- Erhöhung der Integration von KI und IoT in Bioburden-Testinstrumenten : Die Integration von künstlicher Intelligenz (AI) und Internet von Dingen (IoT) Technologien hat einen tiefen Einfluss auf den Bioburden-Testmarkt. Diese Technologien ermöglichen eine Echtzeitüberwachung und Automatisierung, die höhere Effizienz treibt. Bioburden-Testgeräte mit IoT-Sensoren können Umgebungsparameter wie Temperatur, Feuchtigkeit und Partikelzahl in unkontrollierten Fertigungsumgebungen kontinuierlich überwachen. Die gesammelten Daten werden dann mit AI-Algorithmen analysiert, um Abweichungen und Compliance-Probleme zu erkennen. Dadurch wird sichergestellt, dass die Prüfung auf Ausrüstung und Materialien unter den richtigen Bedingungen durchgeführt wird, wodurch die Notwendigkeit einer erneuten Prüfung von Proben beseitigt wird, wodurch erhebliche Zeit und Kosten eingespart werden. Die Kombination von KI und IoT verbessert auch die automatisierte Probenhandhabung in Bioburden-Testinstrumenten. Vision-Systeme, die durch maschinelles Lernen betrieben werden, können Proben automatisch mit hoher Genauigkeit identifizieren und sortieren. Versuche können bei der Detektion der Probe ohne menschliches Eingreifen eingeleitet werden. Live-Videoüberwachung und Remote-Instrument-Betrieb mit IoT verbessern die Arbeitsabläufe weiter, indem Tests von jedem Standort eingerichtet und überwacht werden können. Dies führt zu reduzierten Turn-Around-Zeiten sowie einer optimierten Ressourcennutzung. Beispielsweise verbindet die Sartorius Digital Bioburden Testing Platform Instrumente über IoT, um zentralisierte Probenverwaltung, Video-basierte Remote-Hilfe und automatisierte Datenanalysefunktionen mittels KI bereitzustellen.
Bioburden Testing Market Restraints:
- Hohe Kapitalanlage für analytische Instrumente: Die für analytische Instrumente erforderlichen hohen Kapitalanlagen sind einer der Hauptfaktoren, die das Wachstum des Bioburden-Testmarktes zurückhalten. Die Einrichtung eines Prüflabors mit fortschrittlichen analytischen Instrumenten wie PCR-Maschinen, molekulardiagnostischen Systemen, Nukleotidsequenzierungsplattformen usw. erfordert einen enormen anfänglichen Kapitalaufwand. Diese anspruchsvollen Instrumente kosten überall zwischen 50.000 US$ und 500.000 US$, je nach technischen Spezifikationen und Durchsatz. Darüber hinaus verursacht ihre Wartung und Regularisierung auch erhebliche wiederkehrende Kosten. Diese schweren Investitionsausgaben stellen Herausforderungen dar, vor allem für kleine und mittlere Prüfeinrichtungen in Entwicklungsländern. Die verbietenden Kosten entmutigen neue Teilnehmer und begrenzen den Ausbau bestehender Spieler auf dem Markt. Nur gut finanzierte Großlabore und die mit großen Pharmaunternehmen verbundenen Unternehmen können es sich leisten, stark in Premium-Analysewerkzeuge zu investieren. Selbst für sie beinhaltet die Entscheidung eine sorgfältige Bewertung der Rücksendungen. In dem aktuellen wirtschaftlichen Szenario, das von der Pandemie beeinflusst wird, priorisieren viele Labore wesentliche Tests und Verzögerungen oder Aufhebung teure Pläne, um Technologien für fortgeschrittene Anwendungen wie Bioburden-Analyse zu aktualisieren. So wurde nach einer Studie von 2020 der Weltgesundheitsorganisation (WHO) die Verfügbarkeit von Qualitätskontrollanlagen in Ländern mit niedrigem und mittlerem Einkommen, insbesondere in den afrikanischen und südostasiatischen Regionen, als unzureichend erwiesen. Die Studie ergab, dass nur 15-20% der nationalen Kontrolllabore in diesen Regionen grundlegende Infrastruktur und Fähigkeiten für mikrobiologische Analysen hatten.
- Gegenleistung: Anstatt Geräte zu kaufen, können Unternehmen in Leasing- oder Finanzierungsoptionen suchen. Dieser Ansatz kann die finanzielle Belastung im Laufe der Zeit ausbreiten und den Zugang zu den neuesten Technologien ermöglichen, ohne dass die vollen Kosten im Vordergrund stehen.
- Liebe Fachkräfte: Der Mangel an Fachkräften bei Bioburdentests hat die Industrie in den letzten Jahren erheblich beeinflusst. Aufgrund der Attrition und des Ruhestandes erfahrener Arbeiter, zusammen mit weniger Studenten, die sich für Biologie und Mikrobiologie entscheiden, gibt es jetzt einen Mangel an qualifizierten Technikern, Forschern und Analysten, die in Bioburden-Testmethoden und Standards gut versandt sind. Dieser Mangel hat zu Verzögerungen bei Probentests in der Pharma-, Medizin- und Lebensmittelindustrie geführt. Der biopharmazeutische Sektor setzt sich insbesondere stark auf schnelle und genaue Bioburdentests, um Produktsterilizität und Patientensicherheit zu gewährleisten. Allerdings haben Personalengpässe es schwierig gemacht, Laboratorien und Vertragshersteller zu testen, um die analytischen Bedürfnisse von Unternehmen, die in neue Arzneimittelentwicklung, generische Herstellung und medizinische Produkt Sterilisation. Dadurch werden Produktfreigaben manchmal um 4-6 Monate zurückgeschoben, je nach Verfügbarkeit von spezialisiertem Personal, das die erforderlichen Tests, Validierungen und Dokumentationen durchführen kann. Diese Verzögerung kann die klinischen Testzeiten und Markteinführung Zeitplan von Pharmaunternehmen geplant erheblich beeinflussen. So stellte ein 2022-Bericht der Weltgesundheitsorganisation (WHO) fest, dass fast 35 % der Medizintechnikunternehmen in Ländern mit niedrigem und mittlerem Einkommen hohe Kapitalkosten als eine große Hürde bei der Errichtung von Qualitätskontrolllaboren und beim Zugang zu fortschrittlichen Prüftechnologien anführten.
- Gegenleistung: Investieren Sie in Ausbildungsprogramme, um bestehende Mitarbeiter zu motivieren und sie mit den notwendigen Qualifikationen für Bioburdentests auszurüsten. Dazu gehören Sponsoringkurse, Workshops, Zertifizierungen und Kooperationen mit akademischen Institutionen, Partner mit Universitäten und Hochschulen, um eine Pipeline von qualifizierten Absolventen zu schaffen, die ausgebildet und bereit sind, in Bioburden-Tests zu arbeiten. Praktikumsprogramme können den Studierenden helfen, praktische Erfahrungen zu sammeln und arbeitsbereit zu sein.
Aktuelle Entwicklungen:
- Im August 2022, Lonza führte den Nebula Multimode Reader, den ersten Multimode-Reader, der für den Einsatz mit den turbidimetrischen, chromogenen und rekombinanten Endotoxin-Detektionsmethoden von Lonza zertifiziert wurde.
- Die Lonza Group ist ein schweizerisches multinationales Fertigungsunternehmen für die Pharma-, Biotechnologie- und Ernährungsbranche mit Sitz in Basel, mit großen Anlagen in Europa, Nordamerika und Südasien. Lonza wurde im späten 19. Jahrhundert in der Schweiz unter diesem Namen gegründet. Das Unternehmen bietet Produktentwicklungsdienstleistungen für die pharmazeutische und biologische Industrie, einschließlich der kundenspezifischen Herstellung von Biopharmazeutika und Nachweissystemen und Dienstleistungen für die Biowissenschaften.
- Im Juni 2022, Berkshire Sterile Fertigung (BSM), eine füllfertige CMO in Lee, MA, kündigte an, dass ihr Sterilitätstest-Isolator bereit ist, Sterilitätstests vor Ort für seine GMP-Ansätze durchzuführen. Der neue Service soll die Veröffentlichung für die meisten, wenn nicht alle, der Kunden des Unternehmens verkürzen.
- Berkshire Sterile Manufacturing (BSM) ist eine füllfertige CMO (Contract Manufacturing Organization) in Lee, MA. Das Unternehmen ist spezialisiert auf die sterile Füllung von injizierbaren Arzneimitteln, von denen die meisten in klinischen Studien sind oder einen kleinen kommerziellen Bedarf benötigen. BSM bietet Dienstleistungen wie Enddampfsterilisation von Spritzen, Spezialfüllung, Lyophilisierung von Fläschchen und Zweikammerflüssigkeit/Flüssig/Lyo, alles innerhalb eines Isolators. Das Unternehmen hat kürzlich die Bereitschaft seiner Sterilitätsprüfung Isolator angekündigt, vor Ort Sterilitätstests für seine GMP (Good Manufacturing Practice) Chargen durchzuführen. Dieser neue Service soll die Freigabezeit für seine Kunden verkürzen. BSM hat auch seine Anlagen- und Mikrobiologie-Testfähigkeiten erweitert, und es hat in eine vollautomatische, 100% isolatorbasierte sterile Füll-/Endlinie mit einem Gefriertrockner investiert.
Abbildung 2. Bioburden Testing Market Share (%), nach Produkt, 2024
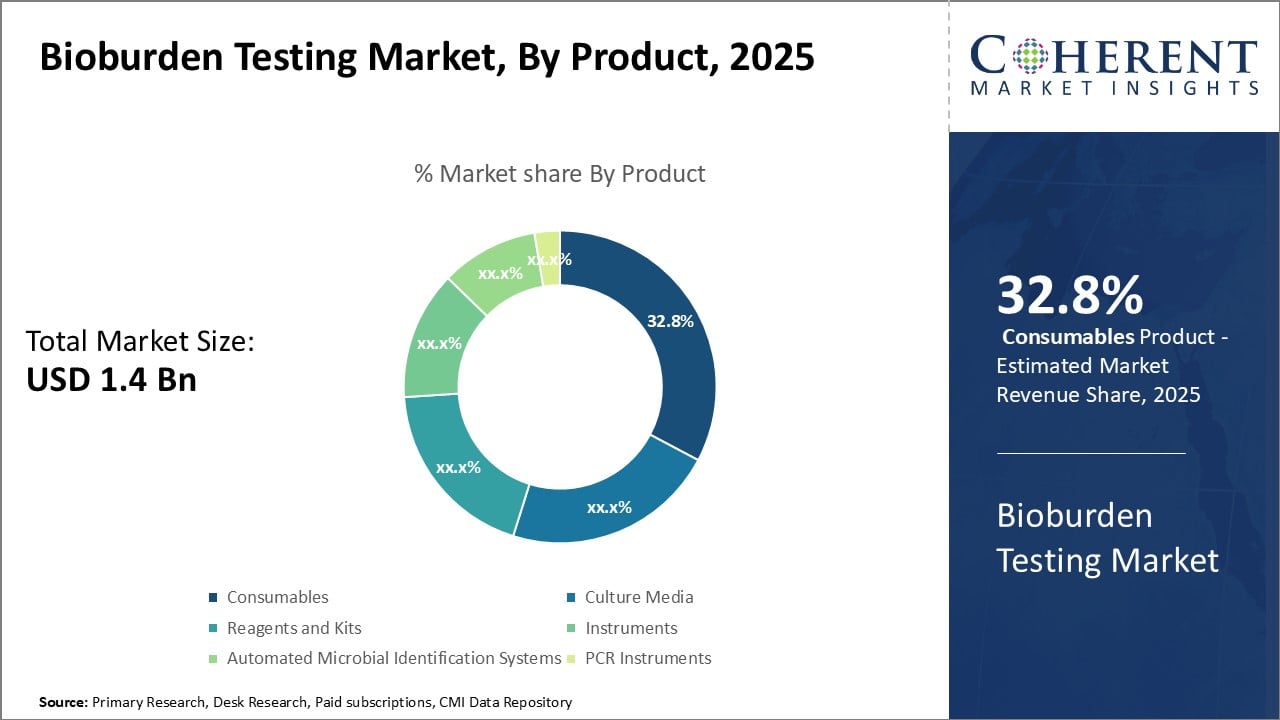
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Top Players:
- Charles River Laboratories International, Inc.
- SGS SA
- Merck KGaA,
- Becton Dickinson und Company
- Das ist die beste
- North American Science Associates Inc.
- Nelson Laboratories LLC
- Biomérieux SA
- Thermo Fisher Scientific
- und Pacific Biolabs.
Begriff: Bioburden-Test ist ein entscheidender Qualitätskontrollprozess, der die mikrobiellen Verunreinigungen in verschiedenen Produkten, einschließlich Wasser, Rohstoffen und Fertigprodukten, misst. Es wird für eine breite Palette von Produkten, wie Medizinprodukte, Pharmazeutika, Lebensmittel und Getränke, Wasser, Verpackung, Rohstoffe, menschliches Gewebe, tierisches Gewebe und Kosmetik durchgeführt. Ziel der Bioburden-Tests ist es, die Sicherheit, Qualität und die regulatorische Einhaltung jeder hergestellten Produktserie sicherzustellen. Es geht darum, das Vorhandensein von lebensfähigen Mikroorganismen vor der Sterilisation zu erfassen und zu quantifizieren, da diese aus Rohstoffen oder durch den Herstellungsprozess eingeführt werden können. Bei den Prüfverfahren handelt es sich um Direktplattierverfahren, wie z.B. die Gießplatten- und Spreizplattenverfahren, wobei das Gießplattenverfahren aufgrund seiner höheren theoretischen Genauigkeit bevorzugt wird.


