预计近期全球Humira生物市场将出现大幅增长,市场规模预计将从2004年开始扩大。 2023年为772.1百万美元至3,871.4美元 到2030年,妇女人数,具有复合年增长率 (CAGR)为25.9%. 这一增长是由若干因素造成的,包括自体免疫疾病发病率上升、对生物同类物的需求增加以及有利的报销政策。
Humira是一种用于治疗各种自体免疫疾病的生物药物,包括: 风湿性关节炎 具有全球最畅销生物药物的区别,每年销售额超过200亿美元。
生物类药物在安全性,疗效和质量方面是高度相似的生物类药物,在某些地区专利保护到期后进入了Humira市场. 这些生物类似物在市场上造成了竞争,并有可能节省费用。 通过提供更负担得起的治疗选择,它们有助于降低价格和改善病人获得关键药物的机会。 各种制药公司都获得了Humira生物相似物的监管批准,市场规模和增长率受到监管框架、市场准入、医生和病人接受等因素的影响。
全球Humira生物类似市场区域透视
北美: 北美市场,特别是美国,一直是胡米拉生物类似市场的重要角色. 但是,引入了 生物类似物 由于专利保护和复杂的监管程序,本区域面临挑战。 随着Humira专利的到期,生物类似物的市场预计将在北美增长. 北美占市场份额的很大比例,约占45.2%。
欧洲: 欧洲一直处于生物相似性采纳的前列,见证了数种Humira生物相似性在其市场上的认可和推出. 该区域制定了监管途径和政策,支持吸收生物相似物,从而增加市场竞争和潜在成本节约。 欧洲拥有大约30.7%的市场份额,突出了其在Humira生物类似市场的重要性。
亚太: 亚太地区,包括日本、韩国和澳大利亚等国家,出现了类似Humira生物的出现。 诸如自发性免疫疾病日益流行和需要更负担得起的治疗办法等因素,推动了该区域的市场。 然而,亚太区域各国对类似生物的管理审批和市场准入各不相同。 亚太约占市场份额的16.8%.
分析视图
在临床试验中证明了Humira生物类似物在治疗某些自体免疫疾病方面的效力。 它们表现出了与原Humira相似的功效和安全性。 而且,患者也并不表现出任何信任问题,这导致市场在预测期间扩张. 患者没有表现出任何信任问题,这导致市场在预测期间扩张,表明这些治疗在管理自体免疫疾病方面有希望的未来. 临床试验的积极成果表明,Humira生物类似原Humira的功效和安全性是相当的,这使保健专业人员和病人都产生了信心。 对这些治疗的有效性的这种信任为预测期间的市场扩张铺平了道路,表明用Humira生物类似物管理自体免疫疾病的前景充满希望。
图 1. 全球Humira生物类似份额(%),按区域分列,2023年
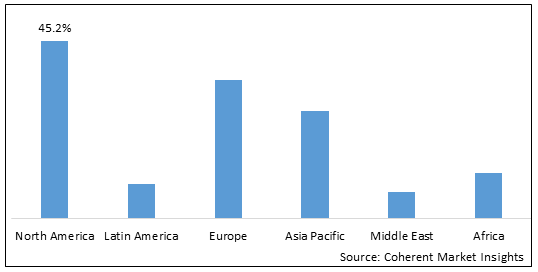
To learn more about this report, request sample copy
全球Humira生物市场驱动力:
- 专利失效: 保护Humira的专利到期为生物类似物的进入铺平了道路。 一旦专利到期,它允许其他制药公司开发和销售类似Humira的生物版本,在市场上形成竞争.
- 节省费用: 生物类似物为参考生物药物提供了更具成本效益的替代品。 随着对负担得起的保健需求的增加,生物类似物为降低病人、保健系统和付款人的治疗费用提供了机会。 这种节省成本的潜力是采用Humira生物类似物的重要动力。 例如,2023年10月26日,一家生物制药公司Celltrion USA公司宣布其经FDA批准的生物类似物YUFLYMA(adalimumab-aatty)被加入CarePartners Specialty Pharmay Cost Federation方案。 YUFLYMA是Humira(adalimumab)生物类同物的高浓度(100毫克/毫升)和无柠檬酸的配体。 CarePartners及其战略伙伴将提供并分发YUFLYMA,作为与1 000多万计划成员类似的最低净成本高浓度Humira(adalimumab)。
- 自我免疫疾病的发病率不断上升: 自动免疫疾病,如风湿性关节炎,s病,以及卡罗恩病在全球都在上升. 这些疾病日益普遍,促使人们需要有效和易于获得的治疗,包括Humira的生物类似疗法,这些疗法已被证明是治疗自体免疫疾病的办法。
- 有利的监管环境: 各区域的管理机构为生物同类物质的批准和市场准入制定了准则和途径。 这些框架明确了Humira生物相似物的开发、评价和商业化。 有利的监管环境鼓励制药公司投资开发生物类似物.
全球Humira生物市场机会:
- 增加获得治疗的机会: 胡米拉生物类似物的可得性为改进自体免疫疾病患者获得治疗的机会。 生物类药物为参照生物药物提供了更负担得起的替代品,使更多的人能够从有效的疗法中受益。
- 市场扩张和竞争力: 引入humira生物类似物在市场上形成竞争,从而推动创新和成本优化. 这一竞争鼓励制药公司开发和推出生物相似物,从而形成更具竞争力的景观. 它还促进市场增长和为病人制定各种治疗方案。
- 增强 治疗选择: 胡米拉生物类似物的提供扩大了医生和病人的治疗选择范围。 医生可以根据患者需求、定价和临床证据等因素,从多种类似生物选择中选择。 患者可受益于根据自己具体条件和偏好选择的更广泛疗法。
- 全球市场扩张: Humira生物市场为全球扩张提供了机会。 随着全世界生物类似物的管理途径和准则不断演变和改进,制药公司可在各区域寻求批准,从而开拓新市场,接触更多的病人。
| 报告范围 | 细节 |
|---|
| 基准年 : | 2023 (英语). | 2023年市场规模: | 772.1亿nn美元 |
|---|
| 历史数据: | 2018年至2022年 互联网档案馆的存檔,存档日期2018-09-02. | 预测周期 : | 2023 - 2030 (英语). |
|---|
| 2023至2030年CAGR预测期: | 25.9% | 2030 (英语). 数值预测 : | (单位:千美元) |
|---|
| 覆盖的地理: | - 北美: 美国和加拿大
- 拉丁美洲: 巴西、阿根廷、墨西哥和拉丁美洲其他地区
- 欧洲: 德国、英国、西班牙、法国、意大利、俄罗斯和欧洲其他地区
- 亚太: 中国、印度、日本、澳大利亚、韩国、东盟和亚太其他地区
- 中东和非洲:海湾合作委员会国家、以色列、南非、北非、中非和中东其他地区
|
| 所涵盖的部分: | - 按产品类型: Biosilar Humira (Adalimumab), 和可交换生物类似Humira
- 通过说明: 风湿性关节炎、风湿性关节炎、克罗恩病、溃疡性结肠炎、Ankylosing Spondylitis、青少年精神病性关节炎和其他自动免疫条件
- 按发行频道: 医院药房、零售药房和网上药房
- 按患者年龄: 成人病人、小儿病人和老年病人
|
| 涵盖的公司: | Amgen Inc., Samsung Bioepis Co., Ltd., Sandoz International GmbH(Novartis AG), Mylan N.V., Boehringer Ingelheim International GmbH, Pfize Inc., Fresenius Kabi AG, Coherus BioSciences, Inc., Biogen Inc., AbbVie Inc., Celltrion Inc., Rani Therapeutics Holdings, Inc., Teva 制药工业有限公司, Merck & Co., Inc., Viatris Inc.,和Alvotech. |
| 增长动力: | - 专利终止
- 节省费用
- 增加自动免疫疾病的发病率
- 有利的监管环境
|
| 限制和挑战: | - 复杂的监管程序
- 知识产权和专利诉讼
- 医生和病人的认识和接受
|
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
全球Humira生物类似市场 趋势:
- 管理审批和市场进入: 世界各地的监管机构为生物同物的核准和市场进入制定了途径和准则,包括Humira。 对Humira生物相似物的监管批准数量一直在增加,使得市场供应和采用得以扩大。
- 市场扩张和区域变化: Humira生物类似市场正在全球扩张,各区域都有生物类似物。 欧洲一直处于生物相似性采纳的前列,批准使用的Humira生物相似性数量相对较多. 然而,其他区域,包括北美、亚太和拉丁美洲,也正在目睹Humira类生物的进入和增长。
- 医生和病人接受: 随着医生在开具生物相似处方方面获得更多的经验和信心,生物相似处方的接受和收养正在增加。 患者对生物相似物的接受程度也在增长,其动力是临床结果呈阳性、成本节约和改善获得治疗选择的机会。
- 协作与伙伴关系: 制药公司、保健提供者和付款人之间正在形成合作伙伴关系,以推动Humira生物类的开发、市场准入和采用。 这类协作旨在改善患者的获得、教育和对生物类似物的认识,并消除其吸收方面的潜在障碍。
全球Humira生物市场限制:
- 复杂的监管程序: 生物类似物的监管审批程序可能很长而且复杂. 证明与参考产品相似以及确保安全和功效的要求,可能对生物同类制造商构成挑战。 这些监管障碍可能延缓市场进入,并阻碍Humira生物类似物的供应。
- 知识产权和专利诉讼: 知识产权和专利诉讼会给Humira生物相似物的进入制造障碍。 原生生物制造商可能为保护其专利而进行法律纠纷,导致生物同类市场进入的延误. 这些法律复杂性可能影响竞争环境,并减缓更负担得起的生物类似选择。
- 医生和病人的认识和接受: 医生和病人对生物类似物的认识和了解有限,可能妨碍其采用。 医生可能担心疗效、安全和可交换性,而病人可能不愿从参考生物药物中切换。 教育医生和病人了解Humira生物相似物的好处和相似性对于克服这些障碍至关重要。
平衡: 关键的市场参与者应当实施方案和举措,提高医生和同伴对生物相似的认识。 需要减少有关知识产权和专利诉讼的法律纠纷。
最近的事态发展
新产品
- 阿布拉达 (adalimumab-atto):ABRILADA是一种无柠檬酸的生物异构物,用于治疗某些患风湿性关节炎,青少年异病性关节炎,血清性关节炎,aykylosing spondylitis,成人克罗恩病,溃疡性结节炎和斑点性结节炎的患者. 2023年10月5日,美国FDA授予Abrilada(adalimumab-afzb)可互换性,这是第二个获得此称号的adalimumab生物类似物.
- 芬兰 (adalimumab-aqvh):YUSIMRY(adalimumab-aqvh)是一种类似humira(adalimumab)的生物物质,是一种肿瘤坏死因子(“TNF”),它表明可以减少风湿性关节炎、少年异病性关节炎、血栓性关节炎和烟管炎的征兆和症状,并治疗克罗恩病、溃疡性结膜炎、血栓性结膜炎和血栓炎。 2023年7月03日,商业级生物制药公司Coherus BioSciences Inc.宣布YUSIMRY(adalimumab-aqvh)可以在美国商业销售,单价为每卡995美元,售价为两台40 mg/0.8 mL自动注射器,代表对humira(adalimumab)的折扣超过85%,目前价格为每卡6,922美元两支笔.
- AMJEVITA(adalimumab-atto):AMJEVITA是一种与Humira(adalimumab)相似的生物,一种抗TNF-α单克隆抗体. AMJEVITA的活性成分是抗TNF-α单克隆抗体,其氨基酸序列与humira相同. 2023年1月31日,美国多国生物制药公司Amgen宣布了AMJEVITA(adalimumab-atto),该生物与humira(adalimumab)类似,现可在美国使用.
购置和伙伴关系
- 2023年7月24日,全球通用创新药领先者泰娃制药股份有限公司和专为全球患者研发和制造生物仿制药的全球生物技术公司阿尔沃科技公司宣布,他们同意扩大现有的战略伙伴关系协议. 泰瓦制药股份有限公司还将收购Alvotech发行的从属可兑换债券. 合作伙伴继续密切合作,处理有关AVT02在等待美国批准的事项,AVT02是Humira(adalimumab)可互换的高浓度生物同类候选物。 现有的战略伙伴关系协议还包括另外四个生物相似的候选者,其中一个是AVT04,这是针对Stelara(ustekinumab)的拟议生物相似物,它正等待美国食品药品管理局(FDA)的批准.
- 2023年6月5日,拉尼治疗 Holdings, Inc.)是一家临床阶段生物治疗公司,专注于口服生理学和药物,他宣布,公司扩大了与Celltrion, Inc.,一家生物制药公司的伙伴关系,达成了开发RT-105的协议,这是一家口服Adalimumab生物类似物. 拉尼疗法 Holdings, Inc.)于2023年1月宣布了与Celltrion的首个合伙企业,开发了RT-111,这是一个口服的ustekinumab生物仿制品. 根据新的许可证和供应协议的规定,Celltrion将专门向Rani治疗控股公司供应RT-105所需的Adalimumab生物类似药物(CT-P17)。 Rani Therapeutics Holdings, Inc.)授予独家使用CT-P17的许可证,用于RT-105的开发与商业化,Celltrion在第一阶段研究后被授予首次谈判的权利,以获得对RT-105的全球权利.
- 2023年6月1日,马克·古巴 成本加药品 一家公益公司和一家全球生物同类公司Coherus BioSciences公司于2023年7月宣布计划向Mark Cuban Cost Plus Drug公司客户YUSIMRY(adalimumab-aqvh)提供HUMIRA(adalimumab注射)的生物相似物。 古巴马克 成本加药品 公司计划从2023年7月开始向客户提供YUSIMRY,价格为569.27美元,外加发货和运输费。
图 2. 2023年按产品类型分列的全球Humira生物类似市场份额(%)
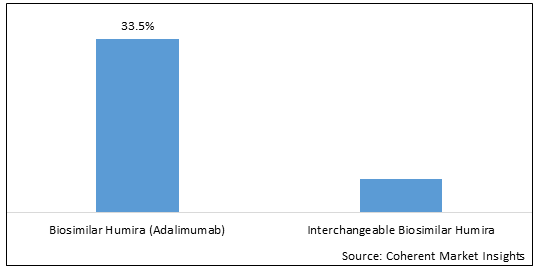
To learn more about this report, request sample copy
全球Humira类似生物市场上的顶级公司
- 安源股份有限公司.
- 三星Bioepis有限公司
- 桑多兹国际 股份有限公司(诺华集团)
- (原始内容存档于2018-09-21). Mylan N.V.
- 博埃林格·因格尔海姆国际有限公司
- 辉瑞股份有限公司.
- 弗雷塞尼乌斯·卡比集团
- 科赫鲁斯生物科学公司
- 生物基因股份有限公司.
- 阿比维公司.
- 手机公司
- 拉尼治疗控股公司
- 泰瓦制药公司 工业有限公司
- Merck & Co.股份有限公司(美联储)
- 维阿特里斯股份有限公司.
- 阿尔沃技术
定义: Humira生物相似物是Humira专利到期后开发并批准的生物药物humira(adalimumab)的高度相似的版本. 这些生物类似物的设计具有与humira相似的疗效,安全性和质量,并为诸如风湿性关节炎, p病和crohn病等自体免疫疾病的患者提供更负担得起的治疗方案.


