Aumentare la prevalenza di malattie e disturbi è previsto per aumentare la crescita dell'uomo globale immunoglobulina ph4 per il mercato di iniezione endovenosa nel periodo di previsione. Ad esempio, secondo i dati forniti dal National Health Service, il sistema sanitario pubblico in Inghilterra, l'immunoglobulina utilizzata per trattare la malattia di Kawasaki viene chiamata globulina gamma. Dopo l'amministrazione di IVIG, i sintomi di febbre, influenza o rash migliorano entro 36 ore.
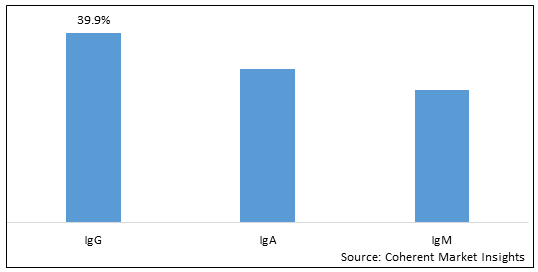
Figura 1. Immunoglobulina umana globale (pH4) per il mercato dell'iniezione endovenosaQuota (%), per indicazione delle malattie, 2023
To learn more about this report, request sample copy
Immunoglobulina umana globale (pH4) per il mercato dell'iniezione endovenosa – Drivers
Aumentare l'incidenza di focolai di malattia
L'incidenza crescente di focolai di malattia sta aumentando la domanda di misure diagnostiche avanzate, che si prevede di aumentare la crescita dell'immunoglobulina umana globale (pH4) per il mercato di iniezione endovenosa. Per esempio, la malattia coronavirus (COVID-19) pandemica è l'epidemia più recente che è stato segnalato per la prima volta il 1 gennaio 2020, a Wuhan, in Cina. L'Organizzazione Mondiale della Sanità ha dichiarato la malattia del coronavirus (COVID-19) come pandemia l'11 marzo 2020. Secondo l'Organizzazione Mondiale della Sanità (OMS), circa 1,991,562 casi della malattia coronavirus (COVID-19) sono stati segnalati il 16 aprile 2020, in tutto il mondo.
Aumentare l'approvazione dei prodotti immunoglobulina umana endovenosa
Le approvazioni dei prodotti immunoglobulina umana endovenosa da parte delle autorità di regolamentazione dovrebbero guidare la crescita dell'immunoglobulina umana (pH4) per il mercato di iniezione endovenosa durante il periodo di previsione. Ad esempio, il 4 maggio 2023, La Food and Drug Administration (FDA)- l'organismo principale di regolamentazione dei farmaci e dei dispositivi medici negli Stati Uniti, ha approvato Kamada Pharmaceuticals- un'azienda biofarmaceutica globale per la produzione di Cytogam (citomegalovirus immuno globulin iniezione endovenosa) presso la sua struttura situata in Israele per trattare COVID-19.
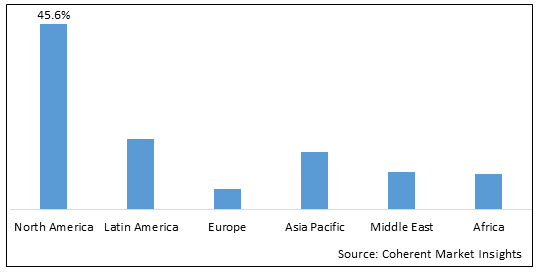
Figura 2. Immunoglobulina umana globale (pH4) per il mercato delle iniezioni endovenose (%), per regione, 2023
To learn more about this report, request sample copy
Immunoglobulina umana globale (pH4) per il mercato dell'iniezione endovenosa - Analisi regionale
Tra le regioni, il Nord America è stimato a tenere una posizione dominante nel ph4 dell'immunoglobulina umana globale per il mercato di iniezione endovenosa nel periodo di previsione. Ciò è dovuto alla prevalenza di COVID-19 nella regione. Ad esempio, secondo un rapporto pubblicato dall'OMS il dicembre 2020, nel 2020 erano stati confermati 10.336,829 casi di COVID-19 con 1,127,152 morti.
Immunoglobulina umana globale (pH4) per il mercato dell'iniezione endovenosa – impatto di Coronavirus (COVID-19) Pandemica
Dal COVID-19 focolaio virus nel dicembre 2019, la malattia si è diffusa in oltre 100 paesi in tutto il mondo, e l'Organizzazione Mondiale della Sanità lo ha dichiarato un'emergenza sanitaria pubblica il 30 gennaio 2020.
Il COVID-19 ha interessato l'economia in tre modi principali: influenzando direttamente la produzione e la domanda di farmaci, creando interruzioni nei canali di distribuzione, e attraverso il suo impatto finanziario sulle imprese e sui mercati finanziari. A causa di blocchi nazionali, diversi paesi come Cina, India, Arabia Saudita, Stati Uniti, Egitto, e altri stanno affrontando problemi con il trasporto di droghe da un posto all'altro.
Tuttavia, la pandemia COVID-19 ha avuto un impatto positivo sul ph4 dell'immunoglobulina umana globale per il mercato dell'iniezione endovenosa. Questo è a causa della crescente carenza di COVID-19 farmaci a livello globale che a sua volta, ha causato i ricercatori a sviluppare nuove terapie immunoglobina per contrastare la crescente domanda. Per esempio, secondo un articolo pubblicato nel marzo 2022 a PubMed- un motore di ricerca gratuito per banche dati biologici, l'Agenzia Italiana Medicinali - l'istituzione pubblica responsabile per l'attività regolamentare dei farmaci in Italia, ha passato un avvertimento sull'alta carenza di azitromicina nel paese a causa della prescrizione senza precedenti del farmaco durante la pandemica.
Immunoglobulina umana (pH4) per il mercato dell'iniezione endovenosa Copertura del rapporto
| Copertura del rapporto | Dettagli | ||
|---|---|---|---|
| Anno di base: | 2022 | Dimensione del mercato nel 2023: | US$ 61.6 Bn |
| Dati storici per: | 2018 a 2021 | Periodo di tempo: | 2023-2030 |
| Periodo di previsione 2023 a 2030 CAGR: | 12,8% | 2030 Proiezione del valore: | US$ 142.8 Bn |
| Geografie coperte: |
| ||
| Segmenti coperti: |
| ||
| Aziende coperte: | Takeda Pharmaceutical Company Limited, Baxter, CSL, Bayer AG, Grifols, S.A, Octapharma Brasil Ltda, Shanghai RAAS Blood Products Co Ltd, Hualan Biological Engineering, Inc, Top Bio Group Co, Ltd (A sussidiaria di China Biologic Products Holdings, Inc), China Resources Boya Bio-pharmaceutical Company Gruppo Co Ltd, ADMA Biologics, Inc, Sinopharm Group Co. Ltd. | ||
| Driver per la crescita: |
| ||
| Limitazioni & Sfide: |
| ||
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
Immunoglobulina umana globale Ph4 per la segmentazione del mercato dell'iniezione endovenosa:
Il ph4 dell'immunoglobulina umana globale per il rapporto del mercato dell'iniezione endovenosa è segmentato nel tipo di prodotto, nell'interfaccia, nell'utente finale e nella regione.
Per tipo di prodotto, il mercato è segmentato in IgG, IgA e IgM. Di cui, il segmento igG dovrebbe tenere una posizione dominante nel ph4 dell'immunoglobulina umana globale per il mercato di iniezione endovenosa durante il periodo di previsione e questo è attribuito alla loro maggiore affinità e capacità di neutralizzare tossine, virus e batteri.
Per indicazione delle malattie, il mercato è segmentato in COVID-19, Malattia di immunodeficienza primaria, Thrombocytopenia mediata da immuni, Malattia di Kawasaki, Leucemia linfocitica B cronica (B-CLL), e altri. Di cui, il segmento COVID-19 dovrebbe tenere una posizione dominante nel ph4 dell'immunoglobulina umana globale per il mercato di iniezione endovenosa durante il periodo di previsione e questo è attribuito ai casi in aumento di coronavirus in tutto il mondo.
Dal canale di distribuzione, il mercato è segmentato in farmacie ospedaliere, farmacie al dettaglio e farmacie online. Di cui, il segmento delle Farmacie Ospedaliera dovrebbe dominare il mercato nel periodo previsto e questo è attribuito al numero crescente di ricovero dei pazienti per trattare COVID-19 durante la pandemia.
Per Regione, il mercato è segmentato in Nord America, America Latina, Europa, Asia Pacifico, Medio Oriente e Africa. Di cui il segmento Nord America dovrebbe dominare il mercato a causa della più alta prevalenza di COVID-19 in questa regione.
Tra tutte le segmentazioni, il segmento di indicazione della malattia ha il più alto potenziale a causa dei crescenti casi di COVID-19 in tutto il mondo. Per esempio, secondo i dati pubblicati dall'Organizzazione Mondiale della Sanità, un'agenzia specializzata delle Nazioni Unite responsabile della salute pubblica internazionale, il 4 maggio 2023, quasi 2,8 milioni di nuovi casi di coronavirus e oltre 17.000 morti correlati al COVID sono stati segnalati tra il 3 e il 30 aprile 2023.
Immunoglobulina umana globale Ph4 per l'analisi sezionale del mercato di iniezione endovenosa:
Tra il tipo di prodotto, il segmento IgG dovrebbe dominare nella regione del Nord America durante il periodo di previsione a causa della dipendenza dei pazienti sulla terapia IgG per il trattamento di varie malattie. Per esempio, secondo i dati pubblicati nel dicembre 2022, in PubMed- un motore di ricerca gratuito per database biologici e rapporti medici, oltre il 40% degli adulti con miastenia gravis generalizzata (gMG) negli Stati Uniti che erano stati prescritti un trattamento di immunoglobulina endovenosa (IVIG), divennero utenti frequenti con una media di 6 dosi somministrate ogni anno.
Immunoglobulina umana globale Ph4 per il mercato dell'iniezione endovenosa: sviluppi chiave
Nel luglio 2022, Takeda Farmaceutica Società Limitata- una multinazionale giapponese azienda farmaceutica, ha annunciato risultati positivi dalla fase 3 trial clinico valutando HYQVIA (Immune Globulin Infusion 10% IVIG con Recombinant Human Hyaluronidase) per il trattamento di mantenimento di Chronic Inflammatory Demyelinating Polyradiculoneuropathy (CIDP).
Secondo un articolo pubblicato nell'ottobre del 2022, a PubMed- un database medico per medici e operatori sanitari, un processo di 16 settimane condotto in dermatomiocitis pazienti nel 2022 ha dimostrato che IVIG ha permesso un miglioramento migliore delle condizioni di malattia rispetto al placebo.
Nel maggio 2020, approvato il Food and Drug Administration (FDA) Octapharma Brasil Ltd a- un'azienda farmaceutica basata sulla Svizzera Investigational New Drug Application (IND) che consente all'azienda di avviare una fase 3 di prova di Octagam (globulina immunitaria endovenosa [umano]) in pazienti con grave progressione della malattia coronavirus.
Immunoglobulina umana globale Ph4 per il mercato di iniezione endovenosa: chiave Tendenze
Nell'aprile 2020, Kamada Pharmaceuticals- un'azienda biofarmaceutica globale, e Kedrion S.p.A- un'azienda che sviluppa e distribuisce medicinali derivati dal plasma, ha collaborato per sviluppare, produrre e distribuire un prodotto immunoglobulina policlonale derivato dal plasma umano (IgG) per il potenziale trattamento COVID-19. Con la collaborazione, Kedrion S.p.A raccoglierà e fornirà plasma presso i suoi centri KEDPLASMA da pazienti recuperati Covid-19. Kamada effettuerà lo sviluppo del prodotto, la produzione e lo sviluppo clinico, in collaborazione con Kedrion S.p.A.
Nel novembre 2020, la Food and Drug Administration (FDA) degli Stati Uniti ha rilasciato un'autorizzazione all'uso di emergenza (EUA) per la terapia anticorpo monoclonale investigativa bamlanivimab di Lilly- una società farmaceutica statunitense, per il trattamento di COVID-19 da lieve a moderato nei pazienti adulti e pediatrici. Bamlanivimab è un anticorpo monoclonale che è specificamente diretto contro la proteina di picco di SARS-CoV-2, progettato per bloccare l'attacco del virus e l'ingresso nelle cellule umane.
Immunoglobulina umana globale Ph4 per il mercato dell'iniezione endovenosa: restrizioni
L'inefficienza di immunoglobuline per trattare COVID- 19
L'inefficacia delle terapie immunoglobina può frenare la crescita dell'immunoglobulina umana globale ph4 per il mercato dell'iniezione endovenosa. Per esempio, uno studio condotto il 2022 gennaio, da The National Institute of Allergy and Infectious Diseases (NIAID, parte degli istituti nazionali di salute), ha concluso che l'aggiunta di anti-coronavirus hIVIG a un regime remdesivir non ha migliorato la salute di un sottoinsieme di adulti ospedalizzati con COVID-19.
Prova e prova in pazienti non ospedalizzati e più indagini sul regime di droga possono servire come un efficace controbilanciamento per determinare l'efficacia effettiva di immunoglobina.
Mancanza di approvazione da parte dell'OMS
La raccomandazione dell'Organizzazione Mondiale della Sanità contro l'uso di ph4 Immunoglobins per il trattamento del coronavirus può frenare la crescita di questo mercato. Per esempio, secondo i dati pubblicati dall'OMS nel dicembre del 2022, era sconosciuto se i prodotti IVIG derivati dal plasma donatore in pool contengono alti livelli di anticorpi neutralizzanti SARS-CoV-2 e gli effetti immunomodulatori dei preparati IVIG, non sembrano beneficiare i pazienti con COVID-19.
Questo può essere superato utilizzando migliori sostituti e alternative che sono già stati approvati come un trattamento efficace contro COVID-19.
Immunoglobulina umana globale Ph4 per il mercato di iniezione endovenosa - i giocatori chiave
I principali attori operanti nel mondo dell'immunoglobulina umana ph4 per il mercato dell'iniezione endovenosa includono Takeda Pharmaceutical Company Limited, Baxter, CSL, Bayer AG, Grifols, S.A, Octapharma Brasil Ltda, Shanghai RAAS Blood Products Co Ltd, Hualan Biological Engineering, Inc, Top Bio Group Co, Ltd (A sussidiaria di China Biologic Products Holdings, Inc), Sichuan Yuanda Boya Bio-pharmaceutical Gruppo Co Ltd, ADMA Biologics, Inc, Sinopharm Group Co. Ltd.
*Definizione: Immunoglobulina endovenosa (IVIG) contiene l'immunoglobulina G (IgG) in piscina immunoglobuline dal plasma di circa mille o più donatori di sangue. I IVIG sono sterili, purificati prodotti IgG prodotti fabbricati dal plasma umano immatricolato e contengono tipicamente più del 95% IgG non modificato, che ha funzioni effettive Fc-dipendenti intatte e solo tracce di immunoglobulina A (IgA) o immunoglobulina M (IgM).
Share
About Author
Vipul Patil
Vipul Patil is a dynamic management consultant with 6 years of dedicated experience in the pharmaceutical industry. Known for his analytical acumen and strategic insight, Vipul has successfully partnered with pharmaceutical companies to enhance operational efficiency, cross broader expansion, and navigate the complexities of distribution in markets with high revenue potential.
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients