In Nordamerika und Europa werden altersbedingte Makuladegenerationstherapien geschätzt, die auf US$ 12.5 Milliarden in 2023 und erwartet eine CAGR von 6.1% während des Prognosezeitraums (2023-2030).
Analysten’ Ansichten über Nordamerika und Europa altersbedingte Makuladegenerations-Therapiemarkt:
Die zunehmende Prävalenz der altersbedingten Makuladegeneration, die zunehmende geriatrische Bevölkerung, neue Produkteinführungen und Strategien wie Fusionen, Akquisitionen und Zusammenarbeit werden erwartet, dass das Wachstum des Marktes für makulare Degenerationstherapien in Nordamerika und Europa im Prognosezeitraum vorangetrieben wird. So leben nach den von den Centers for Disease Control and Prevention veröffentlichten Daten am 31. Oktober 2022 im Jahr 2019 geschätzte 19,8 Millionen (12,6%) Amerikaner im Alter von 40 Jahren mit altersbedingter Makuladegeneration (AMD). Davon lebten 1,49 Millionen (0,94%) mit einer Vision, die AMD bedrohte. Die AMD-Prävalenz stieg mit einem Alter von 2 % bei Personen im Alter von 40 bis 44 bis 46,6 % bei Personen im Alter von ≥ 85 Jahren. Die Rohprävalenz von AMD reichte von einem Tief von 6,2% im District of Columbia bis zu einem Höchstwert von 18,3% in Florida. Solche hohe Prävalenz erhöht den Bedarf an altersbedingten Makuladegenerationstherapeutika.
Abbildung 1. Nordamerika & Europa Altersbezogene Macular Degeneration Therapeutics Marktanteil (%), Nach Krankheitstyp, 2023
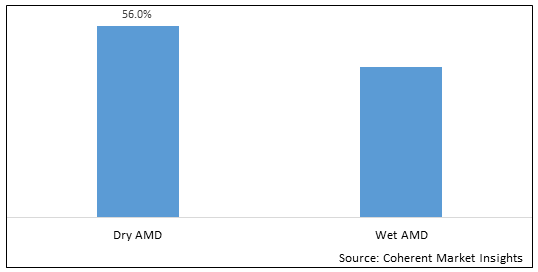
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Nordamerika und Europa Age-Related Macular Degeneration Therapeutics Market– Treiber
Abbildung 2. Nordamerika & Europa Altersbedingte Macular Degeneration Therapeutics Marktanteil (%), Nach Region, 2023
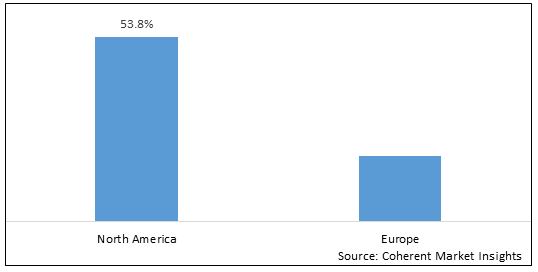
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Nordamerika & Europa Ältere Macular Degeneration Therapeutics Markt- Regionale Analyse
Unter der Region wird Nordamerika geschätzt, eine beherrschende Stellung im nordamerikanischen und europäischen altersbedingten Makuladegenerations-Therapiemarkt über den Prognosezeitraum zu halten, aufgrund der steigenden Produkte. Zum Beispiel, am 7. April 2021, LumiThera, Inc., ein US-basiertes kommerzielles Bühnenmediziner-Unternehmen, das Photobiomodulation (PBM) Behandlung für okulare Störungen und Krankheiten lieferte, gab positive Ergebnisse in seiner LIGHTSITE II, multizentrische klinische Studie bei trockenen Patienten mit altersbedingter Macular Degeneration (AMD) bekannt. Die prospektive, doppel maskierte, randomisierte, multizentrische klinische Studie mit dem Titel LIGHTSITE II wurde in acht führenden Retinazentren mit Sitz in den USA, Deutschland, Spanien, Italien und Frankreich durchgeführt. Ziel war es, alle vier Monate mit einer Dauer von 10 Monaten trockene AMD-Themen im Laufe von drei PBM-Sitzungen zu behandeln. Die Ergebnisse zeigten eine stetige Verbesserung der BCVA-Messungen aus der Basislinie mit den verkürzten PBM-Behandlungsintervallen. Bisher, LIGHTSITE Die Ergebnisse der Studie haben gezeigt, dass alle sechs Monate wieder visuelle Vorteile zwischen PBM-Behandlungen erreicht werden. Die Vorteile von viermonatigen Behandlungsintervallen waren bei der Aufrechterhaltung der Vision Ergebnisse konsequenter.
Nordamerika und Europa Age-Related Macular Degeneration Therapeutics Market– Auswirkungen von Coronavirus (COVID-19) Pandemie
Seit dem Ausbruch des COVID-19 Virus im Dezember 2019 hat sich die Krankheit auf über 100 Länder weltweit ausgebreitet, und die Weltgesundheitsorganisation erklärte es am 30. Januar 2020 zum Notfall der öffentlichen Gesundheit.
COVID-19 beeinflusste die Wirtschaft in drei Hauptrichtungen: indem sie die Produktion und die Nachfrage von Drogen direkt beeinflusste, indem sie Störungen in Vertriebskanälen und ihre finanziellen Auswirkungen auf die Unternehmen und Finanzmärkte verursachte. Aufgrund der bundesweiten Lockdowns konfrontierten mehrere Länder wie China, Indien, Saudi-Arabien, die U.A.E., Ägypten und andere Probleme beim Transport von Drogen von einem Ort zum anderen.
Die COVID-19 Pandemie hatte jedoch negative Auswirkungen auf den Markt für therapeutische Makuladegenerationen in Nordamerika und Europa, da die Patientenbesuche in Krankenhäusern reduziert wurden. Nach einem Artikel, der am 14. April 2022 in der Zeitschrift "Journal Current Opinion in Pharmacology" veröffentlicht wurde, wirkte sich die COVID 19 negativ auf retinale degenerative Erkrankungen aus. Die Komplikationen in der Augenbehandlung wurden erhöht und dies war auf reduzierte Patientenbesuche zurückzuführen. Verzögerte Behandlung durch Angst, Lebensstil oder als nachteilige Wirkung von COVID-19 ist mit visueller Acuity verbunden.
Nordamerika & Europa Ältere Macular Degeneration Therapeutics Marktsegmentierung:
Nordamerika & Europa altersbedingte Makuladegeneration Therapien Marktbericht wird in Krankheitstyp, Drogentyp, Verteilungskanal und Region segmentiert.
Das Segment Krankheitstyp hat unter allen Segmenten das höchste Potenzial, da die Krankheitsprävalenz mit zunehmender geriatischer Bevölkerung zunimmt. So ist die altersbedingte Makuladegeneration (AMD) nach den am 24. August 2022 von Fighting Blindness Canada veröffentlichten Daten die Hauptursache für Sehverluste bei Menschen über 55 Jahren, die etwa 2,5 Millionen Kanadier betreffen. Jedes Jahr in Kanada gibt es fast 200.000 neu diagnostizierte Fälle von AMD.
Nordamerika und Europa Age-Related Macular Degeneration Therapeutics Market Querschnittsanalyse:
Unter Krankheitstypsegment ist das trockene AMD-Segment während der Prognosezeit in der Region Europa aufgrund der zunehmenden Einführung neuer Behandlungen dominant. So haben am 24. Februar 2023 die STADA Arzneimittel AG, ein in Deutschland ansässiges Pharmaunternehmen und Xbrane Biopharma, ein in Schweden ansässiges biopharmazeutisches Unternehmen mit hohem Bedarf Biosimilars und langjährigen injizierenden Injektionen, bekannt gegeben, dass die Arzneimittel und Gesundheitsprodukte der U.K. Regulatory Agency (MHRA) für Ximluci eine Zulassung erteilt hat, eine Biosimilar Referenzencing Augenarzt, Lucentis (ranibizumab). Ranibizumab ist ein monoklonales Antikörperfragment, das aus demselben Elternmaus-Antikörper wie bevacizumab erstellt wurde. Es hemmt Angiogenese (die Bildung neuer Blutgefäße) durch Hemmung vaskulärer Endothelwachstumsfaktor A (VEGF-A). Ranibizumab kann verwendet werden, um Makuladegeneration durch Hemmung von VEGF zu behandeln.
North America & Europe Age-Related Macular Degeneration Therapeutics Market Report Coverage:
| Bericht Deckung | Details | ||
|---|---|---|---|
| Basisjahr: | 2022 | Marktgröße 2023: | US$ 12.5 Bn |
| Historische Daten für: | 2018 bis 2021 | Vorausschätzungszeitraum: | 2023 bis 2030 |
| Vorausschätzungszeitraum 2023 bis 2030 CAGR: | 6.1% | 2030 Wertprojektion: | US$ 18.9 Bn |
| Geographien: |
| ||
| Segmente: |
| ||
| Unternehmen: | Novartis AG, Bayer AG, Bausch Health Companies Inc., Regeneron Pharmaceuticals, Inc., F. Hoffmann-La Roche AG, Pfizer, Inc., Valeant Pharmaceuticals International, Inc., Abb. Vie Inc., Viatris Inc. und Amgen Inc. | ||
| Wachstumstreiber: |
| ||
| Zurückhaltungen & Herausforderungen: |
| ||
Entdecken Sie Makros und Mikros, die anhand von über 75 Parametern geprüft wurden, Sofortigen Zugriff auf den Bericht erhalten
Nordamerika und Europa Age-Related Macular Degeneration Therapeutics Markt: Schlüsselentwicklungen
Am 22. Oktober 2021, F. Hoffmann-La Roche AG, ein in der Schweiz ansässiges multinationales Healthcare-Unternehmen, gab bekannt, dass die US Food and Drug Administration (FDA) Susvimo (ranibizumab Injektion) 100 mg/mL für den intravitrealen Einsatz über Okularimplantat für die Behandlung von Menschen mit neovaskulärer oder „wet“ altersbedingter Makuladegeneration (nAMD) zugelassen hat, die zuvor auf mindestens zwei anti-vaskuläre Endothelialwachstumsfaktor (V. Neovaskulär AMD ist eine potenziell blindende Bedingung, die Behandlung mit Augeninjektionen erfordert, wie oft einmal im Monat. Susvimo, früher Port Delivery System mit ranibizumab genannt, ist die erste und einzige US FDA-genehmigte Behandlung für nAMD, die so wenig wie zwei Behandlungen pro Jahr bietet.
Am 31. März 2022, Novartis AG, ein in der Schweiz ansässiges globales Gesundheitsunternehmen gab bekannt, dass die Europäische Kommission (EG) Beovu (brolucizumab) 6 mg für die Behandlung von Sehbehinderung aufgrund von diabetischen Makulaödem (DME) genehmigt hat. Die Genehmigung in DME stellt die zweite Angabe für Beovu dar, die von der EG erteilt wurde, die zum ersten Mal zur Behandlung der feuchten altersbedingten Makuladegeneration zugelassen wurde. Der EG-Beschluss gilt für alle 27 Mitgliedstaaten der Europäischen Union (EU) sowie Island, Norwegen und Liechtenstein. Die EG-Zulassung basiert auf einem Jahr ein Daten aus der Phase III, randomisierte, doppel maskierte KESTREL- und KITE*-Studien, die ihren primären Endpunkt der Nicht-Unfruchtbarkeit der Veränderung der am besten korrigierten visuellen Akuität (BCVA) aus der Basislinie gegen aflibercept im ersten Jahr erfüllten. In beiden Versuchen, nach der Ladephase, blieben über die Hälfte der Patienten (55,1% in KESTREL und 50,3% in KITE) im Beovu 6 mg Arm auf einem 12-wöchigen Dosierintervall über das Jahr eins. Aflibercept Dosierung wurde auf das zugelassene EU-Label im Jahr einer Behandlung ausgerichtet
Am 13. Mai 2020 kündigte die Boehringer Ingelheim International GmbH, ein in Deutschland ansässiges Pharmaunternehmen, und CDR-Life Inc., ein in der Schweiz ansässiges Biotechnologieunternehmen, an, dass sie eine Kooperations- und Lizenzvereinbarung zur Forschung und Entwicklung von Antikörperfragment-basierten Therapien für die geografische Atrophie (GA) eingegangen sind. GA ist eine progressive, irreversible Retina-Krankheit, die bei Patienten mit altersbedingter Makuladegeneration (AMD) auftritt, für die es keine aktuelle Behandlung gibt. Zusammen mit Boehringer Ingelheims Expertise in der therapeutischen Entwicklung von Biologik und CDR-Lifes starkem Know-how im Antikörper-Engineering werden die beiden Unternehmen den präklinischen Kandidat von CDR-Life vorantreiben, um Patienten mit GA in Sicht zu halten.
Am 27. Januar 2022 kündigte Biogen, ein US-amerikanisches globales Biotechnologie-Unternehmen, an, dass sie eine Vereinbarung abgeschlossen haben, in der Samsung Biologics, südkoreanisches Biotechnologieunternehmen Biogens Beteiligung an dem Joint Venture von Samsung Bioepis für eine Gesamtüberlegung von bis zu 2,3 Milliarden US$ erwerben wird. Nach dem Erwerb des Anteils von Biogen werden die Unternehmen mit ihren exklusiven Vereinbarungen fortfahren, einschließlich der Vermarktung ihres aktuellen Portfolios. Dazu gehören vermarktete Produkte BENEPALI (etanercept), ein biosimilar referencing ENBREL, IMRALDITM (adalimumab), ein biosimilar referencing Humira und FLIXABI (infliximab), ein biosimilar referencing Remicade. Darüber hinaus wird Biogen auch kommerzielle Rechte für BYOOVIZTM (ranibizumab-nuna), eine zugelassene Biosimilar Referenzierung LUCENTIS (ranibizumab), sowie einen Untersuchungsbiosimilar-Kandidat in der Entwicklung, SB15 (aflibercept), eine vorgeschlagene Biosimilar Referenzencing EYLEA.
Nordamerika und Europa Ältere Macular Degeneration Therapeutics Markt: Schlüssel Entwicklung
Forschungskooperation zwischen wichtigen Marktteilnehmern
Die Forschungskooperation zwischen den wichtigsten Marktteilnehmern, um die Entwicklung neuer Therapeutika zu fördern, kann das Wachstum des Marktes vorantreiben. Am 29. Juni 2021 hat Ocular Therapeutix, Inc., ein US-amerikanisches biopharmazeutisches Unternehmen, die sich auf die Formulierung, Entwicklung und Vermarktung innovativer Therapien für Krankheiten und Erkrankungen des Auges konzentrierte, sowie Mosaic Biosciences, ein US-basiertes Biotechnologieunternehmen, in eine Entdeckungskollaboration aufgenommen, um neue Ziele und therapeutische Mittel zur Behandlung von trockenen altersbedingter Macular Degeneration zu identifizieren. Im Rahmen der Vereinbarung konzentriert sich die Zusammenarbeit zwischen Ocular Therapeutix und Mosaic auf die Entdeckung und Entwicklung neuartiger Komplementinhibitoren mit längerer Aktivitätsdauer. Ocular Therapeutix hat im Rahmen der Vereinbarung vereinbart, die im Rahmen der Zusammenarbeit durchgeführte Forschung zu finanzieren und behält alle Programmerfindungen und das damit verbundene geistige Eigentum vor.
Zulassungen für neuere Therapien
Zulassungen für neuere Therapien können das Wachstum des Marktes für therapeutische Makuladegenerationen in Nordamerika und Europa vorantreiben. Am 22. September 2020 kündigte Gyroscope Therapeutics Limited, ein US-amerikanisches klinisch-stufiges retinales Gentherapieunternehmen, an, dass die US Food and Drug Administration (FDA) GT005 für die Behandlung von geografischer Atrophie (GA) sekundär bis zur trockenen altersbedingten Makuladegeneration (AMD) Fast Track-Bezeichnung erteilt hat. GT005 ist eine Untersuchungsgentherapie, die unter der Netzhaut ausgeliefert wird und den Verlauf von GA verlangsamen soll, der zu Blindheit führen kann. Fast Track-Bezeichnung wurde GT005 für die Behandlung von Menschen mit GA, die spezifische Mutationen in ihrem Komplement Factor I (CFI) Gen und niedrige Niveaus des CFI-Proteins in ihrem Blut.
North America & Europe Age-Related Macular Degeneration Therapeutics Market: Restraints
Hohe Behandlungskosten
Die hohen Kosten für die Behandlung werden erwartet, um das Wachstum des Marktes für Makuladegenerationen in Nordamerika und Europa zu behindern. So sind nach einem Artikel, der am 3. November 2022 von den Biomolekülen veröffentlicht wurde, Anti-VEGF-Agenten eine günstige Prognose für nAMD zur Verfügung gestellt, aufgrund ihrer hohen Kosten sowie der Notwendigkeit häufiger Wiederholungsbehandlungen und Besuche mit einer erheblichen finanziellen Belastung für Patienten und das Gesundheitssystem verbunden. Ranibizumab Portal-Liefersystem (RPDS) verwendet in altersbedingter Makuladegeneration mit fester 6-monatiger Nachfüllung über eine einjährige Dauer kostet US$ 21.016. Die monatlichen intravitrealen Injektionen von ranibizumab kosten US$ 1943, aflibercept kostet US$ 5702, und bevacizumab kostet US$ 16,732. Solche hohen Kosten für Medikamente können das Marktwachstum zurückhalten.
Um dieser Zurückhaltung entgegenzuwirken, sollte eine Erstattungspolitik eingeführt werden, um die Gesamtkosten der Behandlung zu senken.
Nebenwirkungen der nassen AMD-Behandlung
Nebenwirkungen der nassen AMD-Behandlung werden erwartet, um das Wachstum des Marktes für Makuladegenerationen in Nordamerika und Europa zu behindern. So gibt es nach einem Artikel, der am 25. Oktober 2021 im Journal of Ophthalmic and Vision Research veröffentlicht wurde, verschiedene Naß-AMD-Medikamente, die eine Vielzahl von Nebenwirkungen haben. Wirkungen wie retinale Vaskulitis, intraokulare Entzündung, gleichzeitige vaskuläre Okklusion, Übelkeit, Erbrechen und dauerhafte Sehverlust bei Individuen werden erwartet. Wenige berichteten Nebenwirkungen wie Lentikularopazitäten, Pünktatkeratitis, Hornhautabrieb, posterior Kapselopacification, Katarakt, erhöhter intraokularer Druck, Blepharitis, Konjunktivitis und Iritis. Dies hemmt die Markterweiterung.
Um diese Zurückhaltung zu kompensieren, sollte mehr Forschung durchgeführt werden, um Nebenwirkungen im Zusammenhang mit der Behandlung zu reduzieren.
Nordamerika & Europa Ältere Macular Degeneration Therapeutics Markt- Schlüsselspieler
Zu den wichtigsten Akteuren, die auf dem Markt für Makuladegenerationstherapie in Nordamerika und Europa tätig sind, gehören die Novartis AG, die Bayer AG, die Bausch Health Companies Inc., Regeneron Pharmaceuticals, Inc., F. Hoffmann-La Roche AG, Pfizer, Inc., Valeant Pharmaceuticals International, Inc., AbbVie Inc., Viatris Inc. und Amgen Inc.
*Definition: Alterbedingte Makuladegeneration (AMD), auch als Makuladegeneration bezeichnet, ist eine Bedingung, die zu einem Verlust der zentralen Vision durch die Verdünnung der Makula der Netzhaut führt. Altersbedingte Makuladegeneration tritt typischerweise in der geriatrischen Bevölkerung auf und kann dauerhafte Sehverluste bei Menschen im Alter von 60 Jahren und darüber verursachen. Die altersbedingte Makuladegeneration besteht aus zwei Arten; die trockene altersbedingte Makuladegeneration (Dry AMD) und die nasse altersbedingte Makuladegeneration (wet AMD). Trockene altersbedingte Makuladegeneration ist eine häufige Form der Makuladegeneration, wo die Makula mit dem Alter dünner wird und zu einem Verlust der zentralen Vision führt. Es gibt keine Behandlung für trockene altersbedingte Makuladegeneration. Nasse altersbedingte Makuladegeneration ist weniger häufig, wo das Wachstum von anormalen Blutgefäßen unter der Netzhaut beobachtet wird. Nasse altersbedingte Makuladegeneration kann durch anti-vaskuläre Endothelial Wachstumsfaktor (Anti-VEGF) Injektionen verwaltet werden.
Teilen
Über den Autor
Ghanshyam Shrivastava
Ghanshyam Shrivastava – Mit über 20 Jahren Erfahrung in der Unternehmensberatung und Forschung fungiert Ghanshyam Shrivastava als leitender Berater und bringt umfassendes Fachwissen in den Bereichen Biologika und Biosimilars mit. Seine Hauptkompetenzen liegen in Bereichen wie Markteintritts- und Expansionsstrategie, Wettbewerbsanalyse und strategische Transformation über ein diversifiziertes Portfolio verschiedener Medikamente für unterschiedliche therapeutische Kategorien und APIs. Er ist hervorragend darin, die wichtigsten Herausforderungen der Kunden zu identifizieren und robuste Lösungen bereitzustellen, um ihre strategischen Entscheidungskompetenzen zu verbessern. Sein umfassendes Verständnis des Marktes gewährleistet wertvolle Beiträge zu Forschungsberichten und Geschäftsentscheidungen.
Ghanshyam ist ein gefragter Redner bei Branchenkonferenzen und trägt zu verschiedenen Veröffentlichungen über die Pharmaindustrie bei.
Vermissen Sie den Komfort, Berichte in Ihrer Landessprache lesen zu können? Finden Sie Ihre bevorzugte Sprache:
Verwandeln Sie Ihre Strategie mit exklusiven Trendberichten :
Häufig gestellte Fragen
Wir schließen uns Tausenden von Unternehmen auf der ganzen Welt an, die sich der Aufgabe verschrieben haben,ng the Excellent Business Solutions..
Alle unsere Kunden anzeigen