Die globale Medizinprodukteprüfung und Zertifizierung MarktwertUS$ 9,687.7 Mnin 2022 und wird prognostiziert, einen Wert zu erreichenUS$ 13,550,8 Mnvon2030beiCAGR von 4,3% zwischen2023 und 2030. Das medizinische Gerät testen und Zertifizierung Der Markt erlebt durch den Anstieg der Fokussierung auf die Medizinprodukteprüfung und Zertifizierung und strenge Regierungsvorschriften ein starkes Wachstum. Darüber hinaus wird mit dem Ausbruch von COVID-19 und der zunehmenden Nutzung von AI und IoT in medizinischen Geräten das Wachstum des Marktes vorantreiben. Allerdings dürften Faktoren wie die Vielfalt der Vorschriften und der Ausbruch von COVID-19 das Wachstum des Marktes behindern.
Global Medical Device Testing und Marktzertifizierung: Regionale Einblicke
Basierend auf Geographie, dem weltweiten Medizinprodukttest und der Zertifizierung Markt ist in Nordamerika, Europa, Asien-Pazifik, Lateinamerika und Mittlerer Osten & Afrika segmentiert.
Unter den Regionen wird erwartet, dass Nordamerika aufgrund der strengen Regierungsvorschriften, des Ausbruchs von COVID-19 und der steigenden Nachfrage nach Verifizierung und Validierung medizinischer Geräte den höchsten Marktanteil im Markt gewinnt. So ist die Food and Drug Administration (FDA) für die Regulierung medizinischer Geräte in den Vereinigten Staaten verantwortlich. Die FDA regelt medizinische Geräte, um ihre Sicherheit und Wirksamkeit zu gewährleisten und entwickelt und führt das nationale Programm durch, um unnötige Expositionen zu kontrollieren und einen sicheren und effizienten Einsatz von ionisierenden und nichtionisierenden strahlungsemittierenden elektronischen Produkten zu gewährleisten.
Europa und Asien-Pazifik werden auch mit einem starken Wachstum der globalen Medizinproduktetests und Zertifizierungen rechnen Markt aufgrund des Ausbruchs von COVID-19, Steigerung der Fokus auf die Qualität der medizinischen Geräte und strenge Regierungsvorschriften in diesen Regionen. So sind beispielsweise die zuständigen Behörden, die notifizierten Stellen und die autorisierten Vertreter am CE-Kennzeichnungsprozess beteiligt. Medizinprodukte werden auf der Ebene der EU-Mitgliedstaaten geregelt, aber die Europäische Arzneimittelagentur (EMA) ist an dem Regulierungsprozess beteiligt. Hersteller können das CE-Zeichen auf einem medizinischen Gerät platzieren, nachdem es eine Konformitätsbewertung bestanden hat.
Abbildung 1. Global Medical Device Testing and Certification Market Share (%), Nach Region, 2023
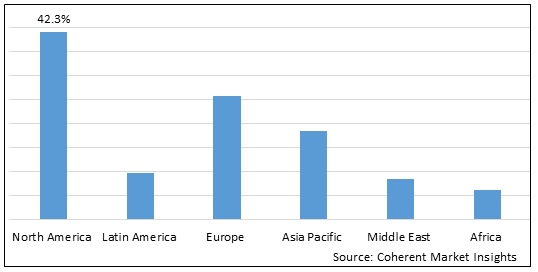
To learn more about this report, request sample copy
Global Medical Device Testing and Market Certification Drivers:
Aufstieg im Fokus Medizinische Geräteprüfung Wachstum des Wachstums auf dem Markt
Einer der wichtigsten Faktoren erwartet, das Wachstum des globalen Medizinproduktetests und Zertifizierung zu erhöhen Markt während der Prognosezeit ist der Anstieg der Fokus auf die Medizinproduktprüfung und Zertifizierung. Zum Beispiel plante TÜV SÜD im Januar 2022, seine Einrichtungen für medizinische und Gesundheitswesen (MHS) in New Brighton, Minnesota zu erweitern. Ein neues Labor bietet eine End-to-End-Testlösung für alle medizinischen Geräte und bietet eine Reihe von biologischen und chemischen Tests von medizinischen Geräten, die TÜV die aktuellen aktiven medizinischen Gerätetestfähigkeiten ergänzen.
Strenge Regierungsvorschriften Marktwachstum untermauern
Ein weiterer Faktor, der das Wachstum der globalen Medizinproduktetests und Zertifizierung vorantreibt Markt ist die strenge Regierungsverordnung auf der ganzen Welt. So variieren die Standardrichtlinien von Medizinprodukten von Land zu Land, und es ist zwingend notwendig, dass die Hersteller diese Richtlinien für die Vermarktung oder den Verkauf ihrer Medizinprodukte im Land verfolgen. Die USA folgen beispielsweise den Leitlinien für die Lebensmittel- und Drogenbehörde (FDA), Europa betrachtet die Zustimmung von Conformitè Europëenne (CE), Kanada braucht die Registrierung von Health Canada, und Indien braucht die Zulassung von der zentralen Drogen-Standardkontrollorganisation (CDSCO).
Global Medical Device Testing und Marktzertifizierung Möglichkeiten:
Der Ausbruch von COVID-19 wird erwartet, dass Spielern in der globalen Medizintechnikprüfung und Zertifizierung erhebliche Wachstumschancen bieten Markt. Zum Beispiel hat der Ausbruch von COVID-19 die Nachfrage nach Medizinproduktentests und Zertifizierungsdienstleistungen weltweit erhöht. Im Jahr 2020 hat die US Food and Drug Administration (FDA) Notfall-Nutzungs-Berechtigungen (EUA) für medizinische Geräte zur Diagnose von COVID-19 sowie Personal Protective Equipment (PPE) herausgegeben, die zum Schutz sowohl von Gesundheitsanbietern als auch von Patienten benötigt werden. Die medizinische Prüfung und Zertifizierung geht weiter und hat während der COVID 19 Situation eine schnelle Phase eingenommen.
Steigerung der Nutzung Künstliche Intelligenz (KI) und Internet der Dinge (IoT) in medizinischen Geräten wird erwartet, dass Spielern in der globalen Medizinprodukteprüfung und Zertifizierung erhebliche Wachstumschancen bieten Markt. So haben beispielsweise die Bereitstellung fortschrittlicher Technologien wie KI und IoT zusammen mit dem Fokus auf die Echtzeit-Patientenüberwachung ein komplexes Ökosystem für medizinische Geräte geschaffen. Um eine Marketing-Autorisierung zu erhalten, müssen diese Geräte methodisch getestet werden und strenge Vorschriften erfüllen. Daher investieren Marktteilnehmer oder Hersteller stark, um ihre Geräte zu testen und eine Marketing-Autorisierung zu erhalten.
Medical Device Testing und Zertifizierung Marktbericht Abdeckung
| Bericht Deckung | Details | ||
|---|---|---|---|
| Basisjahr: | 2022 | Marktgröße 2023: | US$ 10,073.4 M |
| Historische Daten für: | 2017 bis 2021 | Vorausschätzungszeitraum: | 2023 bis 2030 |
| Vorausschätzungszeitraum 2023 bis 2030 CAGR: | 4.3% | 2030 Wertprojektion: | US$ 13,550,8 Mn |
| Geographien: |
| ||
| Segmente: |
| ||
| Unternehmen: | Medistri SA, BSI Group, Ente Certificazione Macchine, GMED, IMQ Group SRL, TOXIKON, TÜV SÜD, WuXi AppTec, Pace Analytical Services LLC, Gateway Analytical LLC, Boston Analytical, Bureau Veritas, UL LLC, TUV Rheinland, SGS SA, Intertek Group PLC, Eurofins Scientific, Element Materials Technology, Dekra Testing GmbH. | ||
| Wachstumstreiber: |
| ||
| Zurückhaltungen & Herausforderungen: |
| ||
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
Global Medical Device Testing und Zertifizierung Markttrends:
Notwendigkeit Prüfung/Zertifizierung von medizinischen Geräten ist ein neuer Trend
Medizinprodukte werden weltweit von verschiedenen Regulierungsbehörden reguliert. Dies liegt vor allem daran, dass Endnutzer dieser Geräte eine hervorragende Leistung, Sicherheit und Wirksamkeit von diesen Geräten erwarten. Daher ist es für die Hersteller unerlässlich, eine medizinische Geräteteststrategie ordnungsgemäß umzusetzen, die das Gerät effektiv macht und den Produktionsprozess erleichtert. Dieser Trend wird voraussichtlich im Prognosezeitraum weitergehen und das Marktwachstum vorantreiben.
Outsourcing von Prüfung und Zertifizierung ein weiterer Trend
Die Nachfrage nach Outsourcing-Tests an Drittanbieter steigt mit einem schnellen Tempo aufgrund der kapitalintensiven Art der Inhouse-Tests. So sind mehrere Hersteller weltweit oder Spieler zunehmend Outsourcing-Test-Services, da strenge Vorschriften es kostspielig machen, in-house-Tests durchzuführen, und damit diese Unternehmen helfen, die Gesamtkosten der Tests zu reduzieren. Dieser Trend wird auch im Prognosezeitraum fortgesetzt und das Marktwachstum vorangetrieben.
Global Medical Device Testing und Marktzertifizierung Rückhaltemittel:
Diversity in Regulations, um das Wachstum des Marktes zu behindern
Einer der wichtigsten Faktoren erwartet, das Wachstum des globalen Medizinproduktetests und Zertifizierung zu behindern Markt ist die Vielfalt der Vorschriften oder strenge Regeln und Vorschriften. Die Standardrichtlinien des medizinischen Geräts variieren von Land zu Land, was für die Hersteller vorgeschrieben ist, ihre Produkte im Land zu vermarkten oder zu verkaufen. Die Verordnungen sind in jedem Land unterschiedlich. Daher ist es für Medizinproduktehersteller sehr wichtig, die Regulierungsrichtlinien dieses Landes zu registrieren und/oder zu erhalten.
Der Ausbruch von COVID-19, um das Marktwachstum zu behindern
Ein weiterer Faktor, der das Wachstum des globalen Medizinproduktetests und Zertifizierung behindert Markt ist der Ausbruch von COVID-19. Die Pandemie hat die Nachfrage nach medizinischen Gerätetests und Zertifizierungsdienstleistungen erhöht. Obwohl es Ausnahmen und Hebelwirkungen in den Vorschriften gibt, setzt die medizinische Prüfung/Zertifizierung fort und hat während der Pandemie eine schnelle Phase eingenommen. Die Pandemie hatte jedoch einen leichten Einfluss auf den Markt, da die Prüfung anderer medizinischer Geräte, die nicht ein Ausbruch sind, in Betrieb genommen wurde.
Abbildung 2. Global Medical Device Testing and Certification Market Share (%), Nach Servicetyp, 2023
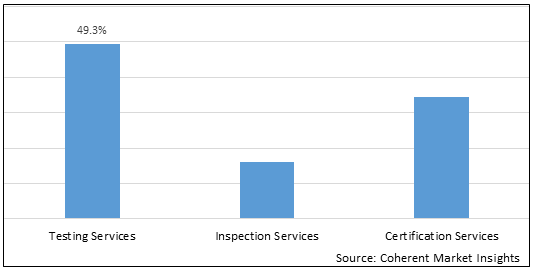
To learn more about this report, request sample copy
Global Medical Device Testing und Zertifizierung Markt Segmentierung:
Die globale Medizinprodukteprüfung und Zertifizierung Marktbericht wird in Service-Typ, Sourcing-Typ, Geräteklasse, Technologie und Geographie segmentiert.
Basierend auf Service Typ, der Markt wird in Testing Services, Inspection Services und Certification Services segmentiert. davon, Testdienste Segment wird erwartet, dass die medizinische Geräteprüfung und Zertifizierung dominieren Markt über den Prognosezeitraum und dies ist auf die steigende Nachfrage nach sicheren und effektiven medizinischen Geräten zurückzuführen.
Inspektionsdienste Segment wird auch erwartet, dass in naher Zukunft ein beträchtliches Wachstum zu verzeichnen ist und dies aufgrund der strengen Regeln und Vorschriften ist. Inspektionsdienste helfen, Kosten zu reduzieren, Risiken zu minimieren und die erwartete Qualität zu bieten.
Basierend auf Sourcing Type, der Markt wird in In-house und Outsourced segmentiert. Davon abgesehen, Ausgelagert Segment wird erwartet, dass der Markt während des Prognosezeitraums dominiert wird und dies auf den wachsenden Trend der Outsourcing medizinischer Geräte Testdienste zurückzuführen ist.
Basierend auf Geräteklasse, der Markt wird in Klasse I, Klasse II und Klasse III segmentiert. Davon abgesehen, Klasse I Segment wird erwartet, dass der Markt über den Prognosezeitraum dominiert wird und dies auf die steigende Nachfrage nach medizinischen Geräten der Klasse I zurückzuführen ist. Aufgrund der Risiken, die mit der Verwendung von medizinischem Gerät verbunden sind, werden diese Geräte als Klasse I, Klasse II oder Klasse III eingestuft. Die Klassifizierung hängt von dem Risiko ab, das dem Gerät zugeordnet ist.
Klasse II Segment wird auch erwartet, dass in naher Zukunft ein beträchtliches Wachstum zu verzeichnen ist und dies aufgrund der steigenden Nachfrage nach medizinischen Geräten der Klasse II.
Basierend auf Technologie, der Markt wird in Active Implant Medical Device, Active Medical Device, Non-Active Medical Device, In-Vitro Diagnostic Medical Device, Ophthalmic Medical Device, Orthopedic und Dental Medical Device, Vascular Medical Device, und andere Technologien segmentiert. Davon abgesehen, Active Implant Medical Device Segment wird erwartet, dass der Markt über den Prognosezeitraum dominiert wird und dies auf den Anstieg der Nachfrage nach aktive Implantat medizinische Geräte (AIMDs). Als eine der höchsten Risikokategorien des Gerätes unterliegen AIMDs strengen Regulierungskontrollen, bevor sie auf globale Märkte gelangen können.
In-Vitro Diagnostic Medical Device Segment wird auch erwartet, dass in naher Zukunft ein beträchtliches Wachstum zu verzeichnen ist, und dies ist auf eine zunehmende Fokussierung auf die Frühdiagnose zurückzuführen (aufgrund einer weltweiten Belastung der lebensbedrohlichen Krankheit). In vitro diagnostische medizinische Geräte sind Tests an biologischen Proben zur Bestimmung des Gesundheitszustands einer Person.
Global Medical Device Testing und Marktzertifizierung: Schlüssel Entwicklung
Im Februar 2021, Alfa Medizin (AMG) plante, in den nächsten fünf Jahren 263,5 Millionen Euro in den Markt zu investieren, um den Gesundheitsmarkt Ägyptens zu erweitern, einschließlich der Erhöhung der Zahl der Laboratorien, Produktionsanlagen und Standards.
Im Februar 2021 zertifizierte BSI die Neuromodulations-Klinik-Programmierer-Anwendung von Abbott und ihre Patientensteuerungs-App für die Verwendung auf kompatiblen persönlichen Apple-Smartphone-Geräten an die Medical Devices Regulation (MDR) (EU 2017/745) über den notified Body in den Niederlanden (2797).
Im April 2021 gab TÜV SÜD bekannt, dass es sich bei Medtec LIVE präsentiert hatte, um seine Fähigkeit, ein One-Stop-Shop für medizinische Gerätetests zu sein.
Im Oktober 2020, TÜV Rheinland kündigte die Eröffnung seiner Biomaterial- und Elektromagnetkompatibilität (EMC) Testlaboratorien in der Andhra Pradesh MedTech Zone (AMTZ), Visakhapatnam (Andhra Pradesh), Indien an.
Global Medical Device Testing und Marktzertifizierung: Schlüsselunternehmen Einblicke
Die globale Medizinprodukteprüfung und Zertifizierung Markt ist sehr wettbewerbsfähig. Dies ist auf die Notwendigkeit für medizinische Gerätetests und Zertifizierung weltweit zurückzuführen, so dass sich die Spieler auf dem Markt auf die Einführung neuer Produkte auf dem Markt konzentrieren.
Einige der Schlüsselakteure im globalen Medizinprodukttest und Zertifizierung Markt sind Medistri SA, BSI Group, Ente Certificazione Macchine, GMED, IMQ Group SRL, TOXIKON, TÜV SÜD, WuXi AppTec, Pace Analytical Services LLC, Gateway Analytical LLC, Boston Analytical, Bureau Veritas, UL LLC, TUV Rheinland, SGS SA, Intertek Group PLC, Eurofins Scientific, Element Materials and Technology, Dekra GmbH.
*Definition: Medizinische Geräteprüfung & Zertifizierung ist notwendig, um Sicherheit und Wirksamkeit von medizinischen Geräten zu gewährleisten. Die USA folgen den Leitlinien der Food & Drug Administration (FDA), Kanada braucht die Health Canada Registration, Europa betrachtet Conformitè Europëenne (CE) Zulassung, und Indien braucht Genehmigung von der Central Drugs Standard Control Organisation (CDSCO).
Share
About Author
Manisha Vibhute
Manisha Vibhute is a consultant with over 5 years of experience in market research and consulting. With a strong understanding of market dynamics, Manisha assists clients in developing effective market access strategies. She helps medical device companies navigate pricing, reimbursement, and regulatory pathways to ensure successful product launches.
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients