의약품 감시 시장 규모 및 예측 - 2025~2032
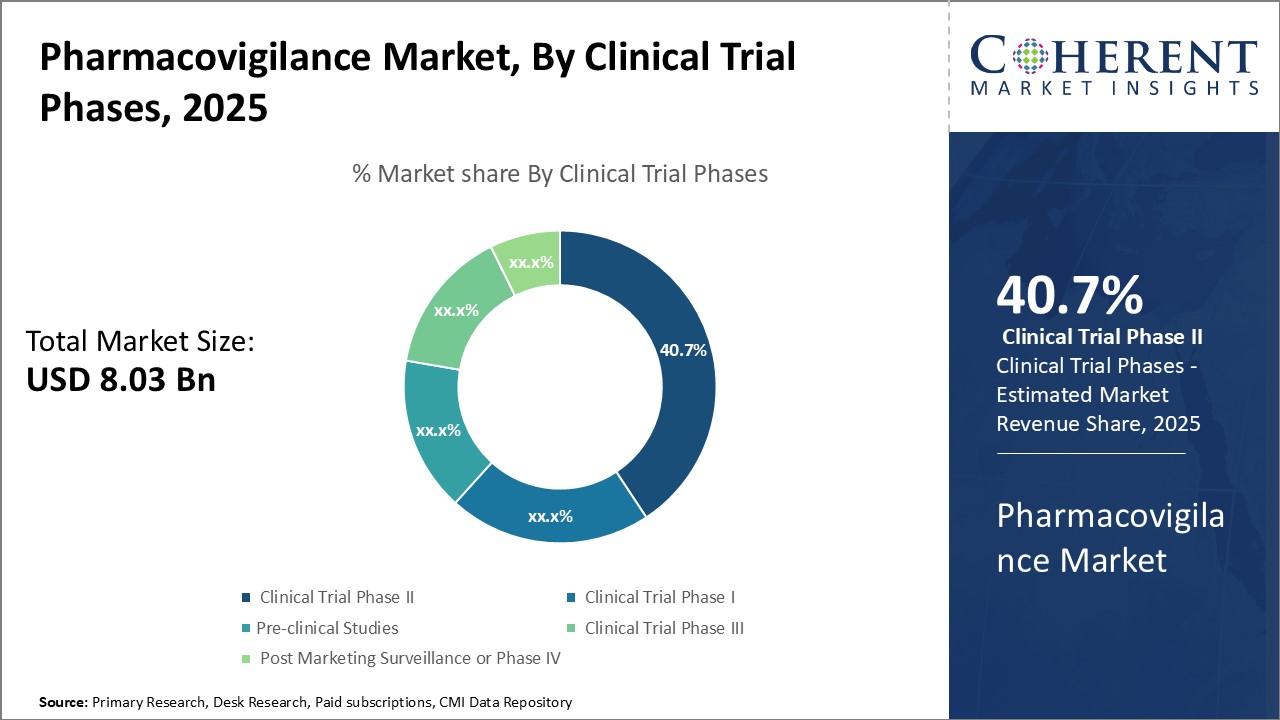
전 세계 약물 감시 시장은 2025년에 80억 3000만 달러 규모로 평가되고 2032년에는 140억 3000만 달러에 도달하여 연평균 성장률(CAGR)을 보일 것으로 예상됩니다. (CAGR) 2025년부터 2032년까지 8.3%
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
주요 사항
- 임상 시험 단계에 따라 3상 부문은 2025년에 전 세계 약물 감시 시장의 40.7% 점유율을 차지할 것입니다. 이는 엄격한 규제 준수 때문입니다.
- 방법 유형별로는 자발적 보고 부문이 가장 큰 시장 점유율을 차지하고 있습니다. 이 부문은 폭넓은 수용으로 인해 2025년 시장 점유율의 35.71% 를 차지할 것으로 예상됩니다.
- 서비스 제공업체 유형별로 보면 아웃소싱에 비해 실질적인 비용 관리 이점으로 인해 사내 부문이 2025년에 60.7% 로 약물 감시 시장에서 가장 큰 점유율을 차지했습니다.
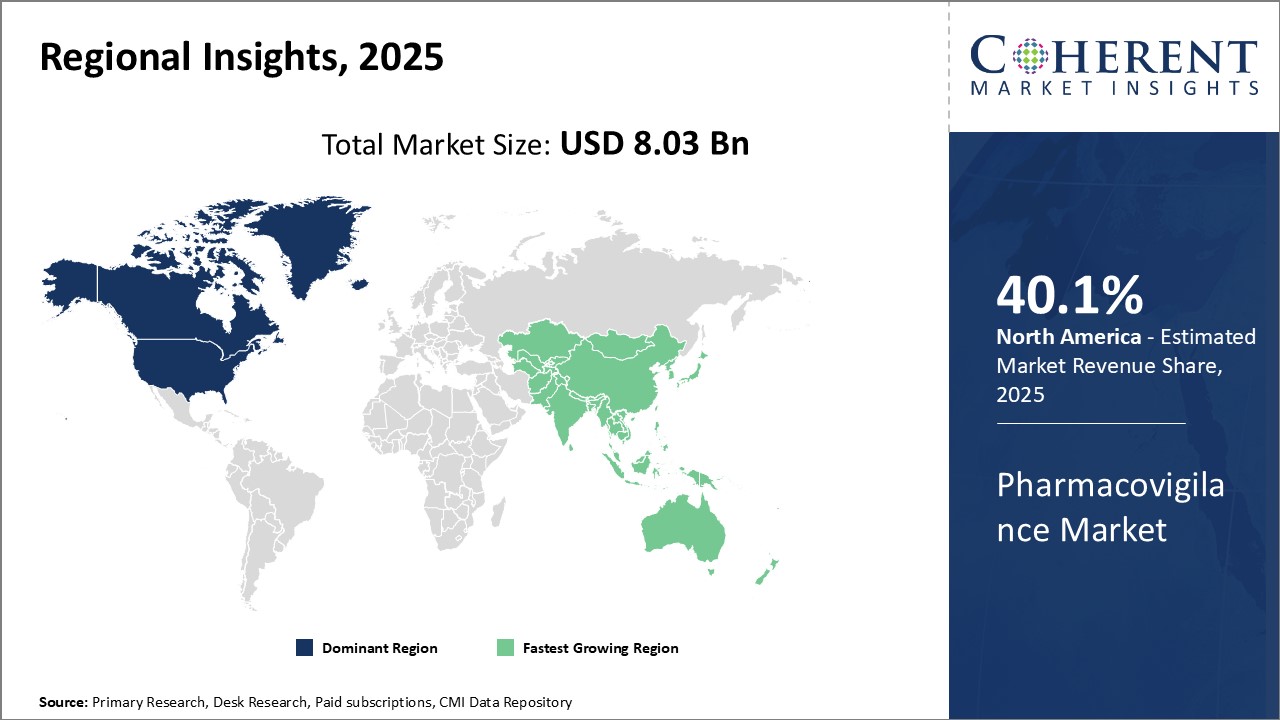
- 북미는 엄격한 규제 요건과 주요 제약회사 및 계약 연구 기관(CRO)의 존재로 인해 2025년 시장 점유율의 40.1% 를 차지할 것으로 예상됩니다.
시장 개요
약물 감시 시장 수요는 주로 약물 안전 모니터링에 대한 요구 사항 증가, 특히 전 세계 약물 소비 증가 및 규제 감독의 여파로 인해 증가하고 있습니다. 약물 개발 및 승인 절차가 점점 더 복잡해짐에 따라 효율적인 약물 감시 관행의 필요성이 그 어느 때보다 시급해지고 있습니다.
이상사례 보고, 위험 관리, 신호 감지를 포괄하는 약물 감시 서비스는 의료 환경의 필수적인 부분이 되고 있습니다.
현재 이벤트와 시장의 영향
현재 행사 | 묘사와 그것의 충격 |
증가된 규제 Scrutiny |
|
AI 및 자동화의 통합 |
|
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
가격 분석
- 케이스 가격 당: 이 모형은 납품업자에 의해, 취급되는 각 불리한 사건의 비용 이용됩니다. 가격은 케이스와 관련된 복잡성을 기반으로합니다.
- 편평한 요금/리테이너 모형: 몇몇 서비스 공급자는 지속적인 지원을 요구하는 회사를 위해 유리할 것이다 서비스의 세트 범위를 위한 매달 그리고 년 수수료 제안할 것입니다.
- Pay-As-You-Go 모델: 이 모델은 소규모 조직 및 프로젝트에서 유용합니다. 고객이 필요로하는 서비스와 비용을 지불하는 반면, 작업 부하를 변동하는 프로젝트.
- 계층화 된 가격 모델: 그것은 다른 가격에 서비스의 다른 수준은 사용자 정의, 분석 및 보고의 수준에 따라 달라집니다.
표본 가격 예상:
- 소형화 회사:
- 케이스 처리 : $ 200 - $ 1,000 케이스 당.
- 신호 탐지 및 위험 평가: $5,000 - 프로젝트 당 $50,000.
- 풀 서비스 pharmacovigilance outsourcing: 연간 $50,000 - $ 300,000, 서비스의 범위에 따라.
- 큰 약제 회사:
- 풀 스케일 pharmacovigilance 시스템 구현 : 매년 $ 1 백만 +.
- 케이스 처리 및 보고: $150 - $800 케이스 당.
- 기술 플랫폼 라이센스 (예 : PV 데이터베이스) : $ 100,000 - $ 500,000 + 매년.
Pharmacovigilance Market의 AI 통합
- 신호 탐지
AI 시스템은 약물이 해를 유발할 수있는 초기 징후 인 "신호"를 감지 할 수 있습니다. 기존 신호 감지는 통계 분석에 크게 의존하지만 AI, 특히 기계 학습 (ML) 및 자연 언어 처리 (NLP)은 구조화 및 구조화 된 데이터의 광대 한 양을 분석 할 수 있습니다 (예 : 임상 시험 보고서, 전자 건강 기록, 소셜 미디어 및 환자 포럼).
- 자동화된 케이스 처리
Pharmacovigilance는 ADR 보고서의 광대한 금액을 수집, 검토 및 처리하는 것을 포함합니다. AI는 다양한 채널을 통해 데이터를 수집하여이 프로세스의 여러 측면을 자동화 할 수 있습니다 (예 : 소셜 미디어, 의료 전문가, 환자 보고서) 분류 및 분류 광고 이벤트.
- Predictive 분석
역사 pharmacovigilance 자료를 분석함으로써, AI 모델은 약물이 안전 위험을 감당할 수 있음을 예측할 수 있습니다. 잠재적으로 안전 문제를 식별하기 전에. Predictive 모델은 demographics, comorbidities 및 이전 부작용과 같은 다양한 요소를 고려할 수 있으며 잠재적 인 위험을 예측하기 위해이 데이터를 사용합니다.
시장 역학
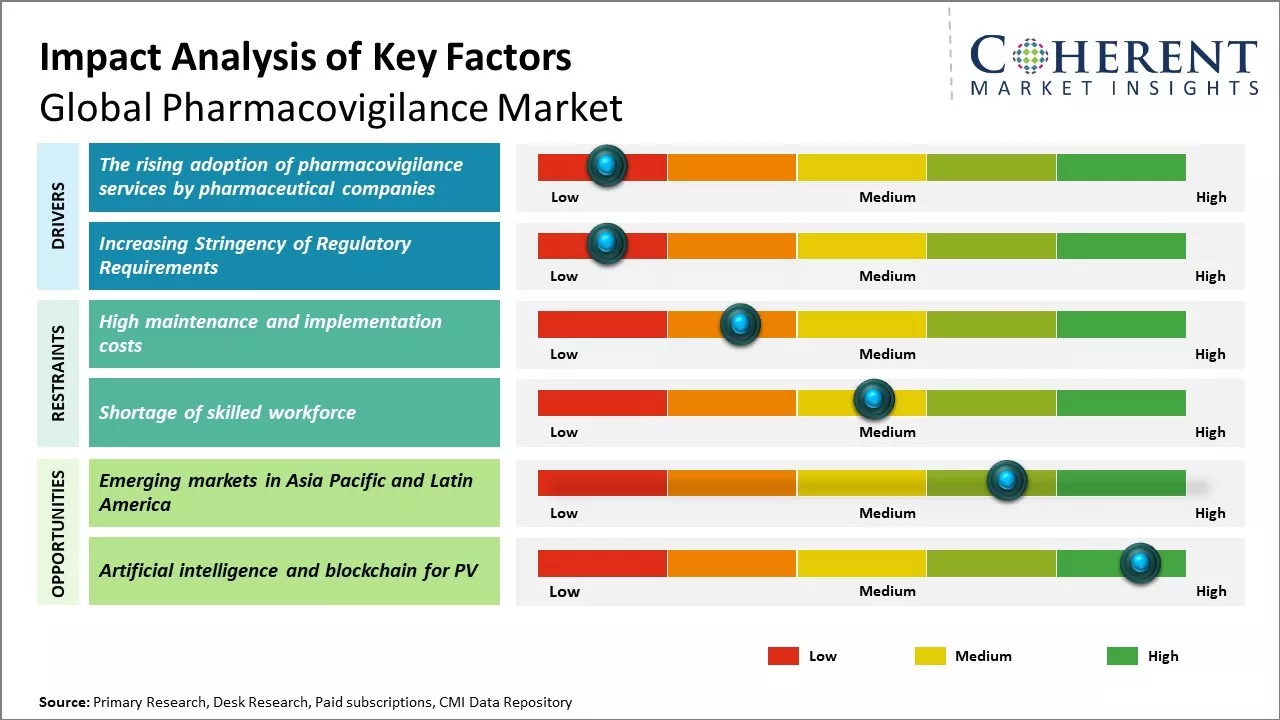
Pharmacovigilance 시장 운전사
- Pharmacovigilance의 증가 의약품 제조업체의 서비스
제약 조직에 의해 Pharmacovigilance 서비스 채택은 약 안전을 보장하기위한 엄격한 규정 때문에 크게 증가합니다. FDA 및 EMA와 같은 규제 당국은 엄격한 규범을 모니터링하고 마케팅 후 약물 안전을 보장합니다. pharmacovigilance 활동을 아웃소싱하는 제약 기관은 경험과 인프라를 갖춘 전문 임상 연구기구 (CROs)에 공급합니다.
Pharmacovigilance 아웃소싱은 약 회사가 CRO 파트너의 전문가에게 약물 안전을 모니터링하는 동안 전방에서 약물 발견 및 개발의 핵심 기능을 유지하도록 도와줍니다. 제약 회사들은 최첨단 기술, 훈련된 사람들 및 결합된 글로벌 전략에 대한 액세스를 통해 이점을 얻습니다.
2024년에 ProPharma Group은 유럽 기반 임상시험 및 약리학 회사인 Clinres Farmacija를 인수했습니다. 이 구매는 ProPharma의 pharmacovigilance 서비스 기능을 강화하고 포스트 시장 규제 강점에 추가합니다.
- 규제 요건의 묶음
다양한 국가의 규제 요구 사항의 증가는 글로벌 제약 시장의 중요한 성장을 주도 할 것으로 예상됩니다. 새로운 약물은 전례없는 속도로 시장에 진입하고 약물 안전 프로파일의 복잡성을 증가, 규제 당국은 더 엄격한 법률 및 안전 표준을 옹호했다.
제약 회사는 이제 포스트 마케팅에도 지속적인 모니터링과 함께 개발 초기 단계에서 약물의 종합적인 안전 프로파일링을 수행 할 수 있습니다. 규제 규범 준수는 지속적인 약물 승인 및 시장 액세스를 위해 절대적으로 중요합니다. 의료 산업은 또한 몇몇 높 단면도 약 안전 문제 및 실패의 aftermath에서 강렬한 scrutiny를 겪었습니다.
Market Opportunity – 아시아 태평양 및 라틴 아메리카의 Emerging 시장
아시아 태평양과 라틴 아메리카의 신흥 시장은 세계 약국 시장의 거대한 성장 기회를 제공합니다. 이 지역은 빈곤에서 수십억 명의 사람들이 들어온 급속한 경제 발전을 경험하고 증가한 지출 전력으로 중간 수준의 소비자 기반을 확장했습니다. 처분할 수 있는 소득 상승으로, 의료 시스템은 또한 더 중대한 투자를 가진 현대화를 겪고 있습니다.
이 환자 인구는 다양한 만성 및 생활성 질환에 대한 고급 약물에 액세스 할 수 있습니다. 동시에 제약 산업의 성장은 거대한 인구의 수요에 대처하기 위해이 지역에서 폭발했다. 많은 대형 다국적 약물 제조업체는 최근 몇 년 동안 아시아 태평양 및 라틴 아메리카 내의 제조 및 R & D 시설을 설치하여 비용을 절감하고 고객 기반에 더 가깝습니다.
글로벌 약국 시장 임상 시험 단계별 통찰력
- Stringent Regulatory requirements 임상 시험 단계 III에 있는 성장을 모십시오
임상 시험 단계 III 세그먼트는 2025에서 가장 높은 점유율에 기여할 것으로 예상됩니다. 엄격한 규제 요건을 준수합니다. 단계 III 재판은 수천 명의 인간 참가자를 참여하고 약물의 전반적인 위험 부담 관계를 확인하고 라벨링을위한 적절한 기초를 제공합니다.
미국 FDA 및 EMA와 같은 규제 당국은 시장 승인 전에 약물 안전을 보장하기 위해 단계 III 재판에 대한 광범위한 규정을 시행했습니다. Sponsors는 포괄적인 위험 관리 계획을 개발해야 합니다. 이것은 강력한 pharmacovigilance 시스템을 유지하고, 평가하고, 참여자로부터 약물 안전 문제를 방지합니다.
글로벌 약국 Market Insights, 방식의
- 이동 전자 보고 드라이브 Spontaneous Segment 정보
방법의 유형에 의하여, Spontaneous 보고 세그먼트는 가장 큰 시장 점유율을 붙듭니다. 이것은 넓은 합격 때문에. 전통적으로, Spontaneous 보고는 의학 전문가 및 소비자에 의해 서류상 근거한 모양에 의하여 제출된 voluntarily를 사용하여 불리한 사건 보고를 모으.
그러나 규제 기관은 현재 pharmacovigilance 관행을 현대화하기 위해 전자보고 기준을 밀어. E2B 및 ICH E2B(R3)와 같은 위임은 개별 케이스 안전 보고서 (ICSR)의 전자 전송에 대한 구조화 된 형식 요구 사항 및 기술 사양을 지정합니다. 이 표준을 준수하면 중앙 집중식 상호 운용성 데이터베이스 및 고급 데이터 분석 기능을 글로벌 수준에서 제공합니다.
Global Pharmacovigilance 시장 통찰력, 서비스 제공자의 유형
- In-House Segment 명령 비용 제어 혜택에서 가장 높은 공유
사내 세그먼트는 2025에 있는 pharmacovigilance 시장의 가장 큰 점유율을 아웃소싱에 무겁게 한 비용 통제 이점에 owing 있습니다. 사내팀은 제3자를 포함한 스폰서의 자체 자원 및 시설로 약물 안전 운영을 관리합니다. pharmacovigilance 기능은 내부적으로 전략적인 사업 우선 순위를 지키기 위하여 프로세스의 직접적인 감독을 제안합니다.
지역 통찰력
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
북미 약국 시장 분석 및 동향
북미는 전 세계 pharmacovigilance 시장에서 지배적 인 지역으로 설립되었습니다. 지역은 세계에서 가장 큰 제약 회사 중 일부이며, pharmacovigilance 서비스를 전문으로 많은 계약 연구 조직 (CROs). FDA와 같은 규제 기관에 의해 부과 된 약물 안전 모니터링에 대한 엄격한 규제 요구 사항은 강력한 약국 시스템을 구축하는 제약 및 생명 공학 회사에 의해 상당한 투자를 구동하고있다.
아시아 태평양 약국 시장 분석 및 동향
아시아 태평양 지역은 전 세계적으로 pharmacovigilance 산업을 위한 가장 빠른 성장 시장으로 출범했습니다. 이 제품은 다국적 플레이어가 임상시험을 확장하고 로컬 CRO의 전문성을 키우는 유전자 생산을 가속화하는 것으로 나타났습니다. 인도, 특정, 낮은 비용의 가용성 때문에 pharmacovigilance 서비스의 세계 sourcing 목적지로 출현, 숙련 된 인력.
주요 제약 회사 중 일부는 지역 pharmacovigilance 센터를 설정하거나 인디언 CROs와 협력하여 포스트 마케팅 안전 활동을 집중합니다. 동시에, 아시아 태평양의 약 규제 기관은 약국과의 연결 규정을 강화하고 안전 모범 사례를 격려했습니다.
글로벌 약국 시장 지배 국가
미국 약국 시장 분석 및 동향
미국은 pharmacovigilance 시장을 글로벌 수준에서 지배하고, 그것의 잘 설립한 pharma 분야 및 엄격한 규칙 체계에 owing의 기간에 있는 큰 기여를 추가합니다. 미국 식품 및 의약품 관리 (FDA)은 엄격한 정책, 안전 모니터링 서비스에 대한 수요 향상을 통해 pharmacovigilance의 포괄적 인 관행을 엄격하게 보장합니다.
다국적 제약 회사뿐만 아니라 계약 연구 조직 (CRO)은 더 부스트에 기여하고, 따라서 미국은 약국 활동의 리더십 역할을합니다. 또한, 인공 지능과 빅 데이터 분석과 같은 새로운 기술의 증가 된 섭취는 시장 성장에 연료를 추가합니다.
시장 보고서 Scope
약력 시장 보고서 적용
| 공지사항 | 이름 * | ||
|---|---|---|---|
| 기본 년: | 2024년 | 2025년에 시장 크기: | USD 8.23 파운드 |
| 역사 자료: | 2020년에서 2024년 | 예측 기간: | 2025에서 2032 |
| 예상 기간 2025년에서 2032년 CAGR: | 8.3% 할인 | 2032년 가치 투상: | USD 14.03 파운드 |
| 덮는 Geographies: |
| ||
| 적용된 세그먼트: |
| ||
| 회사 포함: | Accenture, Cognizant Technology Solutions, 미국 홀딩스 (LabCorp), IBM Corporation, QuintilesIMS (IQVIA), ICON plc, Capgemini, ITClinical, TAKE Solutions Ltd, BioClinica, PAREXEL International Corporation, Wipro Ltd, FMD K&L, Linical Accelovance, United BioSource Corporation (UBC), PRA Health Sciences, ArisGlobal 솔루션 및 Ennov Inc. | ||
| 성장 운전사: |
| ||
| 변형 및 도전 : |
| ||
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
약력 최근 개발 (주)
- 에 2월 6, 2024, 로버트 볼미국 FDA Office of Security and Epidemiology (OSE)의 부장은 DIA Global Pharmacovigilance 및 Risk Management Strategies Conference에서 FDA가 인공 지능과 약리학 노력을 강화하고 있다고 발표했습니다. FDA의 정보 시각화 플랫폼 (InfoViP)는 2022 년에 시작되었으며 AI를 사용하여 애드버스 이벤트 보고서를 검토하고 2 백만 달러를 초과하는 프로세스를 간소화하는 것을 목표로합니다. 또한 FDA는 표준 위험 평가 및 Mitigation Strategies (REMS) 데이터를 사용하여 접근성 및 가용성을 향상시킵니다.
- 인도 8 월 2024에서 소개 약물 반응 모니터링 시스템 (ADRMS) 소프트웨어 pharmacovigilance 소프트웨어는 약과 의료 기기와 관련된 불리한 사건의 수집 그리고 검사를 촉진하고, 따라서 환자와 의료 전문가를 위한 보고 과정을 더 쉽게 만들기.
- 2024년에, Cognizant는 pharmacovigilance 케이스의 가공을 자동화하기 위하여 기계 학습 몬 해결책을 소개했습니다. 이 혁신은 불리한 약 반응 (ADR) 탐지의 정확도 그리고 속도를 개량합니다.
Analyst의 주요 Takeaways:
- 글로벌 pharmacovigilance 시장은 약물 포스트 마케팅 승인의 안전 모니터링에 대 한 증가 필요에 의해 구동 하는 예측 기간에 상당한 성장을 경험 하는 것입니다. 주요 국가 전역의 pharmacovigilance에 대한 엄격한 규제 요구 사항은 pharmacovigilance 서비스에 대한 수요를 제안합니다.
- 북미는 현재 시장은 엄격한 규제 위임 및 주요 아웃소싱 회사의 존재를 옹호합니다. 그러나 아시아 태평양은 중국과 인도와 같은 국가에서 일반 의약품 제조를 증가하여 가장 빠른 속도로 성장할 것으로 예상됩니다.
- pharmacovigilance 활동의 아웃소싱회사 소개서비스 제공 업체는 핵심 운영에 비용 및 초점을 최적화하는 제약 회사 중 글로벌 트렌드가되고 있습니다. 다른 한편으로는 숙련 된 인력의 부족과 경쟁 요구는 시장의 성장을 몇 가지 범위로 hamper 할 수 있습니다. Biologics와 같은 소설 약의 효능 세포 및 유전자 치료 또한 새로운 안전 모니터링 메커니즘과 관련하여 상당한 기회를 제공합니다. 인공 지능과 블록체인과 같은 첨단 기술을 채택하여 신호 감지를 위한 pharmacovigilance 관행을 혁명시킬 수 있습니다. 이러한 붕괴는 안전 모니터링을 더 능동적이고 정확하고 비용 효율적인 것입니다.
시장 Segmentation
- 임상 시험 단계 통찰력 (Revenue, USD Bn, 2020 - 2032)
- 임상연구
- 임상시험 단계 I
- 임상시험 단계 II
- 임상시험 단계 III
- 마케팅 감시 또는 단계 IV
- 방법 통찰력의 유형 (Revenue, USD Bn, 2020 - 2032)
- Spontaneous 보고
- 통합 ADR 회사연혁
- 목표 보고
- Cohort 이벤트 모니터링
- 사이트맵 관련 기사
- 서비스 제공자 통찰력 (Revenue, USD Bn, 2020 - 2032)
- 내 집
- 계약 아웃소싱
- 지역 통찰력 (Revenue, USD Bn, 2020 - 2032)
- 북아메리카
- 미국
- 한국어
- 라틴 아메리카
- 인기 카테고리
- 아르헨티나
- 주요 시장
- 라틴 아메리카의 나머지
- 유럽 연합 (EU)
- 한국어
- 미국
- 이름 *
- 한국어
- 담당자: Mr. Li
- 러시아
- 유럽의 나머지
- 아시아 태평양
- 중국 중국
- 주요 특징
- 일본국
- 담당자: Ms.
- 대한민국
- 사이트맵
- 아시아 태평양
- 중동
- GCC 소개 국가 *
- 한국어
- 중동의 나머지
- 주요 특징
- 대한민국
- 북한
- 대한민국
- 키 플레이어 Insights
- 채용 정보
- Cognizant 기술 솔루션
- 미국 홀딩스 연구소(LabCorp)
- IBM 회사
- 비옥한 (IQVIA)
- 아이콘 plc
- 카테고리
- ITClinical 정보
- TAKE 솔루션
- BioClinica의 특징
- 파스텔 회사 소개
- 회사 소개
- 라디오 K&L
- 의료기관
- 미국 BioSource Corporation (UBC)
- PRA 건강 과학
- 아리스글로벌
- Ennov 솔루션 Inc
공유
저자 정보
Manisha Vibhute는 시장 조사 및 컨설팅 분야에서 5년 이상의 경험을 가진 컨설턴트입니다. 시장 역학에 대한 강력한 이해를 바탕으로 마니샤는 고객이 효과적인 시장 접근 전략을 개발하도록 지원합니다. 그녀는 의료 기기 회사가 가격 책정, 환불 및 규제 경로를 탐색하여 성공적인 제품 출시를 보장하도록 돕습니다.
독점적인 트렌드 보고서로 전략을 혁신하세요:
자주 묻는 질문