Dravet 증후군 치료 시장 크기와 예측 – 2025 – 2032
Global Dravet Syndrome Treatment Market size는 2025년 USD 1.2 억에 달하는 것으로 추정되며 2032년까지 USD 2.8 억에 도달 할 것으로 예상되며 2025년에서 2032년까지 13.5%의 연간 성장률 (CAGR)을 전시합니다.
제품정보
Dravet 증후군 치료는 가혹한, 약 저항하는 epileptic seizures를 전형적으로 infancy에서 집중합니다. 제품 포트폴리오에는 항염증제 (AEDs), cannabinoid 기반 치료제 및 소설 유전자 표적 치료제가 포함됩니다. FDA 승인 옵션 등 교반, fenfluramine, cannabidiol 크게 개선 된 seizure 제어 및 환자 결과.
vagus 신경 자극 장치 및 ketogenic식이 요법을 포함하여 Adjunct 치료는 또한 seizure 관리를 강화하기 위하여 이용됩니다. 최근 혁신 유전자 치료 SCN1A 유전자에서 유전자 변이를 해결하는 데 중점을 둔 정밀 의학 접근법은 장기 질병 수정을위한 새로운 희망을 제공합니다.
키 테이크아웃
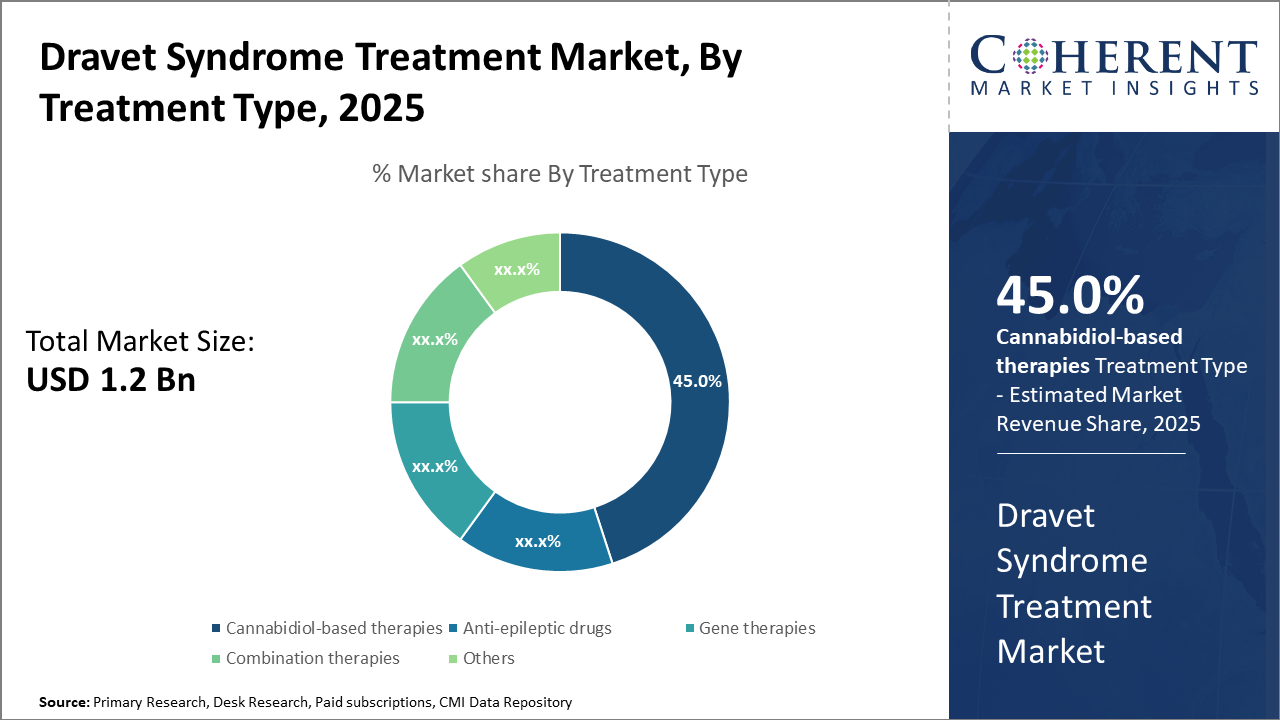
Cannabidiol 근거한 치료 세그먼트는 치료 유형에 있는 가장 큰 시장 점유율을, 비 전통 선택권을 위한 규제 승인 그리고 환자 선호에 의해 몰았습니다.
병원 약국은 선호하는 접근성 및 전문 감독으로 유통 채널 세그먼트를 지배합니다.
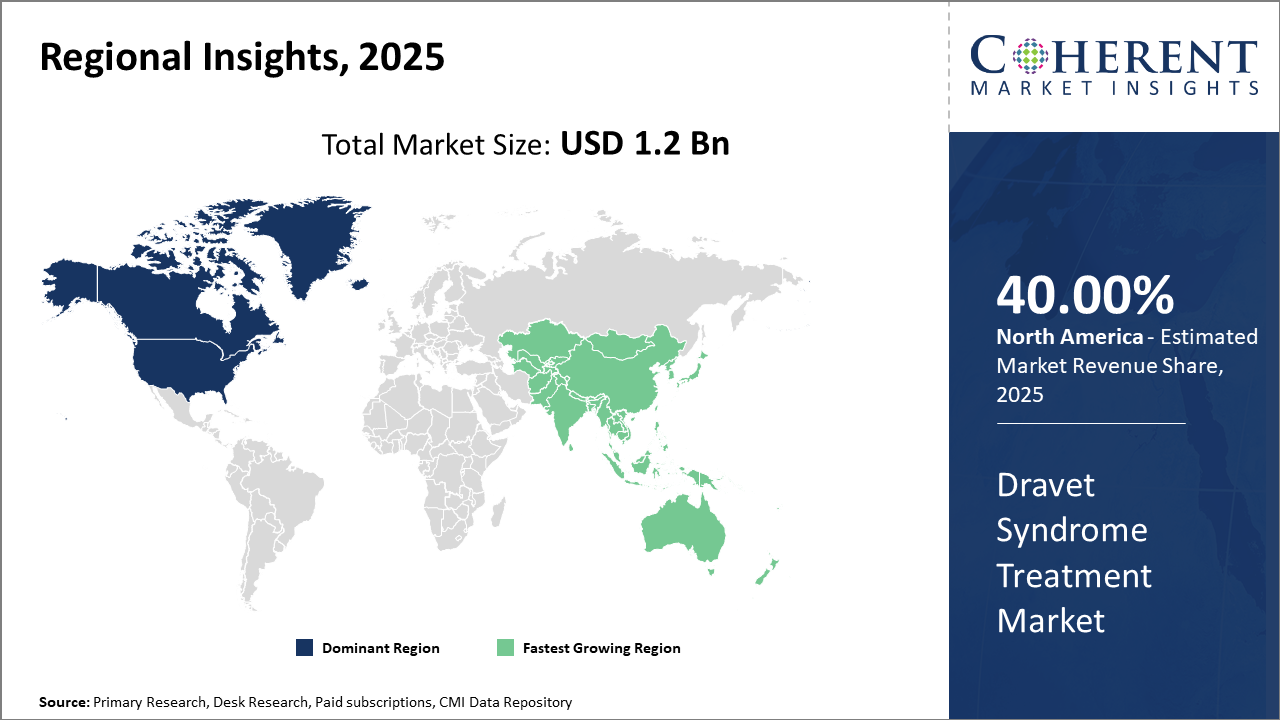
북미는 혁신적인 치료 시작과 더 높은 채택률을 지원하는 견고한 인프라로 시장 수익을 이끌어 냅니다.
아시아 태평양은 가장 빠른 CAGR를 보여줍니다, 주로 향상된 의료 인프라 및 정부 이니셔티브 희귀 질환 진단을 촉진
Dravet 증후군 치료 시장 세그먼트 분석
이 보고서에 대해 자세히 알아보려면: 무료 샘플 다운로드
Dravet 증후군 치료 시장 통찰력, 치료 유형에 의해
Cannabidiol 기반 치료는 약 45%의 시장 점유율을 지배하고, 잘 문서화 된 효능 및 규제 승인에 의해 추진. 이 세그먼트는 광범위한 의사 채택과 환자 수용을 증가, 특히 소아과 경우. Gene therapies는 가장 빠르게 성장하는 subsegment를 대표하며, 유전적 보정 방법에서 획기적으로 연료를 공급합니다. Anti-epileptic 약은 기초 치료 형태로 인하여 임상 사용 및 넓은 가용성을 수립하는 중요한 세그먼트를 유지한다.
Dravet Syndrome 치료 시장 통찰력, 신청
응용 프로그램의 관점에서, 가장 큰 시장 점유율에 대한 소아과 사용 계정, Dravet 증후군의 초기 설정 특성을 반영하고 초기 개입 전략의 우선 순위. 이 subsegment에 있는 수요는 생활의 질을 개량하고 seizure 사건을 감소시키기에 Caregivers의 초점에 의해 우선적으로 몬 입니다. 성인 사용은 개량한 처리 선택권으로 가장 빠른 성장한 subsegment는 수명을 연장하고 성숙한 환자 관리를 강화합니다. Geriatric 사용은 고급 연령대에서 증후군의 강렬로 인해 제한되어 있지만 더 긴 생존률에주의를 기울입니다.
Dravet Syndrome 치료 시장 통찰력, 유통 채널에 의해
병원 약국은 전문 치료 관리 및 모니터링을위한 전문 감독의 필요성에 약 55%의 지배적 인 시장 점유율을 보유합니다. 이 설정은 병원 공식 및 임상 시험 네트워크를 통해 새로 출시 된 치료에 대한 액세스를 용이하게합니다. 온라인 약국은 가장 빠르게 성장하는 채널을 나타냅니다, 증가 디지털 건강 채택 및 향상된 접근성, 특히 보존 지역에서 구동. 소매 약국은 꾸준한 수요를 유지하고, 1 차적으로 정비 치료 및 보충 처방전을 봉사합니다.
Dravet Syndrome 치료 시장 동향
Gene therapies에 대한 지속적인 진화는 Dravet Syndrome 치료 시장을 더 효과적인 장기 솔루션을 도입하여 변형했습니다.
예를 들어 Stoke Therapeutics의 ASO 기반 치료의 진행을 포함, 이는 최근 단계 2 재판에서 45% 감소를 보여.
또한, CBD 기반 제품 승인의 큰 파도는 전 세계적으로, 특히 포스트 2024 FDA 확장, 주류 치료제로 cannabidiol에 위치했다.
seizure 모니터링 및 치료를위한 디지털 건강 플랫폼의 통합은 기술 및 치료 패러다임의 confluence를 준수하고 시장 변화에 대한 서명 질병 관리·
Dravet 증후군 치료 시장 통찰력, 지리학
이 보고서에 대해 자세히 알아보려면: 무료 샘플 다운로드
북미 Dravet Syndrome 치료 시장 분석 및 추세
북미에서 Dravet Syndrome 치료 시장의 지배는 포괄적 인 의료 생태계, 강력한 규제 프레임 워크 및 GW Pharmaceuticals 및 Zogenix와 같은 주요 시장 회사의 존재에 의해 bolstered. 지역은 2025 년에 거의 40 %의 시장 점유율을 차지하고, 유리한 정부 정책과 혁신적인 치료에 대한 환자 접근을 촉진하는 재투자 계획에 의해 지원됩니다.
Asia Pacific Dravet Syndrome 치료 시장 분석 및 동향
한편, 아시아 태평양은 16%를 초과하는 CAGR와 가장 빠른 성장을 전시하고, 의료 인프라를 확장하여 중국과 인도와 같은 국가의 임상 시험 활동을 증가시키고, 드문 유전 적 균류의 인식을 증가시킵니다. 적혈구 연구 및 신흥 지역 제약 회사는 또한 지역의 급속한 시장 성장에 기여하는 것을 목표로 하는 정부 이니셔티브.
Dravet Syndrome 치료 시장 Outlook for Key 국가
미국 Dravet Syndrome 치료 시장 분석 및 동향
미국 시장은 2025 년 가장 큰 수익 기여자를 대표하며 Epidiolex 및 Promising gene therapies를 포함한 광범위한 환자 인구 및 고급 치료 승인으로 인해되었습니다. 드문 질병 치료를위한 보험 적용의 2024 확장은 크게 향상된 치료 접근성을 가지고 있으며 지속적인 FDA 빠른 트랙 디자인은 파이프 라인 제품을 가속화합니다. GW Pharmaceuticals 및 Zogenix와 같은 시장 플레이어는 다음 세대 치료법을 개발하기 위해 학술 기관과 협력하여 미국 시장의 혁신 허브 역할을 통합합니다.
독일 Dravet Syndrome 치료 시장 분석 및 동향
독일의 시장은 강력한 의료 인프라와 정부 기금을 통해 희귀 신경 질환 연구. 정밀의학 채택은 글로벌 기업과 파트너 관계를 맺고 compassionate 사용 프로그램을 확장합니다. 독일의 Reimbursement 시스템의 플래티넘 약물에 대한 유연성은 새로운 치료에 실질적인 환자 접근을 보장, 시장의 수익 성장. 또한, 유명한 연구 센터의 존재는 치료 풍경을 촉진하는 지속적인 임상 시험 촉진.
항문 Opinion
Escalating demand for Precision Medicine treatments tailored to genetic epilepsies 표피 성장 드라이버. 2024의 최근 임상 시험은 SCN1A 유전자의 mutations를 대상으로하는 유전자 치료가 환자의 결과를 향상시키기 위해 개인화 된 접근 방식을 채택하는 환자의 40 % 이상으로 60 % 이상의 환자에 의해 두드러지게 감소했습니다. 이러한 치료 혁신은 전통적인 방부제 약에 고급 치료의 시장 점유율을 증가 할 것으로 예상됩니다.
Cannabidiol (CBD) 근거한 정립은 다수 지구에 있는 강한 임상 검증 및 규제 승인 때문에 처리 의정서를 지배하는 것을 계속합니다. 2025 년 보고서는 CBD 기반 제품 계정이 총 시장 수익의 거의 45 %를 나타내며, 주로 기존 치료와 비교하여 효능 및 감소 된 부작용으로 구동되며 시장 확장에 대한 수요 측면 드라이버를 강조합니다.
가격 역동성은 중요한 micro-indicator 셰이핑 시장 수익을 유지. 일반적인 정립 및 특허 만료의 도입은 업계 점유율을 뛰어넘지 않고 온건한 가격 감소를 가져올 가능성이 있습니다. 예를 들어, 늦은 2024 년, 선도적 인 CBD 기반 약물 중 하나가 15 %의 가격 컷 포스트 패턴 expiry를 경험했으며, 소아과 인구 중 처방량에 상승합니다.
아시아 태평양 시장의 주요 수입업체로 알려진 북미와 유럽의 글로벌 수요를 변화시키는 전문 약물의 수입 수출 패턴은 지역 제조 역량을 강화하고 있습니다. 2025년에, 미국은 수입한 Dravet 증후군 치료에 있는 20% 증가를 목격했습니다, 성장 환자 기초와 처리 채택을 반영해서, 시장 크기에 긍정적인 전망 신호.
시장 범위
| 공지사항 | 이름 * | ||
|---|---|---|---|
| 기본 년: | 2025년 | 2025년에 시장 크기: | 100억 |
| 역사 자료: | 2020년에서 2024년 | 예측 기간: | 2025에서 2032 |
| 예상 기간 2025년에서 2032년 CAGR: | 15% 할인 | 2032년 가치 투상: | 100억 |
| 덮는 Geographies: |
| ||
| 적용된 세그먼트: |
| ||
| 회사 포함: | Zogenix, Inc., GW Pharmaceuticals (재즈 제약의 자회사), Marinus Pharmaceuticals, Inc., Stoke Therapeutics, Biogen Inc., UCB Pharma, Lundbeck, Aquestive Therapeutics, Zynerba Pharmaceuticals, Amneal Pharmaceuticals, Innovus Pharmaceuticals, Neurelis, Inc. | ||
| 성장 운전사: |
| ||
75개 이상의 매개변수에서 검증된 매크로와 마이크로를 발견하세요, 보고서에 즉시 액세스하세요
Dravet 증후군 치료 시장 성장 인자
Dravet 증후군을 포함하여 희귀 한 소아과 간질 질환의 상승 예비 발병은 2024 년 간질 연구와 함께 중요한 시장 성장 드라이버로 봉사하고 전 세계적으로 15,000 명의 출생의 약 1의 발병률을보고합니다. 약물 개발의 혁신은 다른 구동력이며, 규제 빠른 트랙 메커니즘을 자본화하는 유전자 치료 및 CBD 기반 제품에 대한 임상 개발 시간을 가속화하여 특징으로합니다. 증가된 인식 캠페인 및 개선된 진단 비율은 더 처리 채택율을, 시장 범위를 확장하. 북미와 유럽과 같은 주요 지역에서 선호하는 수익 정책은 지속 가능한 시장 성장에 기여하는 시장의 접근성과 수익 흐름을 개선합니다.
Dravet Syndrome 치료 시장 개발
1월 2025일 FDA는 Relutrigine (PRAX-562)를 수여했습니다. Dravet 증후군을 위한 희귀한 소아과 질병 지적, SCN2A-DEE와 SCN8A-DEE를 위한 이전 지적에 추가하십시오. 이 지적은 Praxis 정밀도 약, seizures를 통제하기 위하여 persistent 나트륨 현재를 금하는 작은 분자에 의해 개발된 약을 위해 입니다.
12월 2024일· Stoke 치료 Zorevunersen (STK-001)에 대한 미국 FDA의 Breakthrough Therapy Designation을 받았다. 환자의 Dravet 증후군에 대한 antisense oligonucleotide 치료는 SCN1A mutations를 확인했습니다. ( gain-of-function mutations 제외). Phase 1/2a 및 open-label extension study의 임상 데이터는 표준 항시 약을 넘어 인식 및 행동에 대한 인식 및 지속적인 개선에 실질적 및 지속적인 감소를 보여주었다.
키 플레이어
시장의 선도 기업
주식회사 Zogenix
GW Pharmaceuticals (재즈 제약 자회사)
Marinus 제약, Inc.
Stoke 치료
UCB 소개 약력
사이트맵
Aquestive 치료
Zynerba 제약
Amneal 약제
Innovus 제약
주식회사 니어리
몇몇 시장 선수는 그들의 발자국을 확장하기 위하여 제품 혁신 및 전략적인 파트너십을 채택했습니다. 예를 들어, GW Pharmaceuticals의 성공적인 FDA 승인은 2024 년 Epidiolex 제품의 시장 수익과 공유를 크게 향상했습니다. 마찬가지로, Zogenix는 2025 년 초 Stoke Therapeutics의 인수로 강력한 유전자 치료 파이프라인 향상을 활성화하여 투자자의 신뢰와 비즈니스 성장을 증가시킵니다.
Dravet 증후군 치료 시장 미래 전망
Dravet 증후군 치료를위한 미래 전망은 심리학 관리에서 질병 퇴치 치료에 의해 강력하게 정의됩니다. 유전자 치료, antisense oligonucleotides 및 mRNA 기반 치료를위한 진행 임상 시험은 직접 표적 SCN1A mutations-the 유전적 뿌리 원인 질병을 대상으로합니다. 정밀의학 접근법은 게놈 sequencing 및 개인화 된 약물 디자인의 발전에 의해 지속적으로 확장 될 것입니다. 디지털 건강 플랫폼과 seizure 감시 기술은 실시간 관리와 환자 안전을 개량할 것입니다. 규제 기관 및 환자 자문 그룹은 혁신적인 치료를위한 더 빠른 승인 통로를 촉진하고 향후 몇 년 동안 Dravet 환자를위한 새로운 시대를 제안하고 있습니다.
Dravet Syndrome 치료 시장 역사 분석
역사적으로 Dravet 증후군의 관리는 대부분의 전통적인 항염증제 약에 그것의 저항 때문에 도전되었습니다. 수십 년 동안, 치료는 주로 valproate, clobazam 및 topiramate와 같은 광범위한 스펙트럼 항체를 사용하여 빈번하고 머리말을 붙였습니다. 그러나 환자는 종종 제한된 혜택과 상당한 부작용을 경험했습니다. 시간이 지남에 따라 의료 공동체는 증상을 완화하는 나트륨 채널 차단제의 조합 요법과 피를 자극하기 시작했습니다. 교질환, cannabidiol (Epidiolex)의 소개, 그리고 fenfluramine는 표적과 더 안전한 seizure 통제를 제안하는 중요한 이정표를 대표했습니다. ketogenic식이 요법, 행동 치료 및 지지 요법을 포함하여 pharmacological 진도에 병렬은 치료의 필수적인 부분이되었습니다. 유전 진단의 발전은 이전과 더 정확한 검출을 위해 허용, 개별화된 치료를 개선.
이름 *
1 차적인 연구 인터뷰:
신경학
소아과 Epileptologists
임상 약리학
희귀 질환 연구자
데이터베이스:
신경 장애 및 뇌졸중의 국립 연구소 (NINDS)
FDA Orphan 약 데이터베이스
잡지 :
Epilepsy 오늘
신경 과학
희귀 질병 보고서
제약 기술
저널:
Epilepsia는
Lancet 신경학
어린이 신경학
사이트맵 의약품
신문 :
뉴욕 타임스 (Health)
가디언 (Science)
경제 시간 (Healthcare)
힌두교 (Health & Research)
협회 :
Epilepsy 재단
Dravet 증후군 재단
국제 리그에 대한 Epilepsy (ILAE)
미국 신경학 아카데미 (AAN)
공유
저자 정보
Ghanshyam Shrivastava - 경영 컨설팅 및 연구 분야에서 20년 이상의 경험을 가진 Ghanshyam Shrivastava는 수석 컨설턴트로서 생물학 및 바이오시밀러에 대한 광범위한 전문 지식을 제공합니다. 그의 주요 전문 분야는 시장 진입 및 확장 전략, 경쟁 정보, 다양한 치료 범주 및 API에 사용되는 다양한 약물의 다각화된 포트폴리오에 걸친 전략적 전환과 같은 분야입니다. 그는 고객이 직면한 주요 과제를 파악하고 전략적 의사 결정 역량을 강화하기 위한 강력한 솔루션을 제공하는 데 능숙합니다. 시장에 대한 그의 포괄적인 이해는 연구 보고서 및 비즈니스 의사 결정에 귀중한 기여를 보장합니다.
Ghanshyam은 업계 컨퍼런스에서 인기 있는 연설자이며 제약 산업에 대한 다양한 출판물에 기고합니다.
독점적인 트렌드 보고서로 전략을 혁신하세요:
자주 묻는 질문

