Hemophiliaは、患者の血液が凝固因子として知られている血漿タンパク質の欠如のために、通常は腐敗しない遺伝子障害です。 慣習的な処置の選択は特定の clotting の要因の時機を得た取り替えを含んでいます。 大手薬局やバイオテクノロジー企業は、従来の治療と様々な欠点により、血友病の遺伝子治療を開発するために研究開発を行っています。 治療および強力な製品パイプラインを必要とする多くの血友病患者の増加は、血友病遺伝子治療市場の成長を促進することが期待されます。
世界的な血友病遺伝子治療市場は、評価されると推定される US$ 330.9 百万 お問い合わせ 2022年 展示予定 カグレ について 43.6%の% 予報期間中 (2022-2030).
図1. グローバル Hemophilia 遺伝子治療市場シェア(%)、血友病タイプ、2022
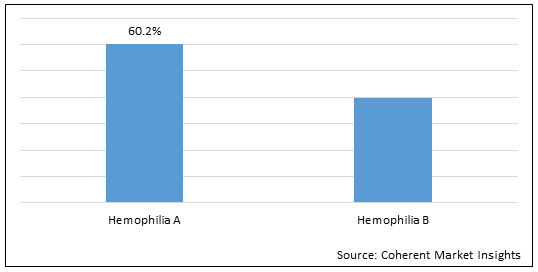
このレポートの詳細, サンプル コピーをリクエスト
血友病遺伝子治療市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2021年 | 2022の市場のサイズ: | US$ 330.9 Mnの |
| 履歴データ: | 2017年~2020年 | 予測期間: | 2022年~2030年 |
| 予測期間 2022〜2030年CAGR: | 43.6% | 2030年 価値の投射: | US$ 2,197.9 から ログイン |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | BioMarin Pharmaceuticals, Inc., Spark Therapeutics, Pfizer, Inc., UniQure NV, Ultragenyx Pharmaceutical, Shire, Sangamo Therapeutics Inc., およびFreeline Therapeutics. | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータで検証されたマクロとミクロを明らかにする, レポートにすぐにアクセス
開発途上国で世界中に広がる血友病患者基盤は、血友病遺伝子治療市場の成長を促すことが期待されています。
血友病の高い罹患率は、予測期間にわたって市場成長を促進するために計画されている病気の持続可能な治療のための需要が増加しています。 国立血友病財団ファクトシート2018によると、世界中の400,000人を超える個人に影響を受けた血友病。 また、同じソースによると、血友病に苦しんでいる患者の推定75%は治療にアクセスしたり、不十分な治療を受けることができません。 疾病管理予防センター(CDC)報告によると、ヘモフィリア 5,000人の生の男性の出産のうち1で起こる。 それはヘモフィリアBよりも4倍以上一般的です。ヘモフィリアのために利用可能な効果の高い治療は、組換えバイオテクノロジーまたはヒト血漿によって製造された高価な薬の寿命の注入を必要とします。
さらに、2019年9月、マネージドケアのアメリカンジャーナルによると、メタアナリシスは、世界中の1,125,000人の男性が遺伝性出血障害を持っていることを示しています。 それらの418,000は、ほとんど診断されていない病気の厳しいバージョンを持っています。 以前は、世界中で400,000人だけが血友病を抱えていると推定されました。
この研究では、10万人の男性が、次のようなものがあります。
- hemophilia Aのすべての多様性のための1つのケース
- 重度のhemophilia Aのための0の場合
- hemophilia Bのすべての多様性のための8つのケース
- 重度のhemophiliaのための場合 ツイート
100,000人の男性につき、出産時の優先順位は次のとおりです。
- hemophilia Aのすべての重症のための6つのケース
- 重度のhemophilia Aのための5つの場合
- hemophilia Bのすべての重症のための0のケース
- 重度のhemophilia Bのための5つの場合
血友病で生まれた人にとって、通常の持続期間と品質の生活を生きるチャンスは、上中所得国で64%、中所得では77%、低所得国では最大93%減少します。 2020年に、ヘモフィリア(WFH)の世界連盟は、世界中にヘモフィリアAと33,076人で165,379人を特定しました。
また、病気の予防と予防のためのセンターによると、血友病 5,000人の男性の出生と約400人の赤ちゃんが毎年血友病Aで生まれます。
プロフィール 2.グローバルヘモフィリア 遺伝子治療市場シェア(%)、地域別、2022
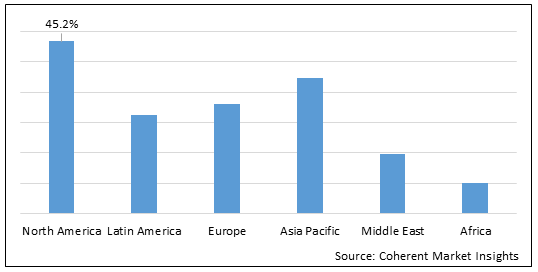
このレポートの詳細, サンプル コピーをリクエスト
血友病治療のための強力な遺伝子ベースの製品パイプラインは、血友病遺伝子治療市場成長を促進することが期待されます
hemophiliaのための遺伝子治療は、近い将来市場で参入することが期待されている強力な製品パイプラインを持っています。 それはhemophiliaの管理のための新しい処置の選択の可用性をもたらすので、これは市場成長を運転する予定です。 2019年1月には、15以上の治験遺伝子治療が臨床開発段階にあります。 2018年12月、Spark Therapeuticsは、ヘモフィリアAの調査SPK-8011の進行中のフェーズ1/2臨床試験のための更新された予備データを発表しました。
血友病を治療するための現在の治療法は、凝固因子XIIIまたはIXを投与することによって、病気の症状管理のみである。 さらに、プラズマ由来製品に関連した深刻な副作用があり、治療へのアクセスが制限されています。 遺伝子治療は、特定のレベルにこれらの問題に対処することができます。 BioMarinの薬剤の遺伝子治療プロダクトValoctocogene roxaparvovecのためのhemophilia Aは2019年の臨床開発のフェーズIIIにありました。
さらに、2021年1月、臨床研究のリーグ、ロシアは、ヘモフィリアAを治療するためにEfmoroctocogアルファ注射[Eloctate]のためのインターベンショナル研究を実施しました。 現在、フェーズ4では研究が終了し、2022年11月15日に研究が終了と推定されています。
グローバル Hemophilia 遺伝子治療市場 – コロナウイルスの影響 (COVID-19) パンデミック
2019年12月に発生したCOVID-19ウイルスの感染拡大に伴い、世界保健機関が2020年1月30日に公衆衛生緊急事態を宣言しました。
COVID-19は、流通チャネルの混乱を発生させ、企業や金融市場への金融影響を通じて、医薬品、医療機器、栄養補助食品などの生産と需要に直接影響を及ぼすことで、経済に影響を及ぼすことができます。 中国、インド、サウジアラビア、U.A.E.、エジプトなど、全国のロックダウンにより、薬物の輸送に関する問題に直面しています。
しかし、COVID-19パンデミックは、COVID-19パンデミックによる研究開発活動の減少に陥った世界的な血友病遺伝子治療市場に悪影響を及ぼしました。 例えば、新型コロナウイルスの予防に用いられるワクチンの開発のための国立研究開発センターによると、2020年7月には、COVID-19パンデミックの時に優先的に開発されたワクチンの研究開発活動が挙げられました。 WHOの応答の一環として、R&D Blueprintは、この新型コロナウイルスに対する診断、ワクチンおよび治療薬を加速するために活性化しました。 Blueprintは、科学者とグローバルヘルスの専門家との間の協調性を改善し、研究開発プロセスを加速し、グローバルな反応で学び、改善するための新しい規範と基準を開発することを目指しています。 2020年1月30日、WHO理事長は、国際問題(PHEIC)の公衆衛生緊急事態を構成すると宣言した。 COVID-19の世界の科学者たちは、2020年2月11日〜12日に世界保健機関のジュネーブ本社で会い、新しいウイルスに関する知識の現在のレベルを評価し、緊急に答える必要がある重要な研究の質問に合意し、この破壊を抑制し、将来のために準備するための優先的な研究を加速し、資金を供給するために一緒に働く方法を見つける。 したがって、それは血友病の治療で使用される薬の研究と開発活動を遅くしました。
グローバル Hemophilia 遺伝子治療 市場: 主な開発
2022年7月、Sanofi社、医薬品・ヘルスケア会社、スウェーデンOrphan Biovitrum社、バイオ医薬品会社は、efanesoctocogアルファの開発・商品化に協力しています。 米国食品医薬品局(FDA)は、フェネソクトコグアルファ(BIVV001)へのブレークスルー療法の指定を、ヘモフィリアAの人々の治療のために、まれで生命を脅かす出血障害、ピボタルXTEND-1フェーズ3の研究からのデータに基づいて認めた。 EfanesoctocogアルファはFDAによってブレークスルー療法の指定を与えられる最初の要因VIII療法です。 Efanesoctocogアルファは、週1回程度の予防処置レジメンの週の過半数のための正常な要因活動レベルに正常に提供するように設計された新しく、調査因子VIII療法です。 ブレークスルーセラピーの指定は、深刻なまたは生命を脅かす条件をターゲットとする米国における薬の開発と見直しを明示するために設計されています。 この指定のために修飾する薬は、薬が利用可能な治療上の臨床的に重要なエンドポイントに対する実質的な改善を示す可能性がある予備臨床証拠を示す必要があります。
グローバル Hemophilia 遺伝子治療 市場: 拘束
世界的な血友病遺伝子治療市場の成長を妨げる主要な要因には、プラズマ由来製品に関連する深刻な副作用、および血友病治療への限られたアクセスが含まれます。 例えば、2019年9月には、バイオテクノロジー情報センターによると、凝固因子による治療の大きな合併症は、因子VIIIまたはIXに対して指示されるアオアンティーバーの開発です。 血友病の一般的な長期合併症は、繰り返し出血エピソードによって引き起こされる関節(肝症)に永久的な損傷です。
キープレイヤー
世界的なhemophilia遺伝子治療市場で動作する主要なプレーヤーには、BioMarin Pharmaceuticals, Inc.、Spark Therapeutics、Pfizer、Inc.、UniQure NV、Ultragenyx Pharmaceutical、Shire PLCが含まれます サンガモセラピューティクス株式会社、フリーラインセラピューティクス
独占トレンドレポートで戦略を変革:
よくある質問


