Hemoglobinopathyの処置の薬剤の市場は2025年のUSD 5.29 Bnで評価され、USD 9.3に達すると期待されます 2032年にBn、2025年から2032年までの8.4%の化合物年間成長率(CAGR)を展示。
グローバルヘモグロビノパシー治療薬市場に関するアナリストの意見:
遺伝子疾患、新製品の発売、合併、買収、コラボレーションなどの戦略の普及は、予測期間における世界的なヘモグロビノパシー治療薬市場成長を加速する見込みです。 たとえば、世界保健機関が公表するデータによると、2021年9月7日、30万人から400,000人の赤ちゃんが毎年深刻なヘモグロビン障害で生まれ、これらの出生の90%が低・中所得国で起こる。
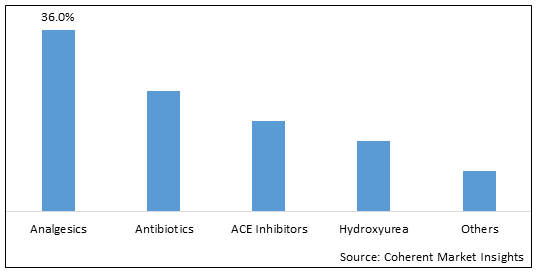
図1. グローバルヘモグロビノパシー治療薬市場シェア(%)、医薬品の種類、2025
このレポートの詳細, サンプル コピーをリクエスト
グローバルヘモグロビノパシー治療薬市場-ドライバー
hemoglobinopathyの処置の研究開発の活動の増加
hemoglobinopathy治療における研究開発活動の増加は、予測期間にわたって世界的なヘモグロビノパシー治療薬市場成長を促進することが期待されます。 たとえば、2022年6月16日、米国に拠点を置く研究機関である国立心、肺、血液研究所(NHLBI)の研究者は、赤血球中のタンパク質の活性化が貧血を改善し、人々と暮らす人々のための激しい痛みの急性エピソードを軽減することを発表しました。 病気の細胞病気お問い合わせ ピルビン酸キナーゼ(PKR)活性を刺激する治療は、PKR欠乏症がPKLR遺伝子の変異によるので、重度の痛みの危機を防止または軽減することができます。 新薬は、継承されたピルビン酸キナーゼ欠乏症で患者を治療することができることを開発しています。 初期フェーズ 1 臨床研究試験, 経口療法を介して SCD 患者で PKR を活性化することが安全かつ十分に許容されたことを示しました. 研究者は、今後もさらなる研究で長期にわたる安全・有効性を評価してまいります。 この経口療法が経験する病気のイベントの数を減らし、貧血を改善できるかどうかを具体的に見ていきます。
hemoglobinopathy治療のための新療法の承認の増加
hemoglobinopathy治療の新しい療法の承認の増加は、世界的なヘモグロビノパシー治療薬市場成長を促進することが期待されています。 たとえば、2022年2月17日、Agios Pharmaceuticals, Inc.は、遺伝的に定義された疾患の治療を開拓する細胞代謝の分野で米国ベースの製薬会社であるAgios Pharmaceuticals, Inc.は、米国食品医薬品局(FDA)が、ピルビン酸キナーゼ(PK)欠乏症の成人における血友病の治療のために、米国でPYRUKYND(緩和)を承認したことを発表しました。 PYRUKYNDは、ファーストクラスの経口PK活性化剤であり、この病気のための最初の承認された疾患修飾療法です。 成功したACTIVATEとACTIVATE-Tの研究は、PK欠乏症と貧血を大幅に改善するミタピバトの影響を示しています。
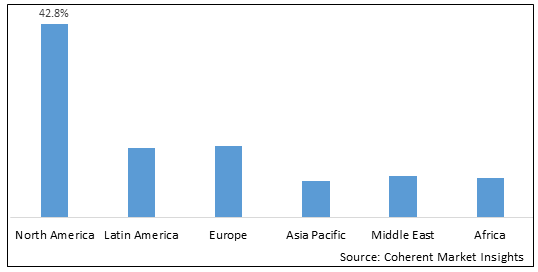
図2. グローバルヘモグロビノパシー治療薬市場シェア(%)、地域別、2025
このレポートの詳細, サンプル コピーをリクエスト
グローバルヘモグロビノパシー治療薬市場-地域分析
地域の中で、北米は、予測期間にわたって世界的なヘモグロビノパシー治療薬市場で優勢な地位を保持すると推定され、パートナーシップを増加させる。 たとえば、2021年11月11日、米国に拠点を置く商業段階のバイオ医薬品会社および病気の治療のリーダーであるEmmaus Life Sciences, Inc.は、UpScript IP Holdings, LLCとのパートナーシップを発表しました。米国ベースの消費者医薬品プロバイダーは、病気の細胞疾患患者にテレヘルスソリューションを提供し、Endari、Emmausの処方Lグルタミン経口パウダーへのアクセスを拡大し、病気の細胞疾患の治療に役立ちます。
グローバルヘモグロビノパシー治療薬市場–コロナウイルスの影響(COVID-19)パンデミック
2019年12月に発生したCOVID-19ウイルスの感染拡大に伴い、世界保健機関は2020年1月30日に公衆衛生を宣言しました。
COVID-19は、流通チャネルの混乱や、企業や金融市場への金融影響を通じて、薬物の生産と需要に直接影響を及ぼす3つの主要な方法で経済に影響を与えました。 中国、インド、サウジアラビア、U.A.E.、エジプトなど、全国のロックダウンにより、薬物の輸送に関する問題が1か所から別の場所へ直面しています。
しかし、COVID-19のパンデミックは、血輸血率を低下させるため、世界的なヘモグロビノパシー治療薬市場にマイナスの影響を受けました。 hemoglobinopathyの処置で処置として血のtransfusionが要求されます。 しかし、COVID-19期の献血が減少しました。 例えば、2020年2月6日(金)から4月3日(日)まで、インドの献血率が大幅に減少し、家族医学会とプライマリケア会が公表した記事によると、インドの献血率は、2020年2月6日(火)から4月5日(火)まで大幅に減少しました。 国のロックダウン制限が最も厳格だったときに、インド中部で最低寄付額8,037が4月に見られました。
グローバルヘモグロビノパシー治療薬市場セグメンテーション:
グローバルヘモグロビノパシー治療薬市場レポートは、薬の種類、病気の種類、分布チャネル、地域に分けられます。
薬の種類に基づく、全体的なヘモグロビノパシーの処置の薬剤の市場は鎮痛剤、抗生物質、エースの抑制剤、ヒドロキシ尿素および他のに分けられます。 そのうち、鎮痛セグメントは、製品発売を増加させるため、市場を支配することが期待されます。
疾患の種類に基づく、全体的なヘモグロビノパシーの処置の薬剤の市場はthalassemia、病気の細胞病気および他のHbの変形の病気に分けられます。 これらの中で、病気の細胞疾患セグメントは、この病気の治療の増加による予測期間にわたって市場を支配することが期待されます。
配布チャネルに基づく、全体的なヘモグロビノパシーの処置の薬剤の市場は病院の薬局、小売薬局およびオンライン薬局に分けられます。 これらの中で、病院薬局のセグメントは、薬の入手のための病院薬局の数を増やすために、予測期間上の市場を支配することが期待されます。
地域に基づいて、 世界的なヘモグロビノパシー治療薬市場は、北米、中南米、欧州、アジア太平洋、中東、アフリカに分けられます。 そこで、北米のセグメントは、この地域で製品の発売を増加させることにより市場を支配することが期待されます。
すべてのセグメンテーションの中で、薬の種類セグメントは、主要な市場プレイヤーによる研究開発活動の増加による最も高い可能性を持っています。 たとえば、2021年10月19日、米国食品医薬品局(FDA)は、成人の治療のために、セロコキシブとトラカドル(Seglentis)を含むコンビネーションピルを承認し、急性疼痛を十分に強くして、オピオイド鎮痛を要求し、代替治療が十分な痛みを軽減するために失敗した。 Celecoxibは非ステロイドの抗炎症薬であり、Tramadolはオピオイドのアゴニストです。 Seglentis は celecoxib の 56 の mg およびトラムアドルの 44 の mg を含んでいます。 スペインに拠点を置く国際製薬会社であるEsteve Pharmaceuticals社が製造しています。
グローバルヘモグロビノパシートリートメント医薬品市場 断面分析:
欧州地域の主要市場プレイヤーによるヘモグロビノパシーの治療における新製品や技術の導入は、地域における疾患種別セグメントの増殖を促すことが期待されています。 例えば, 上 4 月 28, 2023, Akebia Therapeutics, Inc., 米国ベースのバイオ医薬品会社, 欧州委員会からの承認を受け、その経口低酸素化因子プロリルヒドロキシラス阻害剤 Vafseo をヨーロッパで販売する. Vafseo(vadadustat)は、慢性メンテナンス透析に関する成人の貧血のための1日の治療として承認されました。 承認は、すべての27 EU加盟国とアイスランド、ノルウェー、リヒテンシュタインに適用されます。 Vadadustatは32カ国で貧血を治療するために使用するために承認されています。 経口低キシアインダクシブル因子プロリンヒドロキシラス阻害剤は150mg、300mg、450mgの錠剤でECによって承認されました。 承認は貧血のために扱われる透析の7,500人の大人で行われる段階3の試験に基づいています。
Hemoglobinopathyの処置は市場報告の適用範囲を薬剤にします
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 5.29 ポンド |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 8.4% | 2032年 価値の投射: | 米ドル 9.3 Bn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | ブリストル・マイアス・スクイブ・カンパニー、GlycoMimetics Inc.、Pfizer Inc.、Anthera Pharmaceuticals Inc.、Eli LillyおよびCompany、MastのTherapeutics、Daiichi Sankyo Company株式会社、Novatis International AG、Bluebird Bio Inc.、HemaQuest Pharmaceuticals Inc.、Emaus Medical Inc.、Prolongの薬剤、Merck及びCo.、Medunik USA Inc.、SangamoのTherapeurapeutics、Inc.、Global Inc.の血栓症および薬剤の薬剤の薬剤のAccom。 | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータで検証されたマクロとミクロを明らかにする, レポートにすぐにアクセス
グローバル Hemoglobinopathy 治療薬市場: 主な開発
2021年10月18日 エスティーブ, スペインに拠点を置く国際医薬品会社、米国食品医薬品局(FDA)は、EsteveのR&Dチームによって開発された独自の製品であるSeglentis(celecoxibおよびTramadol Hydrochloride)を承認しました。 大人の急性疼痛の治療のために、セロコキシブ(抗炎症薬)と路面電車(鎮痛剤)の共同結晶形態で構成された革新的なファーストインクラス製品です。 米国市場参入に向けたESTEVE初の独自リサーチ製品です。 Seglentisは、celecoxibとTurcadol塩酸塩で構成されたコクリスタルを含む錠剤の取引名です。 4つの補完的な痛み緩和メカニズムを標的とするマルチモーダル治療アプローチで急性疼痛管理のために設計された新しい鎮痛剤です。 これは、マルチモーダル鎮痛剤と整列された急性疼痛管理のための新しい治療法オプションを提供します。
2021年3月22日 パシラバイオサイエンス株式会社 米国を拠点とする製薬会社である米国食品医薬品局(FDA)は、米国食品医薬品局(FDA)の承認を受けており、EXPARELラベルの拡張を求める補助食品(sNDA)の提出を承認し、患者6歳以上で使用し、外科用鎮痛剤を産生する。 この承認を得て、EXPARELは、6歳ほど若き小児の人口に対するFDAが初めてかつ唯一の局所鎮痛薬を承認しました。 sNDAは、手術を受けている小児患者におけるEXPAREL浸潤のフェーズ3 PLAY研究から肯定的なデータに基づいていました。 全体的な調査結果は4 mg/kgの線量で識別される安全心配無しの大人の患者のためのpharmacokineticおよび安全プロフィールと一貫しました。 PLAY研究では、患者様が12歳未満の患者様および6歳未満の患者様が12歳未満の患者様および12歳未満の患者様を対象に、EXPARELの安全性と薬効を評価するために98人の患者様を登録しました。 米国FDAのガイダンスでは、PLAY研究の主な目的は、EXPARELの医薬品および安全性を評価することであった。
2023年7月1日、インドは、病気を早期に検出し、治療で管理できるように、7つのクレアの若い部族をスクリーニングすることを目指し、国民の病気の細胞貧血の排除ミッションを開始しました。 2023年、国連予算で発表されたミッションは、17州の278地区の部族区域の0-40歳グループにおける人々の意識の創造と普遍的なスクリーニングに焦点を当てています。 政府は2047年までに病気を排除する計画です。 この使命は、病気の細胞遺伝的状態カードの配布を含み、病気の影響を受ける子供や家族の生活を保存します。 政府はまた、患者の治療と診断のための22の部族地区で血友病およびヘモグロビノパシーのための統合センターを確立しました。
2022年6月21日、米国バイオテクノロジー社のPrecision BioSciences, Inc.(Precision BioSciences, Inc.)は、スイスのNovatis AG社と共同開発およびライセンス契約を締結しました。 本契約の一環として、Precision BioSciences, Incは、特定のヘモグロビノパシーを含む疾患の潜在的な1回変形治療オプションとして、ゲノムの安全な港地にある治療用トランス遺伝子である、インサートするように設計されたカスタムARCUSの核を開発します。 一方、Novatis AGは、その後の研究、開発、製造、商品化活動に責任を負います。 プレシジョンは、75万ドルの支払いを受け、将来のマイルストーンの追加支払いで約1.4億米ドルの総計額を受け取る資格があります。
グローバルヘモグロビノパシー治療薬市場: 主なトレンド
hemoglobinopathyの処置のための高められた臨床試験
hemoglobinopathyの処置のための研究開発の活動は市場の成長を運転できます。 2021年11月6日、ブリストル・マイアス・スクイブ、米国に拠点を置く多国籍製薬会社、米国に拠点を置く臨床段階のバイオ医薬品会社であるAcceleon Pharma Inc.は、第2フェーズのBEYOND研究から最初のデータを発表しました。Reblozyl(luspatercept-aamt)、第1クラスのエリストロイド成熟剤、および非輸血依存症(NTT)の成人患者における最高のサポートケア。 結果は、Reblozylで治療された患者の77.7%が、プラセボアームの患者の0%と比較してヘモグロビン増加(≥1.0グラム/デシリットル)を達成したことを示しています。 患者報告された結果の変化もヘモグロビンの増加と関連しています。
主要な市場プレイヤーによる合意のような戦略
主要な市場のプレーヤー間の一致のような戦略は市場の成長を運転できます。 2020年9月8日、米国に拠点を置くバイオ医薬品会社であるGlobal Blood Therapeutics(Global Blood Therapeutics)は、Bahrain、Kuwait、Oman、Qatar、サウジアラビア、UAEのOxbryta(voxelotor)タブレットをBahrain、Kuwait、Oman、Qatar、Gulf Cooperation Council(GCC)地域として共同で知られるBiopharma-Middle Eastとアフリカの独占契約を締結したことを発表しました。 病気の細胞疾患(SCD)を生きるこの地域で10万人以上の年齢層が12歳以上であることが予想されます。 Oxbrytaは、ヘモグロビンの重合、SCDの赤血球の病気と破壊の根本原因を直接阻害する経口療法です。
グローバルヘモグロビノパシートリートメント医薬品市場: 拘束
臨床試験の撤退
臨床試験の撤退は、世界的なヘモグロビノパシー治療薬市場成長を妨げることが期待されます。 例えば、臨床試験サイト臨床治療によると。 plerixaforを使用して病気の細胞疾患(scd)の患者からの末梢血幹細胞のコレクションを研究するためにgov研究が行われました。 この研究は、成人および小児科のSCD患者におけるPlerixaforの安全性と有効性が始まったときには不明であったため、2023年4月7日に終了しました。 治療オプションなしで患者をリクルートすることは、倫理的に正当化できませんでした。
この拘束を相殺するために、適切な安全と有効性の評価は、研究の撤退を避けるために行われるべきです。
代替治療の可用性
骨髄のような代替治療の可用性は、世界的なヘモグロビノパシー治療薬市場成長を妨げることが期待されます。 骨髄移植 hemoglobinopathyのための唯一の信頼できる処置はほとんどの処置の選択として障害の徴候を減らすことに焦点を合わせています。 例えば、2021年6月13日、2023年6月13日、米国政府機関、保健省およびサービス管理局が公表したデータによると、非関連性4,276の関連骨髄およびコード血液移植が米国で行われた。 ドナーレジストリは、米国で9百万以上の潜在的なドナーが含まれています。 ほぼ268,000コードの血液ユニットは、ドナーレジストリにあります。 この合計は、国立コード血液在庫(NCBI)から111,000台以上で、2022年に3000台以上のNCBIユニットを追加しています。
この拘束を均衡させるためには、ヘモグロビノパシー治療薬の利点に対するより多くの意識が広がるはずです。
グローバルヘモグロビノパシートリートメント医薬品市場- キー プレイヤー
世界的なヘモグロビノパシー治療薬市場で動作する主要な選手は、ブリストル・マイアス・スクイブ・カンパニー、グリコメディック株式会社、フィザー株式会社、アンセラ・ファーマ株式会社、エリ・リリーおよびカンパニー、マスト・セラピューティクス、第一三協株式会社、ノヴェリシスインターナショナルAG、ブルーバード・バイオ株式会社、ヘマQuest Pharmaceuticals Inc.、エマウス・メディカル株式会社、バクスター・インターナショナル株式会社、プロロン・医薬品、Medurapeutics、Inc.、Inc.、Inc.、Inc.、Inc.、Inc.、Inc.
*定義: ヘモグロビノパシーはヘモグロビンの構造の異常を伴う遺伝的血液障害のグループです。 これらの障害は、病気の細胞疾患(SCD)と血糖の両方を含みます。 条件の一般的な症状は、重度の痛み、呼吸の不足、拡大脾臓、および子供の成長の問題を含みます。 構造ヘモグロビンの変形にリンクされているヘモグロビノパシーの他のタイプは、HbS、HbE、およびHbCです。 ヘモグロビノパシーの非常に可変的な臨床症状は、軽度の低血症から適度な血液学的疾患から重度の寿命、多臓器関与を伴う輸血依存性貧血までの範囲です。 ヘモグロビノパシーの症状を治療する薬には、鎮痛剤、抗生物質、ACE阻害剤、およびヒドロキシ尿薬が含まれます。 国立研究開発法人バイオテクノロジー情報センターのデータによると、現在、患者の90%以上が成人期を存続しています。 最適に扱われた患者は50から60年の写し出された寿命を持っています。
著者について
Ghanshyam Shrivastava - 経営コンサルティングとリサーチの分野で 20 年以上の経験を持つ Ghanshyam Shrivastava は、プリンシパル コンサルタントとして、生物製剤とバイオシミラーに関する幅広い専門知識を持っています。彼の主な専門知識は、市場参入と拡大戦略、競合情報、さまざまな治療カテゴリと API に使用されるさまざまな医薬品の多様なポートフォリオにわたる戦略的変革などの分野にあります。彼は、クライアントが直面する主要な課題を特定し、戦略的意思決定能力を強化するための堅牢なソリューションを提供することに優れています。彼の市場に関する包括的な理解は、リサーチ レポートとビジネス上の意思決定に貴重な貢献をします。
Ghanshyam は、業界カンファレンスで人気の高い講演者であり、製薬業界に関するさまざまな出版物に寄稿しています。
独占トレンドレポートで戦略を変革:
よくある質問


