米国のトランスサイレチンアミロイドーシス治療市場 規模と傾向
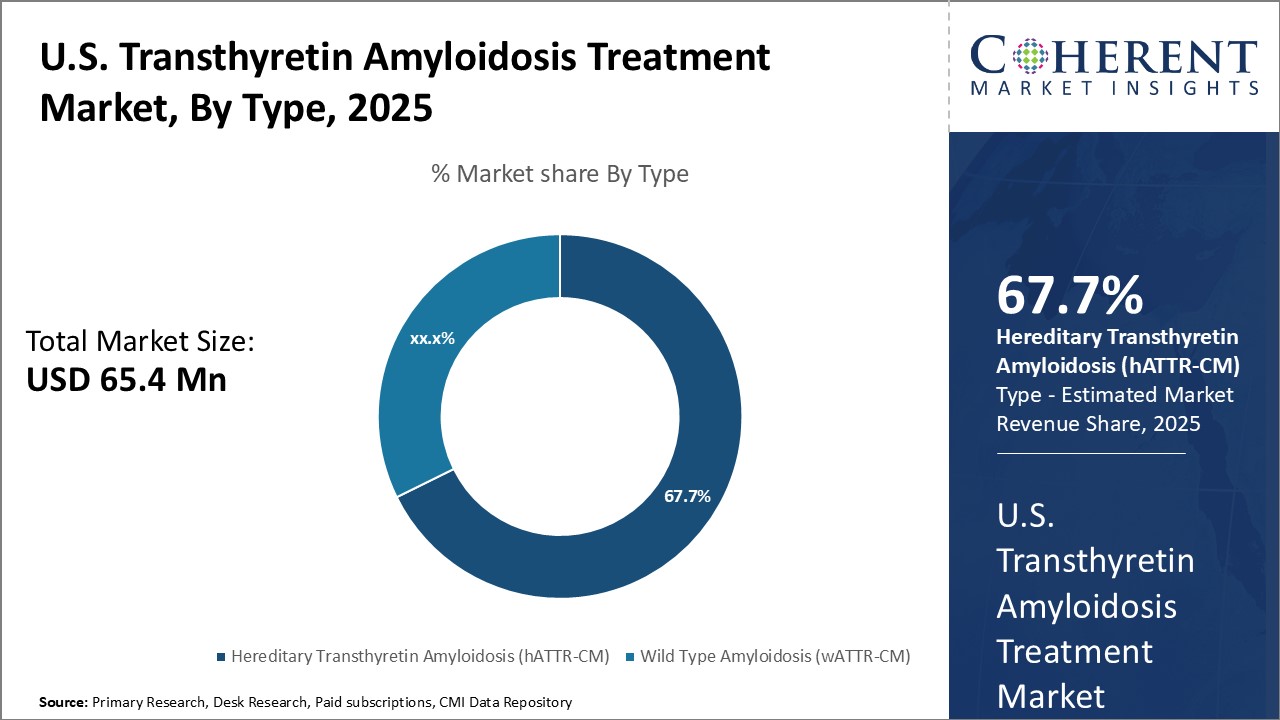
米国のtransthyretinのamyloidosisの処置の市場は評価されると推定されます 2025年のUSD 65.4 Mn そして到達する予定 米ドル 124.4 によって Mn 2032、混合物の年次成長率を展示する 2025年から2032年にかけて9.6%のCAGR。
業界を形成する市場の動向を知る: サンプルコピーをリクエストする
製薬会社と臨床試験のための研究機関間の高度化されたコラボレーションとともに、革新的な治療を目指した研究開発の努力を増加させ、トランスチレンアミラードーシス治療の需要を高めることが重要である。 また、非営利団体や支援団体が主導する意識への取り組みは、市場成長を推進する見込みです。 しかし、承認された薬の希少性や治療に伴う高コストなどの課題は、今後数年間でこの成長軌跡を妨げる可能性があります。
2025-02-07 09:20:21 更新
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
種類別インサイト - 野生型アミロドーシス(wATTR-CM)の遺伝的要因駆動需要
種別では、野生型アミロドーシス(wATTR-CM)のセグメントは、認知度や診断度が向上し、2025年に最高水準の市場シェアに貢献することが予想されます。 トランスチレンアミロイド症に関する意識が大幅に増加しました。, 改善された診断速度につながる. ヘルスケアの専門家とWATTR-CMに関連付けられている症状とリスクに関する公衆の理解を強化し、早期の診断と治療の開始を容易にします。
医薬品によるインサイト タイプ - ノベル薬物承認は、タファミディスセグメントの成長を促進します
薬の種類に関しては、tafamidis セグメントは 2025 年に 39.8% の最高の市場シェアに貢献することが推定され、最初の FDA が hATTR のアミロイド症の治療. その経口投与は、患者のコンプライアンスを強化します。, 臨床的証拠は、神経機能の安定化と死亡率の低下を示しています. 2030年までの特許保護により、市場位置をさらに確保し、中でも迅速な採用を奨励 ヘルスケア プロバイダー。
ディストリビューションチャネルによる洞察 – 病院の専門知識は、病院薬局を介して分布を駆動します
分配チャネルの面では、病院の薬局のセグメントは、トランスチレンアミラードーシスの複雑な症例を管理するために病院の専門知識に起因する48.7%の最高市場シェアに貢献することが期待されています。 これらの専門センターは、学際的なチームによる包括的なケアを提供し、統合された診断と治療オプションを促進します。 病気の悪化の患者様ケアの必要性は更に病院の薬剤師による調達を統合し、彼らの市場の位置を高めます。
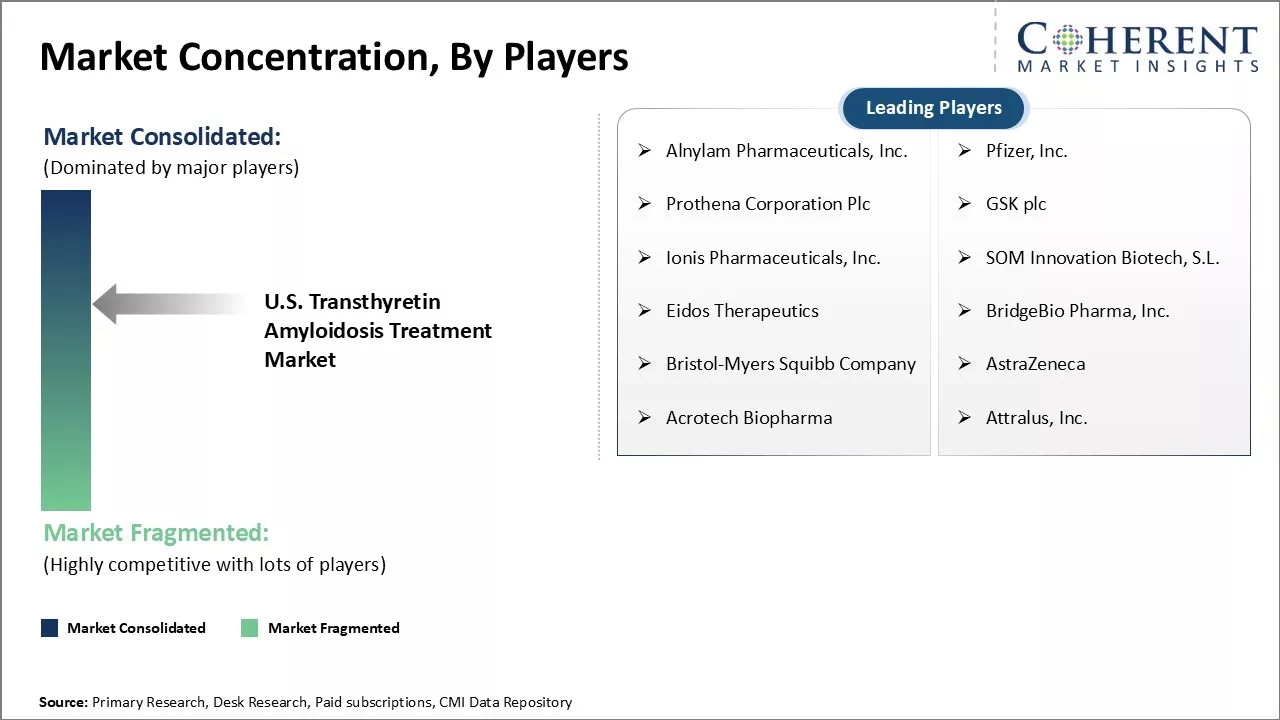
市場集中と競争環境
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
米国のTransthyretinのAmyloidosisの処置の市場 プレイヤーによって続く上の戦略
- 米国トランスチレン・アミロドーシス治療業界に選手を設立し、R&Dで新しい医薬品や治療を革新する。 たとえば、Pfizer, Inc.などの企業は、トランスチレン・アミラードーシスなどの希少疾患の新しい治療オプションを開発するために、R&D活動に毎年8億米ドル以上投資しています。
- 中堅企業は、より費用対効果の高い一般的な特許薬のバージョンを提供することで競争します。 例えば、大手ブランド名が知的財産権の保護を失うと、いくつかの企業が手頃な価格のバイオシミラーを起動します。 また、受託製造機関や医療機器メーカーと連携し、より低いアウトレイで生産能力を拡充します。
- 市場における小規模なプレーヤーは、ニッチ領域とハード・ツー・トリート患者サブグループに焦点を当てています。 いくつかのターゲット特定の遺伝子変異または専門的薬物による疾患の段階 サービスお問い合わせ 競争を維持するために、このような企業は、個別化医療や遠隔監視のためのテレヘルスのための3D印刷などの新しい技術を活用します。
米国トランスチレンアミラードーシス治療市場における新興スタートアップ
- 最先端技術を用いた革新的なソリューションを開発しています。 Anthropicのような他の人は、病気の進行と治療応答の自宅モニタリングのためのモバイルヘルスアプリと統合スマートバイオセンサーの開発に従事しています。 このような技術は、診断と治療の風景を変換する可能性があります。
- サステナビリティは、多くのスタートアップにとって重要なポイントです。 BioCellectionのような会社は単一の使用の医学プロダクトのための農業の無駄を使用して従来のプラスチックに持続可能な選択肢で働いています。 緑の化学的アプローチは、材料処分に関する懸念に対処することができます。
- 多くのスタートアップは、ニッチの患者グループにサービスを提供するギャップを特定し、ニーズに対処します。 専門的オルファン医薬品開発プログラムによるオーファン表示に重点を置いています。 他はカスタマイズされた療法を進めるために研究の組織との戦略的なパートナーシップを形作ります。
米国のトランスサイレチンアミロイドーシス治療市場 業界ニュース
- 2019年10月9日 アルニラム医薬品株式会社, RNAiの治療会社, 米国にサプリメントニュードラッグアプリケーション(SNDA)の提出を発表しました。. 食品医薬品局(FDA) vutrisiran, 調査RNAi治療は、心臓血管症(ATTR-CM)でATTRアミラードーシスを治療することを目的とした. AMVUTTRAの一般的な名前であるVutrisiranは、成人の遺伝性ATTRアミラードーシスの多重症を治療するために既にFDA承認されています。
- 2024年2月5日、米国食品医薬品局(FDA)が新薬申請(NDA)を承認し、ATTRアミロイド症(ATTR-CM)の調査治療を受けました。 このアプリケーションは ATTRibute-CM 試験から正の結果に基づいています。
- 2023年3月 アストラゼネカ、グローバルバイオ医薬品会社、NEURO-TTRansform Phase III の検査結果を発表し、遺伝的トランスチレン媒介陽性アロイドポリネロパシー(ATTRv-PN)の患者を関与させました。 試験は、エプロンテルセンが首尾のエンドポイントを66週間以上満たしたことを示しています。
アナリストからのキーテイクアウト
病気の増大率は、効果的な治療オプションに対する意識と要求を高めるため、主要な成長ドライバーであることが期待されます。 さらに、遺伝的および野生型ATTRアミロイド症に対する最近の薬物承認は、重要な新しい治療法を患者に提供する。
さらに、遺伝的および野生型ATTRアミロイド症に対する最近の薬物承認は、重要な新しい治療法を患者に提供する。 これにより、医師の治療選択肢を拡大し、患者プールを拡張しました。
高い薬剤価格はすべての患者が高価な薬物のための十分な保険の適用範囲を持っているので市場の拡大のための抑制残ります。 これは、その採用を制限することができます。 それにもかかわらず、製薬会社はアクセスを改善するために忍耐強い支持プログラムを提供するために努力しています。
市場レポートの範囲
U.S. TransthyretinのAmyloidosisの処置の市場レポートの適用範囲
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 65.4 Mn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 9.6% | 2032年 価値の投射: | 米ドル 124.4 Mn |
| カバーされる区分: |
| ||
| 対象会社: | Alnylam Pharmaceuticals, Inc., Pfizer, Inc., Prothena Corporation Plc, GSK plc, Ionis Pharmaceuticals, Inc., SOM Innovation Biotech, S.L., Eidos Therapeutics, BridgeBio Pharma, Inc., ブリストル・マイアス・スクイブ・カンパニー, AstraZeneca, Acrotech Biopharma, Attralus, Inc. | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータで検証されたマクロとミクロを明らかにする, レポートにすぐにアクセス
市場の動向
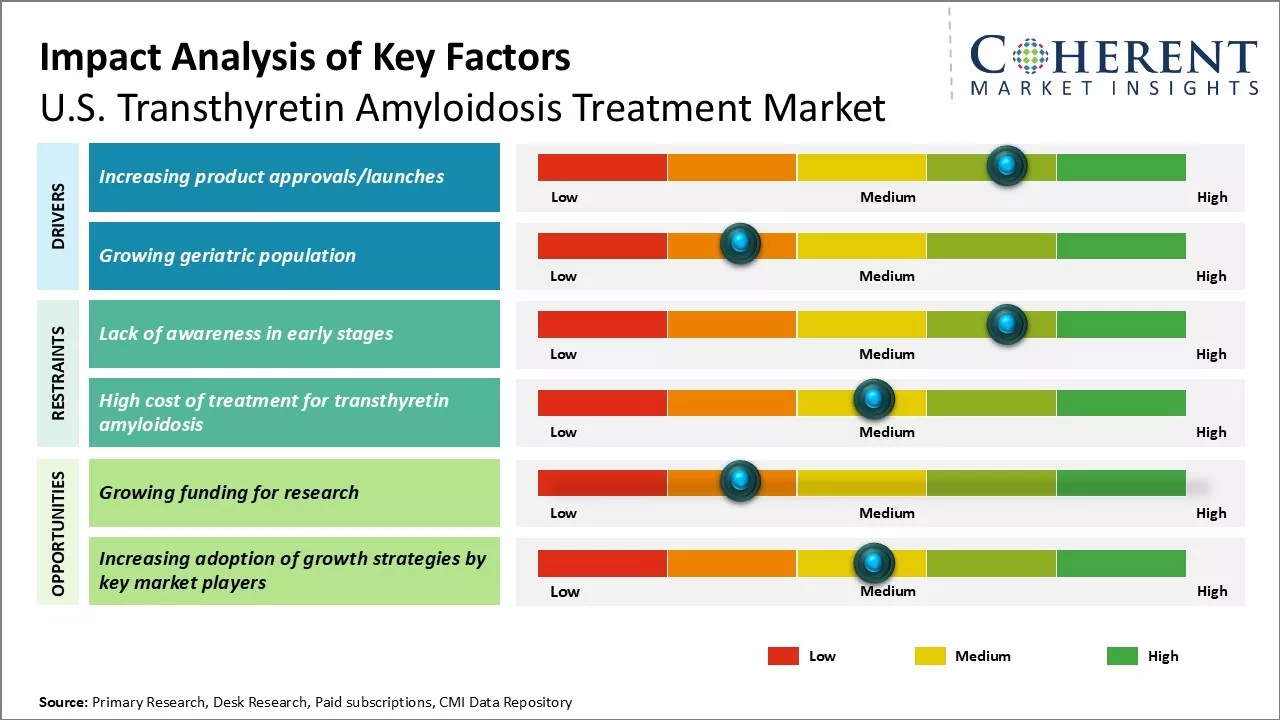
市場ドライバ - 製品の承認/リリースを増加させる
トランスチレンアミロイド症の高まりに伴い、製薬会社は新規治療の開発に取り組んでいます。 2023年12月、Ionis Pharmaceuticals、Inc.、製薬会社、およびAstraZenecaは、米国食品医薬品局(FDA)がIonisおよびAstraZenecaのWAINUA(エプロロンテルセン)を承認し、成人における遺伝的トランスチレン媒介症の治療のために、一般にhATTR-PNまたはAT-TRV.PNと呼ばれていると発表しました。
市場チャレンジ - 初期段階における意識の欠如
米国のtransthyretinのアミラードーシスの処置の企業の重要な挑戦の1つは早い段階の病気についての意識の欠如です。 トランスチレンアミロイド症は、しばしば漠然とした症状による初期段階で診断され、治療の遅延と不可逆的な損傷につながる。 医療従事者と早期の標識に関する公衆の意識を高めることは、タイムリーな介入のために不可欠です。 教育的イニシアチブとスクリーニングプログラムの実施は、リスクのある人口の早期発見と健康的結果を大幅に向上させることができます。
市場機会 - 研究のための成長資金
研究のための成長の資金は、米国トランスチレンアミロドーシス治療業界で重要な機会を提示します. 政府や民間組織からの財務支援の増加は、病気の病因の理解を高め、高度な診断と治療を開発することを目指しています。 この投資は、すでに米国食品医薬品局の承認に導かれています。複数の病気修飾薬の, パイプラインの有望な候補は、治療の有効性と患者の結果を改善することが期待されています.
市場セグメンテーション
- 種類別インサイト(Revenue、USD Mn、2020 - 2032)
- 遺伝性トランスチレンアミラードーシス(hATTR-CM)
- ワイルドタイプ アミラードーシス(wATTR-CM)
- によって 薬物型インサイト(Revenue、USD Mn、2020 - 2032)
- タファミディス
- Diflunisalの特長
- ログイン
- パティオ
- トルカボン
- その他
- によって 流通チャネルの洞察(Revenue、USD Mn、2020 - 2032)
- 病院薬局
- 小売薬局
- オンライン薬局
- キープレーヤーの洞察
- アルニラム医薬品株式会社
- 株式会社Pfizer
- 株式会社プロテナ Plc
- GSK 液晶
- 株式会社イオニス製薬
- SOMイノベーションバイオテクノロジー、S.L.
- Eidos 治療薬
- BridgeBioファーマ株式会社
- ブリストル・マイアーズ・スクイブ・カンパニー
- アストラゼネカ
- Acrotechバイオ医薬品
- 株式会社アトララス
著者について
Ghanshyam Shrivastava - 経営コンサルティングとリサーチの分野で 20 年以上の経験を持つ Ghanshyam Shrivastava は、プリンシパル コンサルタントとして、生物製剤とバイオシミラーに関する幅広い専門知識を持っています。彼の主な専門知識は、市場参入と拡大戦略、競合情報、さまざまな治療カテゴリと API に使用されるさまざまな医薬品の多様なポートフォリオにわたる戦略的変革などの分野にあります。彼は、クライアントが直面する主要な課題を特定し、戦略的意思決定能力を強化するための堅牢なソリューションを提供することに優れています。彼の市場に関する包括的な理解は、リサーチ レポートとビジネス上の意思決定に貴重な貢献をします。
Ghanshyam は、業界カンファレンスで人気の高い講演者であり、製薬業界に関するさまざまな出版物に寄稿しています。
独占トレンドレポートで戦略を変革:
よくある質問


