第一次性胆硬変医薬品市場規模と予測 – 2025 – 2032
世界の第一次胆嚢胞症の薬剤 市場規模は2025年に1,35億米ドルで評価され、2032年までに2,12億米ドルに達する見込みで、2025年から2032年までに6.3%の連結年間成長率(CAGR)を占めています。
プロフィール
PBC医薬品には、慢性自己免疫の管理を目的とした治療製剤が含まれます 肝疾患 病気の進行を遅らせ、胆汁酸の蓄積を減らすことによって。 主要なプロダクト タイプは尿素酸(UDCA)、farnesoid Xの受容器(FXR)のような胆汁酸のアナログおよびPPARのアゴニストおよび免疫調節器のような新興の処置を含んでいます。 これらの薬は経口投与形態で利用可能であり、肝機能と生活の忍耐強い品質を向上させることに重点を置いています。
キーテイクアウト
ursodeoxycholic 酸の区分は 53.4% のシェアと薬剤のクラスカテゴリを、十分に確立された効力および許容のプロフィールによってbuoyed分けます。
臨床進歩による有望な機会を提示し、肥満酸の区分は急速に成長しています。
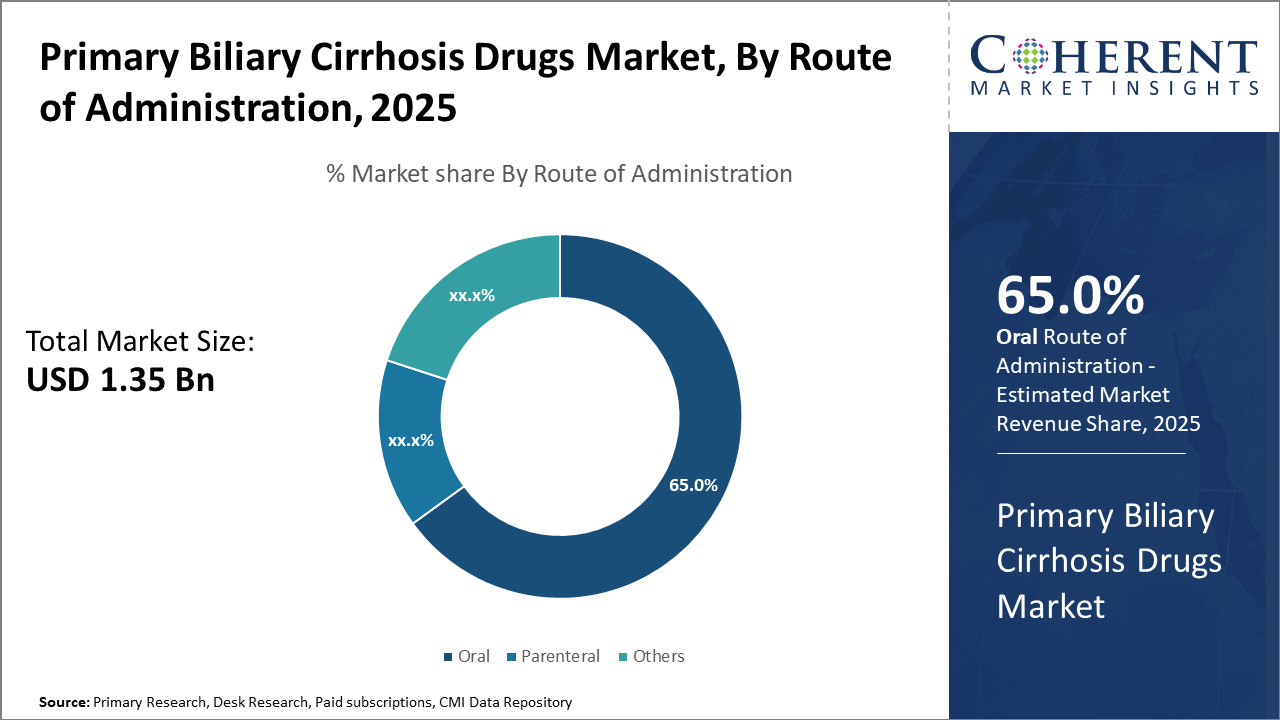
経口投与は、65%で配達の経路をリードし、患者の利便性とより高いコンプライアンスに起因します。 特定の場合のためのニッチなアプリケーションを維持するためのペアレントルート。
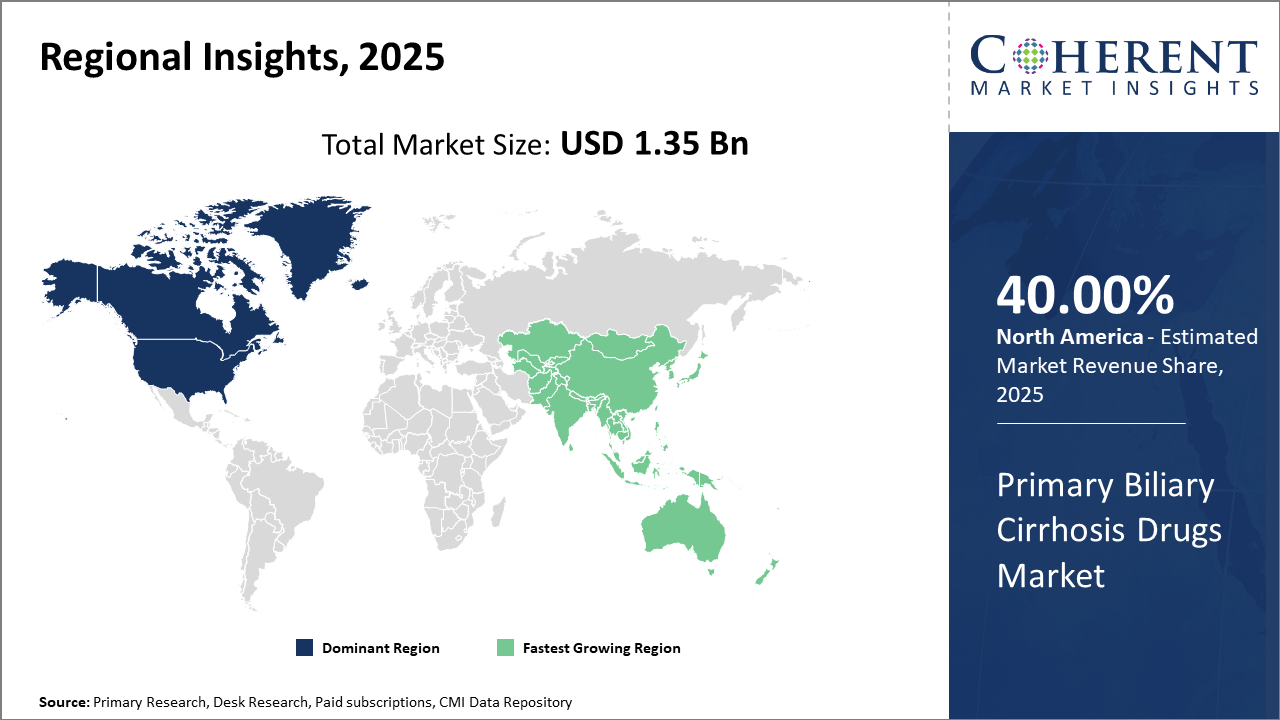
北米は、先進的な医療インフラと償還フレームワークによって駆動され、市場シェアの40%以上を占める主要な地域市場として継続しています。
アジアパシフィックは、患者の拠点を拡大し、ヘルスケアのアクセシビリティを向上させることで、8%を超えるCAGRを展示し、急速に成長する地域を表しています。
第一次胆嚢胞症は市場区分の分析に薬剤を入れます
このレポートの詳細, サンプル コピーをリクエスト
第一次胆嚢胞症は薬剤のクラスによって市場の洞察、薬剤を薬剤で薬剤します
ウルソデオキシコリン酸は、病気の進行と好ましい許容プロファイルを遅らせることで、その実証済みの有効性を支持し、市場シェアを支配します。 肥満酸のサブセグメントは、最も急速に成長しているクラスを表し、耐火性PBC症例の規制当局の承認から恩恵を受けており、2024年の処方傾向を増加させることで実証されたバイオ化学的反応。 フィブラッツは、炎症経路を標的するアドジャンクの利点を提供しますが、限られた浸透を持っています。 免疫抑制剤は、目立たないが、コンビネーション療法でトラクションを獲得しています。
第一次胆嚢胞症は管理のルートによって市場の洞察を、薬剤で薬剤を入れます
管理のルートに関しては、市場は経口、ペアラル、およびその他のルートを迂回し、実質的に支配します。 有用性、費用効果が大きい、および改善された忍耐強い付着力は口頭公式のunderscoreに彼らの市場の優位に関連付けました。 育児ルートは、専門的ケア設定と高度な肝疾患合併症の患者のために限られています。 経口バイオアベイラビリティを高め、副作用を減らすことを目的とした新興製剤は、このセグメント内で成長を促進します。
第一次胆嚢胞症は配分チャネルによって市場の洞察を、薬剤にします
病院薬局は医学の監督および管理された分配を要求するPBCの処置の慢性的な性質による支配します。 小売薬局は、主にメンテナンス療法と補充の要求に食料調達しますが、規制と処方の制約に直面しています。 オンライン薬局は、高度成長を目撃しています, 特に先進のテレメディシンインフラを持つ地域で, 改善された薬物のアクセシビリティを提供します. 特別な薬局のような追加のチャネルは、希少で先進的な治療に焦点を当て、全体的な市場範囲を増強し、患者中心のケアをサポートする。
第一次性胆嚢炎薬市場 トレンド
第一次胆嚢胞症薬市場は、その軌跡を形づける3つの重要な傾向によって特徴付けられます。
第一に、バイオマーカー主導のセラピスの採用の増加は、治療のパーソナライゼーションを高め、優れた臨床結果を提供し、プレミアム価格設定戦略を支援します。
例えば、2024年からの研究では、治療が標準的なプロトコルと調整されると、病気の進行率が12%低下する。
第二に、ライフスタイルや環境要因による自己免疫肝障害の上昇可能性は、世界的な効果的なPBC治療薬の需要の高まりを強調しています。
第三に、デジタルヘルス技術は、特に開発市場でより良い患者の遵守と監視を促進し、薬物の有効性と寿命の忍耐強い品質を向上させます。
第一次性胆嚢胞症は地理によって市場の洞察を、薬剤にします
このレポートの詳細, サンプル コピーをリクエスト
北アメリカの第一次性胆嚢胞症は市場分析および傾向を薬剤で造ります
北米では、第一次胆嚢胞薬の市場での優位性は、確立された医療インフラ、堅牢な払い戻し方針、および高度な診断機能から成ります。 地域は、業界全体のシェアに40%以上貢献しています。 AbbVieやIntercept Pharmaceuticalsなどの主要なプレーヤーは、米国内の臨床試験および製品起動イニシアティブに大きく投資し、市場リーダーシップを強化します。
アジア・パシフィック・プライマリ・ビリーリシス医薬品市場分析とトレンド
アジアパシフィックは、PBC医薬品市場で最も速い成長を遂げ、CAGRは8%を超える。 増加するヘルスケアの支出、強化された規制枠組み、および成長する患者意識などの要因は大幅に貢献します。 中国やインドなどのエコノミエの新興国は、医薬品の輸入量の増加と現地の医薬品投資を目撃し、非met臨床ニーズに対応します。
主要な国のための第一次性胆嚢胞症の薬剤の市場見通し
アメリカ 第一次胆嚢胞症は市場分析および傾向を薬剤にします
米国の市場は、初期病態検出能力と強力な受給者サポートのために、主に第一次胆性肝硬変薬のための重要な成長エンジンとして立っています。 2024年、前方率は9%増加し、同時に10%以上で薬の販売上昇を運転する。 インターセプト医薬品などの戦略的患者支援プログラムおよび臨床革新の企業は、二重桁の収益成長を報告しました。 さらに、新免疫調節剤のFDA承認は、国の市場ダイナミズムを持続させました。
日本一次胆嚢胞症薬市場分析と傾向
日本市場は、自己免疫肝疾患に対処する政府主導の医療政策によって強化され、PBC療法のための有利な償還条件を作り出しています。 この国は、2024年までに総薬収入の約30%を占める革新的な治療で、臨床研究投資のサージを見てきました。 製薬企業は、地域ポートフォリオを積極的に拡大し、アジア・パシフィック・マーケットのシェアを増加させ、堅牢な事業成長に貢献しています。
アナリストオピニオン
需要側の指標は、第一次胆性肝硬変症に対する患者の診断率が2023年から2024年にかけて約8.2%上昇すると明らかにし、治療開始とその結果の市場収益が大幅に増加します。 たとえば、米国は、2024年に報告された新しいPBCケースで10%上昇を見ました。これは直接薬物の採用率を高めました。
ウルソデオキシコリン酸を含む主要な治療用化合物の生産能力は、2024年にヨーロッパと北アメリカの主要製薬ハブで12%拡大し、薬の可用性を高め、安定した市場成長を支援します。
PBC医薬品市場の価格推移は、平均治療費が2023年から2025年にかけて4.5%上昇し、新規、特許取得済みの薬処方の導入を反映し、患者の手頃な価格を維持しています。
アジアパシフィックの革新的なPBC治療薬の輸入量は、ヘルスケアインフラと規制当局の承認を増加させることで、15%を占めています。 この傾向は、新興国が消費成長にますます貢献する市場ダイナミクスをシフトすることを示しています。
市場規模
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2025年 | 2025年の市場規模: | 1億米ドル |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 6.3% | 2032年 価値の投射: | 米ドル 2.12 億 |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | AbbVie株式会社、武田薬品工業株式会社、インターセプト医薬品株式会社、ジラドサイエンス株式会社、ノバルティスAG、Pfizer Inc.、Sanofi S.A、メルク株式会社、三菱田辺ファーマ株式会社、シプラ株式会社、サン・ファーマ株式会社、Dr. Reddy’s Laboratories Ltd. | ||
| 成長の運転者: |
| ||
75 以上のパラメータで検証されたマクロとミクロを明らかにする, レポートにすぐにアクセス
第一次性胆嚢胞症は市場成長因子を薬剤にします
自己免疫肝疾患の世界的な増加の優先順位は、主要な成長ドライバーを維持します。, によって証明 7.1% 2023 と 2025 の間の診断 PBC 症例の増加. 薬剤の公式、特に第2世代の胆汁酸のアナログの開発で進歩し、高度の採用率を運転する治療上の効力を高めて下さい。 北米および欧州における慢性肝疾患の緩和スキームを提供する政府の取り組みの増加は、患者の財政的負担を大幅に軽減し、長期的治療の遵守を奨励しています。 さらに、PBCのコンビネーション療法を評価する臨床試験の拡大は、多様化する治療の風景を創り出すことで、革新的な医薬品の発売を触媒化し、市場成長を刺激することが期待されています。
第一次性胆嚢症薬市場開発
2024年8月、米国食品医薬品局(FDA)は、PBCの治療のためにseladelpar(ブランド名:Livdelzi)を承認しました。 この承認により、 尿素酸(UDCA) を UDCA に適切に反応しない、または UDCA を許容できない人のためのモノセラピーとして使用することができる。 Seladelpar は、PBC 患者における pruritus および interleukin-31 レベルを削減する有効性を実証しました。
2024年6月10日 イプセン 米国食品医薬品局(FDA)が承認を加速したと発表 お問い合わせ Iqirvo®(elafibranor) プライマリ胆管支炎の治療のための80 mg錠(PBC))お問い合わせ 治療は、ウルソデオキシコール酸(UDCA)と組み合わせて使用するために承認されます) UDCAへの不十分な応答を示す大人、またはUDCAを許容できない患者のためのモノセラピーお問い合わせ 米国における有資格患者は、直ちにIqirvoを処方することができる。
キープレイヤー
市場をリードする企業
株式会社AbbVie
武田薬品工業株式会社
インターセプト医薬品 代表取締役
ジャイラドサイエンス株式会社
ノバルティスAG
サノフィ S.A.
マーク&株式会社
三菱田辺ファーマ株式会社
株式会社シプラ
サン製薬工業株式会社
株式会社レッドディの研究所
大手企業が2024年に堅牢な市場成長戦略を採用しました。 例えば、Intercept Pharmaceuticalsは、北米の患者アクセスプログラムを正常に導入し、11%のPBC薬の市場浸透を増加させました。 アッブ バイオテクノロジー社との戦略的コラボレーションにより、次世代の免疫抑制剤を開発し、R&Dの効率性を9%向上し、希少な自己免疫肝疾患に焦点を当てた。 武田薬品は、アジア太平洋地域におけるライセンス契約を増強し、新興地域における市場参入率が13%向上しました。
第一次性胆嚢炎薬市場将来の見通し
将来のPBC薬の開発は、胆汁酸合成、炎症を調節するために設計されたマルチターゲットと組み合わせ療法を強調し、 フィブロシス 同時に。 選択的PPAR変調器、FGF19アナログ、免疫ターゲティング薬などのノベル剤は、開発中、より優れた耐性と有効性を約束します。 遺伝的およびバイオマーカーベースの治療選択を含む個人化された薬アプローチは、治療の最適化を導きます。 持続的な解放の公式のような薬剤の配達革新は、再生レバー療法に研究が高度の病気の段階の薬学の処置を補うことができる間、順守を高めます。
第一次性胆嚢症薬市場履歴分析
第一次予選 Cirrhosisの薬剤の開発は歴史的にursodeoxycholicの酸(UDCA)のような胆汁のアナログによって症状管理に焦点を合わせ、レバー機能を改善し、病気の進行を遅らせました。 2010年代は、標的療法へのシフトをマークし、肥満酸の導入、より効果的に病気のメカニズムに対処するFXRアゴニスト。 PPARアゴニストと免疫調節器の探査につながったサブシーケント研究は、治療オプションを拡大します。 製剤は、治療耐性症例に対処し始めている間、配合療法は、生理性および患者の遵守を改善しました。
ソース
第一次研究インタビュー:
肝専門医
消化器科医
臨床薬理学
バイオ医薬品研究者
データベース:
NCBI 臨床試験
お問い合わせ 医薬品データベース
雑誌:
医薬品技術
ファーマタイムズ
バイオファーマ ダイビング
創薬・開発
ジャーナル:
ヘパトロジー
ライバーインターナショナル
ヘパトロジージャーナル
臨床薬理学および治療薬
新聞:
経済時代(Pharma)
ガーディアン(健康)
ウォールストリートジャーナル(ヘルスケア)
ビジネススタンダード(医薬品)
協会:
肝疾患研究協会(AASLD)
肝臓の研究のための欧州連合(EASL)
国際交流基金
著者について
Vipul Patil は、製薬業界で 6 年間の経験を積んだダイナミックな経営コンサルタントです。分析力と戦略的洞察力に優れた Vipul は、製薬会社と提携して業務効率の向上、より広範な拡大、収益性の高い市場での流通の複雑さへの対応に成功しています。
独占トレンドレポートで戦略を変革:
よくある質問


