ゲノムがん検査市場は2025年に22.00ドルで評価され、USD 64.85に達すると予想される 2032年にBn、2025年から2032年にかけて16.7%の化合物年間成長率(CAGR)を展示。
ゲノムがん検査は、ゲノムデータを使用してさまざまなタイプの診断および治療を行う医療試験の一種です。 がんばりお問い合わせ 患者のゲノムデータのシーケンシングと解析は、特定の変異や変化を識別し、がんの発症または関与する可能性があります。 このタイプの検査は、医師が患者の特定のタイプの癌に対して最も効果的な治療計画を決定するのを助けることができます。 また、遺伝子構造に基づいて特定の種類の癌を発症する患者のリスクを予測するために使用することができます。
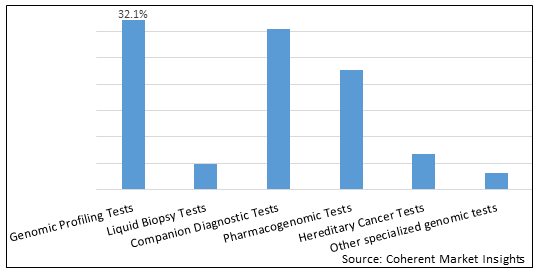
ゲノムがん検査市場は、試験の種類、がんの種類、技術、エンドユーザー、バイオマーカーの種類、サービスプロバイダ、アプリケーション、テスト設定、地域別に分けられます。 試験の種類によって、市場はゲノムプロファイリングテスト、液体バイオプシーテスト、コンパニオン診断テスト、薬理学テスト、遺伝性がん検査、およびその他の専門性ゲノムテストに分けられます。 ゲノムプロファイリングテストは、世界的ながんの罹患率が増加しているため、最大の市場シェアのためのアカウントをセグメント化します。
グローバルゲノムがん検査市場 地域的インサイト:
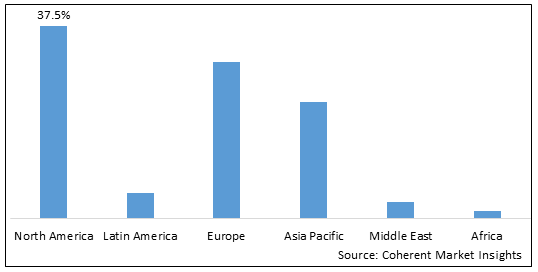
- 北アメリカ ゲノムがん検査市場におけるリーダーとして誕生し、健康に配慮した医療インフラを活用し、精密医療に関する高い関心を寄せています。 米国、特に、臨床的慣行におけるゲノムテストの重要な進歩と広範な採用を目撃しました。 2025年に37.5%のシェアで市場を支配する見込みです。 地域の成長は、がんの高病変、ゲノムがん検査技術への投資の増加、多数の主要な選手の存在など要因によって燃料を供給されます。
- ヨーロッパ また、ゲノムがん検査を含む精密薬のイニシアティブにも積極的に投資しています。 英国、ドイツ、フランスなどの国では、ゲノムテストを定期臨床ケアに組み込むことに著しい進歩を遂げています。 2025年、欧州は30.4%のシェアで2番目に大きい市場であることを期待しています。 地域の成長は、パーソナライズされたがんのケア、政府のイニシアチブの増加、重要な選手の数の存在に対する増加の需要によって駆動されます。
- インフォメーション アジアパシフィック 地域は、ゲノムがん検査市場で大きな成長の可能性を示しています。 中国、日本、韓国などの国は、ゲノム研究と技術に投資し、腫瘍学におけるゲノム試験の採用率を高めています。 アジアパシフィックは、予測期間中に最も急速に成長している市場であり、22.6%のCAGRを投影した。 地域における成長を促進する要因は、がんの増大率を含み、ゲノムがん検査技術への投資の増加、ゲノムがん検査のメリットに対する意識の高まりなどです。
プロフィール 1.グローバルゲノムがん検査市場シェア(%)、地域別、2025
このレポートの詳細, サンプル コピーをリクエスト
グローバルゲノムがん検査市場ドライバー:
- がんの増大 インシデント: がんのグローバル化は、ゲノムがん検査市場にとって重要なドライバーです。 がん症例の数が増え続けるにつれて、腫瘍の分子特性を理解し、パーソナライズされた治療戦略を導き出すために、正確で包括的なゲノム検査の必要性が高まっています。 たとえば、2023年7月に世界保健機関(WHO)が公表したデータによると、2020年は、母乳がんと診断された女性は2億2億2千万人の死亡を突破しました。
- ゲノム技術の進歩: ゲノムシークエンシングや分析技術における技術開発 次世代シーケンシング(NGS)、 ゲノムの分野に革命をもたらしました。 これらの進歩は、よりアクセス可能で、費用効果が大きい、そして効率的に、臨床練習の採用を運転するゲノム癌のテストをしました。 たとえば、2022年3月には、米国ベースのバイオテクノロジー会社であるイルミナ社が、TruSight Oncology(TSO)の統合(EU)の立ち上げを発表しました。複数の腫瘍遺伝子とバイオマーカーを評価する単一のテストで、患者のがんの特定の分子プロファイルを明らかにします。 欧州で最初に開催するグローバル・ローンチにより、インビトロ診断(IVD)キットは、がん患者様に対し、大陸横断の精密医療の決定を促します。
- 行き方へ 個人化された薬: ゲノムがん検査は、パーソナライズド医薬品へのシフトにおいて重要な役割を果たしています。 医療従事者は、患者の腫瘍の遺伝的プロファイルに基づいて治療計画を調整し、よりターゲティングされ効果的な治療法につながることを可能にします。 パーソナライズされた医療アプローチの高まりは、ゲノムがん検査の需要を促進しています。
- 改善された処置 Outcomes: ゲノムがん検査では、治療結果を改善するための有望な結果が示されています。 腫瘍内の特定の遺伝的変化を識別することにより、医療提供者は、より効果的である可能性が高い標的療法を選択することができ、それによって患者の結果を高め、不要な治療や副作用を減らすことができます。
グローバルゲノムがん検査市場 機会:
- 拡大された臨床適用: ゲノムがん検査は、がん治療のさまざまな段階で既に使用されてきましたが、その臨床応用におけるさらなる拡大の機会があります。 がんのゲノム基礎の理解によって、治療の決定を導き、患者の成果を向上させることができる新しいバイオマーカーと遺伝的ターゲットを識別する可能性があります。 これらの追加の臨床アプリケーションを探索し、検証することで、ゲノムがん検査の新しいアベニューを開くことができます。
- ビッグデータと人工知能との統合: ゲノムがん検査は、ゲノムの膨大な量のデータを生成します。 このデータを高度な分析、ビッグデータ技術、人工知能(AI)アルゴリズムで統合することで、データ解釈を強化し、治療予測モデルを改善し、患者の戦略を最適化することができます。 AIと機械学習アルゴリズムを活用することで、より正確な行動可能な遺伝的変化の特定を可能にし、精密腫瘍学の開発を容易にすることができます。
- 液体の生物精神および非侵襲的なテスト: 血液サンプルの循環腫瘍DNA(ctDNA)および他のバイオマーカーを検出する非侵襲的な方法である液体生検は、ゲノムがん検査市場で重要な約束を保持しています。 それは従来のティッシュの生物多様性により少ない侵襲的な代わりを提供し、腫瘍の動的および処置の応答の実時間監視を可能にします。 液体生検技術のさらなる研究と技術の進歩は、そのユーティリティとアクセシビリティを拡大し、ゲノムがん検査の新しい機会を開くことができます。 また、予測期間における市場成長の推進が期待されている製品発売に焦点を当てた市場で動作する主要なプレーヤー。 たとえば、2023年5月、ラボコープは、先進的または転移性固形腫瘍を有する患者に対する標的治療選択を可能にする新しい液体生検検査であるLabcorpプラズマフォーカスを発売しました。 腫瘍細胞によって放出される細胞フリーDNA(cfDNA)を循環させ、腫瘍細胞のケアをより適切に管理し、個人化された治療計画を通じて患者のケアを管理することができます。
- 新興市場: 新興市場でのゲノムがん検査の機会は、特にがんの負担が高まり、医療インフラを成長させる地域にあります。 これらの領域は、ヘルスケアシステムを開発し、高度な診断へのアクセスを高めるため、ゲノムがん検査の採用が増加する可能性があります。 これらの市場に適した戦略とソリューションを開発することで、新たな成長機会を開放することができます。
ゲノムがん検査市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 22.00 Bn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 16.7%の | 2032年 価値の投射: | 米ドル 64.85 Bn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | 株式会社イルミナ(本社:東京都千代田区、代表取締役社長:樋口 宏、以下「当社」)、株式会社インビタエ、株式会社ネオゲノム研究所、株式会社ミリアド遺伝学、株式会社ゲノムヘルス、株式会社(本社:東京都千代田区、代表取締役社長:山口 宏、以下「当社」)、株式会社カーリスライフサイエンス、ArcherDX、株式会社(以下「Invitae」)、株式会社ガードラントヘルス、株式会社、株式会社インフォメリアド健康研究所、株式会社、株式会社、株式会社、株式会社、ゲノミノミノミックヘルス、株式会社(以下「バイオメディカルサイエンス」)、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、株式会社、 | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータで検証されたマクロとミクロを明らかにする, レポートにすぐにアクセス
グローバルゲノムがん検査市場 トレンド:
- 次世代シーケンシング(NGS):の採用拡大 次世代シーケンシングは、がん全ゲノムの迅速で費用対効果の高いシーケンシングを可能にすることで、ゲノムがん試験に革命をもたらしました。 NGSプラットフォームは、臨床設定でますます使用されています。これにより、腫瘍の包括的なプロファイリングと、実用的な遺伝的変化の特定が可能になります。 NGSの技術の採用は市場を運転する重要な傾向です。 また、規制機関による製品承認の増加は、予測期間にわたって市場成長を促進することが期待されます。 たとえば、2022年3月、サーモフィッシャーサイエンスは、ライフサイエンスソリューション、分析機器、専門診断、およびラボ製品およびバイオ医薬品サービスを提供し、CE-IVDマークのイオントレントゲネクスDx統合シーケンサー、自動化された次世代シーケンシング(NGS)プラットフォームを1日限りで実現しました。 臨床実験室の使用のために設計されていて、十分に検証されたシステムは1つの器械の診断テストそして臨床研究を両方実行することを可能にします。
- 精密医学のエンファシスの増加: 精密医学のアプローチは癌の心配の牽引を得、ゲノム癌のテストはこのパラダイムシフトで重要な役割を果たします。 生理学者およびヘルスケアプロバイダーは、各患者の腫瘍のユニークな遺伝的プロファイルに基づいて治療計画を調整するゲノム情報の価値を認識しています。 精密薬への傾向は、ゲノムがん検査の要求を運転しています。
- ゲノムデータを臨床意思決定に統合: ゲノムデータは臨床的意思決定プロセスにますます統合されています。 高度なバイオインフォマティクスツールとアルゴリズムは、大規模なゲノムデータを解釈し、分析するために採用され、医療専門家は、腫瘍の遺伝的特性に基づいて情報処理の決定を下すことを可能にします。 ゲノムデータを定期的な臨床練習に統合することは、市場で重要な傾向です。
- 液体の生検の上昇: 体液中の腫瘍由来の遺伝物質を検知する非侵襲的手法である液質バイオサイプは、ゲノムがん検査分野における有意性を高めています。 それは従来の組織の生物多様性に代わり、腫瘍の動的および処置の応答の実時間監視を可能にします。 液体生検は、がんの診断とモニタリングに革命をもたらし、その採用は市場で注目すべき傾向です。
グローバルゲノムがん検査市場の抑制:
- 高い費用: ゲノムがん検査は、次世代シーケンシング(NGS)などの先端技術を使用した場合、特に高価な検査が可能です。 テストに関連した高いコストは、患者やヘルスケアプロバイダーのアクセシビリティを制限し、広範な採用への重要な障壁をポーズすることができます。 コストの考慮事項は、特に限られた医療予算や不利な政策を持つ地域で市場成長を妨げることができます。 たとえば、米国癌協会、Inc.が公表したデータによると、腫瘍組織のゲノムテストには、特定の遺伝子や染色体の変化や、腫瘍パネルテストなど、複数の遺伝子の変化を同時に確認するためのテストが含まれています。 これらの試験は、US $ 300からUS $ 10,000までの費用で、ターゲット処理の価格は年10万USドル以上です。
カウンターバランス: 主要企業は、研究開発に投資し、より費用対効果の高いゲノムシーケンシング技術と分析ツールを作成する必要があります。
- 融資課題: ゲノムがん検査の払い戻し風景は複雑で変化します。 異なる国と医療システムは、ゲノムテストをカバーするための払い戻し方針と基準が異なる。 償還プロセスをナビゲートし、ゲノム試験の適切な払い戻しを得るには、ヘルスケアプロバイダーの不確実性を作成し、採用に対するインセンティブを減らすことができます。
- 限定臨床 証拠: ゲノムがん検査は約束を保っていますが、臨床的有用性を実証し、患者の成果への影響を実証する堅牢な臨床証拠の可用性は依然として進化しています。 大規模臨床試験および現実的な証拠がゲノムテストの有効性と価値を検証するための必要性は、ヘルスケアプロバイダが実質的な証拠なしで定期的な臨床練習にそれを統合することについて注意すべきかもしれないので、市場成長と採用を遅くすることができます。
最近の開発:
新製品の発売/承認:
- 2023年7月 ガードラントヘルス株式会社日本保健省、労働福祉省(MHLW)の全国的償還承認を受け、2023年7月24日(火)、2023年7月24日(日)に、先進的または転移固形腫瘍癌を有する患者に対して、Guardant360 CDx液体生検試験(CGP)が実施されると発表した。 本アナウンスは、2022年3月 MHLW による Guardant360 CDx 試験の規制承認書に従います。
- 2023年10月、Arima Genomics、米国バイオテクノロジー会社、Protean BioDiagnostics、バイオテクノロジー会社、ジョイントベンチャー、Aventa Genomicsを結成し、新会社がAventa FusionPlus、遺伝子融合、トランスロケーション、および361遺伝子をホルムリンフィング、パラフィン組み込み腫瘍組織から361遺伝子に及ぼす再構成テストを呼び出す。
- 2023年6月、診断ソリューションを開発、製造、販売するDevyserは、臨床研究所に2つの新製品、Devyser LynchFAPおよびDevyser BRCA PALB2の発売を発表しました。 これらのキットは、リンチ症候群、および母乳および卵巣癌に関与するなど、増加したがんリスクに関連する遺伝子の効率的、標的、および自信のある分析を提供します。
買収とパートナーシップ:
- 2022年1月株式会社イルミナ 早期がん検出試験で有力者であるGrailを買収したことを発表しました。 この買収は、ゲノムプロファイリングを用いたマルチカンサー早期検出の最前線でイルミナとGrailを配置します。 組み合わせたエンティティティティティティティティティティティティティティティは、世界中のそのような救命テストの商用可用性を加速することを目指しています。
- 2022年1月、分子診断会社であるExact Sciences Corp.は、先進がん診断ポートフォリオを補完し、遺伝がん検査(HCT)への入試を支援するために、予防薬、遺伝子検査室を買収したことを発表しました。 予防遺伝学は、HCTの可用性を加速するために必要な臨床ラボ、専門知識、基礎技術を提供し、より多くの患者ががんや他の病気の細菌リスクを知っています。
- 2022年12月、ゲノムおよび診断テストのリーダーであるPrenetics Global Limitedは、香港、台湾、日本、シンガポール、タイ、英国におけるオペレーションにおける精密腫瘍学に特化したアジアベースのゲノムス・ホールディングス株式会社のACT Genomics Holdings Company Limitedの過半数の株式を取得しました。
プロフィール 2. 世界ゲノムがん検査市場シェア(%)、テストタイプ、2025
このレポートの詳細, サンプル コピーをリクエスト
ゲノムがん検査市場におけるトップ企業:
- 株式会社イルミナ
- サーモフィッシャーサイエンス株式会社
- 酸素N.V.
- ホフマン・ラ・ロチェ株式会社
- 財団医学株式会社(ロチェ)
- 株式会社インビタエ
- 株式会社ネオゲノム研究所
- Myriad Genetics(マイリアド・ジェニックス)
- ゲノムヘルス株式会社(株式会社Exact Sciences)
- カリスライフサイエンス
- 株式会社アーチャーDX(株式会社インビタエ)
- ガードラントヘルス株式会社
- パーソナルゲノム診断株式会社
- バイオセプト株式会社
- テンパスラボ株式会社
定義: ゲノムがん検査は、ゲノム腫瘍評価とも呼ばれ、腫瘍遺伝子におけるDNA変異や変化を識別する医療試験の一種です。 DNAシーケンスにおけるこれらの変化は、細胞分裂と成長を促進し、細胞死に対する正常な制御を阻害することによって、癌の成長を促すことができます。 ゲノムがん検査の目的は、腫瘍の成長を促す可能性のあるがん細胞内の特定の遺伝子変異を識別することです。
著者について
Manisha Vibhuteは、市場調査とコンサルティングで 5 年以上の経験を持つコンサルタントです。市場動向を深く理解している Manisha は、クライアントが効果的な市場アクセス戦略を策定できるよう支援しています。彼女は、医療機器会社が価格設定、償還、規制の経路をうまく利用して、製品の発売を成功に導くお手伝いをしています。
独占トレンドレポートで戦略を変革:
よくある質問


