中枢神経系疾患を対象とした遺伝子および細胞治療の市場規模と動向 - 2026 年から 2033 年まで
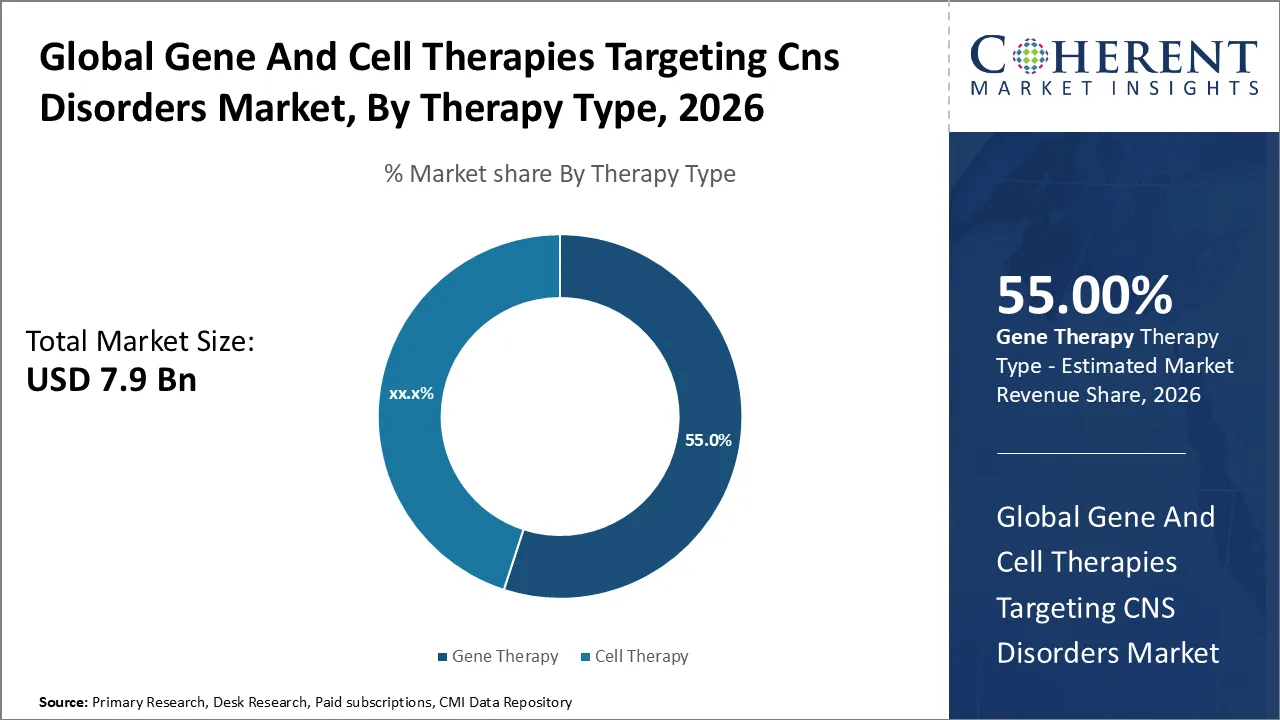
中枢神経系疾患を対象とした世界の遺伝子細胞治療市場は、2026 年に79 億米ドルと推定され、2033 年までに240 億米ドルに達すると予想されており、年平均成長率(CAGR)で成長すると予想されています。 2026 年から 2033 年までに 16.5% の割合。
重要なポイント
- 治療タイプに基づくと、遺伝子治療セグメントは、先進的な臨床プログラムと近い将来の承認により、2026 年には55%のシェアを獲得して市場をリードすると予想されます。
- 適応症に基づくと、パーキンソン病セグメントは、CNS疾患の中で最も活発な臨床試験と研究に重点を置いているため、2026年には28%のシェアを獲得すると予測されています。
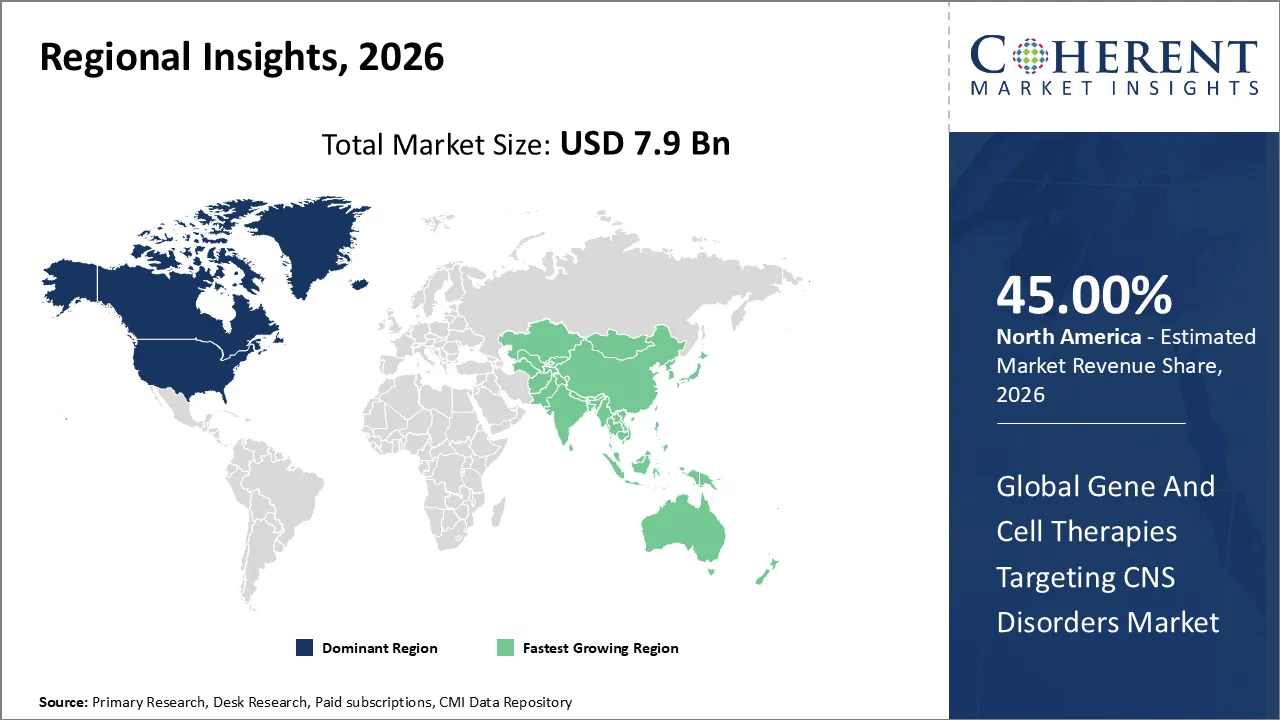
- 地域別に見ると、北米は 2026 年に中枢神経系疾患を対象とした遺伝子細胞治療市場をリードし、45% のシェアを獲得すると予想されています。一方、アジア太平洋地域は最も急速に成長している地域であると予想されています。
市場概要
パーキンソン病、アルツハイマー病、ハンチントン病などの神経変性疾患や神経疾患の有病率の増加が、CNS疾患市場を対象とした遺伝子治療および細胞治療の成長を促進する主な要因です。 遺伝子治療および細胞治療は、従来の治療法では不可能な、CNS障害に対する有望な長期治療または治癒治療を提供するため、医療従事者や患者にとって非常に魅力的なものとなっています。 さらに、遺伝子編集技術、ウイルスベクター送達システム、幹細胞研究の開発の増加が市場の成長を推進しています。 製薬会社やバイオテクノロジー企業による投資の拡大、政府の強力な支援や有利な規制の取り組みにより、CNS 疾患に対する遺伝子治療および細胞治療の市場成長がさらに促進されています。
現在のイベントとその影響 CNSをターゲットとする遺伝子および細胞療法 Disorders マーケット
現在のイベント | 説明とその影響 |
規制フレームワークの進化とポリシーの変更 |
|
CNS治療におけるAIとデジタルヘルスの統合 |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
遺伝子と細胞療法の市場インサイト, 治療の種類によって – 遺伝子 高度の臨床プログラムおよび承認による療法の優位
治療の種類によって、遺伝子治療セグメントは、2026年に55%の最高市場シェアに貢献し、高度な臨床プログラムと短期の承認を得ると推定されます。 遺伝子治療は、ハンティントンやパーキンソンなどの疾患の遺伝的原因を根本的にターゲットとするCNS障害でますます好まれています。 ウイルスベクターやCRISPRベースのアプローチなど、新たなデリバリー技術の利用可能性が高まり、他のモダリティに対する遺伝子治療の採用を強化します。
たとえば、2025年11月、米国FDA認定Itvisma®(onasemnogene abeparvovec-brve)、SMA患者の遺伝子置換療法2年以上、乳児を超えて遺伝子治療アクセスを拡大しています。
Gene & Cell Therapies Market Insights、Indicationによる - Parkinsonの病気は、強力な研究の焦点と活性臨床試験に起因する
パーキンソン病分は、2026年に28%で最大のシェアを占めることが予測されます。 遺伝子治療と細胞治療の先進的な段階でCNS病態に対する臨床検査を積極的に追求する最高数を所有しています。 パーキンソン病における研究の目的は、失われた神経機能を取り戻すことです, それによって、疾患の進行を減速, それは、市場需要のための駆動力になります. 例えば、遺伝子治療とステム細胞移植を併用する臨床研究は、将来的にその治療に大きく影響を及ぼします。
例えば、2025年9月、バイエルは、パーキンソン病の細胞治療であるベマデプロセルのピボタルフェーズIII試験を開始しました。 試験, 呼ばれる exPDite‐2, 失われたドーパミン産ニューロンを交換し、パーキンソンの第1段階の細胞療法の努力の1つを表すことを目指しています.
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカ遺伝子と細胞療法はCNS障害市場分析とトレンドを標的
北米は、2026年にCNS障害を治療するために使用される遺伝子および細胞療法のための市場で最も高い成長を期待しており、約45%の市場シェアを持っています。 これらの要因は、遺伝子および細胞療法の開発を加速する主要なバイオテクノロジーおよび製薬会社、設備の整った研究設備および好ましい規則の確立された存在に起因する可能性があります。
例えば、2025年9月、バイエル(BlueRock Therapeutics経由)は、パーキンソン病のベマデセルのピボタルフェーズIII試験を開始しました。 試験はCNS障害を対象とする地域における第一次期細胞治療プログラムの1つです。 治療は、失われたドーパミン産生ニューロンを交換するように設計されています, 神経変性疾患の最先端治療を推進する北アメリカのリーダーシップを示す.
アジアパシフィック遺伝子とCNS障害市場分析とトレンドを標的とする細胞療法
アジアパシフィック市場は、医療業界への投資の上昇、神経変性障害の認識、中国、日本、インドの臨床研究インフラの進歩による最速成長が期待されます。 アジア太平洋地域におけるバイオテクノロジーベンチャーおよび多国籍企業とのコラボレーションにより、遺伝子および細胞療法におけるイノベーションを推進しています。
例えば、2025年5月、 Belief バイオメッド 中国では、BBM-P002、パーキンソンの遺伝子治療のためのIND承認を受け、地域の最初の臨床試験を可能にしました。 この開発は、アジアパシフィック市場がCNS障害の遺伝子と細胞療法の急速な採用を反映しており、グローバル市場成長に大きく貢献する可能性を秘めています。
米国のためのCNS障害市場見通しをターゲットとする遺伝子と細胞療法.
研究のリーダーシップと臨床的進歩からブームするCNS障害のための米国遺伝子および細胞療法の市場はありますか?
米国市場は、強力なバイオテクノロジーの存在、高度な臨床試験インフラストラクチャ、および遺伝子および細胞療法の開発を加速する支持的規制フレームワークによって燃料を供給し、ブームしています。 地域は、パーキンソン、アルツハイマー、ALSなどの神経変性疾患を標的とした治療におけるイノベーションの拠点となっています。
たとえば、2025年9月には、Gene Solutionsは、アルツハイマー病やパーキンソン病を含む神経疾患を標的とするミトコンドリア療法プラットフォームの特許を保護し、CNS障害の治療薬を次世代に発展させるために利用できるツールを広げることを発表しました。 特許は、ミトコンドリア機能、ニューロンデジェネレーションの重要な側面に対処するために設計された治療のための米国における研究開発能力を強化します。
中国のためのCNS障害市場Outlookをターゲットとする遺伝子と細胞療法
中国はCNS遺伝子および細胞療法の採用を高めるヘルスケアおよび臨床試験の生態系を成長させていますか?
中国の市場は、医療費の増大、有利な政府規制、およびバイオテクノロジーの現地の知識と専門知識の急成長を期待しています。 規制の改善と国際臨床試験への参加は、CNSターゲット遺伝子および細胞療法における主要なプレーヤーとなります。
例えば、2025年8月には、NMPAは、原子トロフィック横の脊柱側弯症(ALS)の新しい遺伝子治療であるSNUG01のINDアプリケーションをクリアすると発表し、中国と米国の両方でフェーズI/IIa多領域臨床試験を有効にします。 SNUG01のINDマークのクリアランスは、主要な神経変性障害に及ぶCNSに焦点を当てた遺伝子治療を開発しています。
マーケットレポートスコープ
遺伝子と細胞療法はCNS障害市場レポートカバレッジを標的
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2025年 | 2026年の市場規模: | 米ドル 7.9 Bn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2026 へ 2033 |
| 予測期間 2026〜2033 CAGR: | 16.5%の | 2033年 価値の投射: | 米ドル 24.0 Bn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | Novartis、BrainStorm Cell Therapeutics、Corestem、Q Therapeutics、Helixmith、Rapa Therapeutics、Neuroplast、SteemCyte、Ferrer Internacional、Neuralstem、Stemedica Cell Technologies、Libella Gene Therapeutics、Sangamo Therapeutics、Hoffmann-La Roche、LSio Gene Therapies、Lelily and Company、Neurotherapy、Neurotherapy、Neuro... | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
マーケット・ダイナミクス
GeneとCNS Disorders市場ドライバーをターゲットとするセルセラピー
神経変性疾患の有望性
パーキンソン病などのCNS障害の増大、 アルツハイマー病ALSは市場成長に貢献する主要な要因の一つです。 多くの患者は、世界の高齢化人口による現在、これらの進行性障害の影響を受けています。 これは、症状の管理ではなく、疾患の進行状況を変更したり、遺伝子および細胞療法ソリューションにおける投資および開発を運転したりすることができる高度な療法のための強力な要求を作成します。
CNS Disorders Market Opportunityをターゲットとする遺伝子と細胞療法
革新的な遺伝子と細胞療法プラットフォームの開発
市場は、遺伝子および細胞療法の領域における新興イノベーションの踵の拡張に大きな可能性を秘めており、ウイルス性ベクトルベースの遺伝子治療、CRISPRベースの遺伝子編集アプローチ、および幹細胞から得られた神経先駆細胞の使用を伴います。 CNSターゲットセラピスの安全性と有効性を保証できるイノベーションは、市場での非メートルの医療ニーズをタップする機会を持つ企業を提示するためにバインドされています。
アナリストオピニオン(エキスパートオピニオン)
CNS障害を標的とする遺伝子および細胞療法の市場は、最先端の科学によって運転され、病気修正治療のための緊急の必要性が急速に進んでいます。 パーキンソン、アルツハイマー、ALS、CNS障害を補強し、不当と見なす、治療の介入のために最終的に実行可能なターゲットであるパーキンソンの後半段階の試験では、いくつかのプログラムが今あります。 ベマデセルとAskBioのAB 1005アンダースコアマーションのバイエルのピボタルトライアルなどのプログラムでは、損傷した神経機能を復元するか、または置き換えるように設計されました。
ほとんどの療法は、ウイルスベクター遺伝子の配信、幹細胞由来のニューラルプロジェニター、遺伝子の編集ツールなどの洗練された技術を利用し、様々なアプローチにおける複雑さと精度の高まりを反映しています。 初期の臨床信号は、有効性のハードルだけでなく、安全ハードルも満たされていることを示しています, 市場への信頼性を貸し、さらなる投資を奨励.
北米は、研究と開発のための優勢な拠点であり、強力なバイオテクノロジーエコシステム、経験豊富な臨床インフラ、および規制対応の恩恵を受けています。 同時に、中国は、規制当局の承認を受けている複数の企業で、初めての臨床試験を開始しています。 アジアパシフィックの革新的なパイプラインと進化する規制枠組みの組み合わせは、CNS療法開発の未来の拠点として地域を位置付けています。
ランドスケープは、増分、症状管理による治療から、真に変化する治療法へと移行しています。 希少または複雑なCNS障害に対するターゲティングされた介入に焦点を当て、企業による戦略的移動を実証し、広範囲にわたるアプローチで精密医薬品を優先します。 この市場はもはや推測的ではありません。それは、以前に考えられなかった方法で、次世代の神経治療薬の潜在能力を実証し、忍耐強いケアを高めるための重要なアリーナになっています。
CNS障害業界ニュースをターゲットとする遺伝子と細胞療法
- 11月2025日、ノバルティスは、米国FDA認定Itvisma®(onasemnogene abeparvovec-brve)、脊椎筋萎縮(SMA)のための遺伝子置換療法、高齢者、十代、大人への治療の拡大を発表しました。
- 5月2025日 お問い合わせ 結果発表の発表 運動障害におけるパーキンソン病のためのAB-1005遺伝子治療のフェーズ1b試験は、治療が臨床的傾向を奨励することで良好に許容されました。
- Longeveronは2025年3月、Natural Alzheimerの病気のPhase 2a laromestrocel (Lomecel-BTM)の臨床試験の結果がNature Medicineに掲載され、改善された認知機能、生活の質、および脳の容積を実証し、CNS障害の治療の可能性を強化しました。
市場区分
- 療法のタイプ洞察(Revenue、USD Bn、2026 - 2033)
- 遺伝子治療
- 細胞療法
- 徴候(Revenue、USD Bn、2026 - 2033)
- アルツハイマー病(AD)
- ハンティントン病(HD)
- パーキンソン病(PD)
- Amyotrophic の横のSclerosis (ALS)及びモーター ネオン病気
- 多発性硬化症(MS)
- Adrenoleukodystrophyとメタクロマチック レコディストロフィー
- ニューロパシーズ
- バットテン病(BD)
- 地域インサイト(Revenue、USD Bn、2026 - 2033)
- 北アメリカ
- アメリカ
- カナダ
- ラテンアメリカ
- ブラジル
- アルゼンチン
- メキシコ
- ラテンアメリカの残り
- ヨーロッパ
- ドイツ
- アメリカ
- スペイン
- フランス
- イタリア
- ロシア
- ヨーロッパの残り
- アジアパシフィック
- 中国・中国
- インド
- ジャパンジャパン
- オーストラリア
- 韓国
- アセアン
- アジアパシフィック
- 中東
- GCCについて 国土交通
- イスラエル
- 中東の残り
- アフリカ
- 南アフリカ
- 北アフリカ
- 中央アフリカ
- 北アメリカ
- キープレーヤーの洞察
- ノベルティ
- BrainStorm細胞治療薬
- コアステム
- Q 治療薬
- ヘリックスミス
- ラパ治療薬
- ネロプラスト
- ステムケイト
- フェラー・インターナル
- ネラルステム
- Stemedica の細胞の技術
- リベラ遺伝子治療薬
- サンガモの治療薬
- ホフマン・ラ・ロチェ
- LSio遺伝子治療
- エリ・リリーと会社
- ニューロジェネレーション
- 脳神経治療バイオ(AskBio)
- ユニキュアバイオ医薬品
ソース
第一次研究インタビュー
- バイオテクノロジー&医薬品研究開発ヘッド
- 遺伝子と細胞治療科学者
- 臨床試験の研究者と神経科医
- 法令・コンプライアンス役員
- 病院・学術 リサーチセンター・ディレクター
- バイオテクノロジー投資家とベンチャーキャピタルアナリスト
- その他
データベース
- 臨床トライアル.gov
- パブフィード
- WHO国際臨床試験レジストリプラットフォーム(ICTRP)
- 米国FDAデータベース(Drugs & Biologics)
- 欧州医薬品庁(EMA)データベース
- 国家医療製品管理(NMPA、中国)
- その他
雑誌
- 自然バイオテクノロジー
- 遺伝子工学・バイオテクノロジー ニュース
- バイオセンター
- ファーマボイス
- ファースバイオテクノロジー
- その他
ジャーナル
- 分子療法
- 幹細胞レポート
- Neuroinflammationのジャーナル
- 運動障害
- 神経科学のフロンティア
- その他
新聞
- ウォールストリートジャーナル(健康&バイオテクノロジー部門)
- ファイナンシャル・タイムズ(医薬・ヘルスケア)
- ロイターヘルス&サイエンス
- ブルームバーグニュース(バイオテクノロジーカバレッジ)
- ニューヨークタイムズ(保健課)
- その他
協会について
- 幹細胞研究国際社会(ISSCR)
- 遺伝子と細胞療法のためのアメリカの社会(ASGCT)
- パーキンソン財団
- アルツハイマー協会
- 国際細胞療法学会(ISCT)
- その他
パブリックドメインソース
- 米国国立医学図書館出版
- 神経障害に関するWHOレポート
- FDAの生物的論理免許証の塗布及び承認
- 電子メール 規制更新とパブリックアセスメントレポート
- CDC・NIHによる臨床ガイドライン
- その他
独自の要素
- ログイン データ分析ツール
- プロモーション CMI 過去8年間の情報の既存のリポジトリ
独占トレンドレポートで戦略を変革:
よくある質問