治験管理システム市場規模と予測 - 2025〜2032
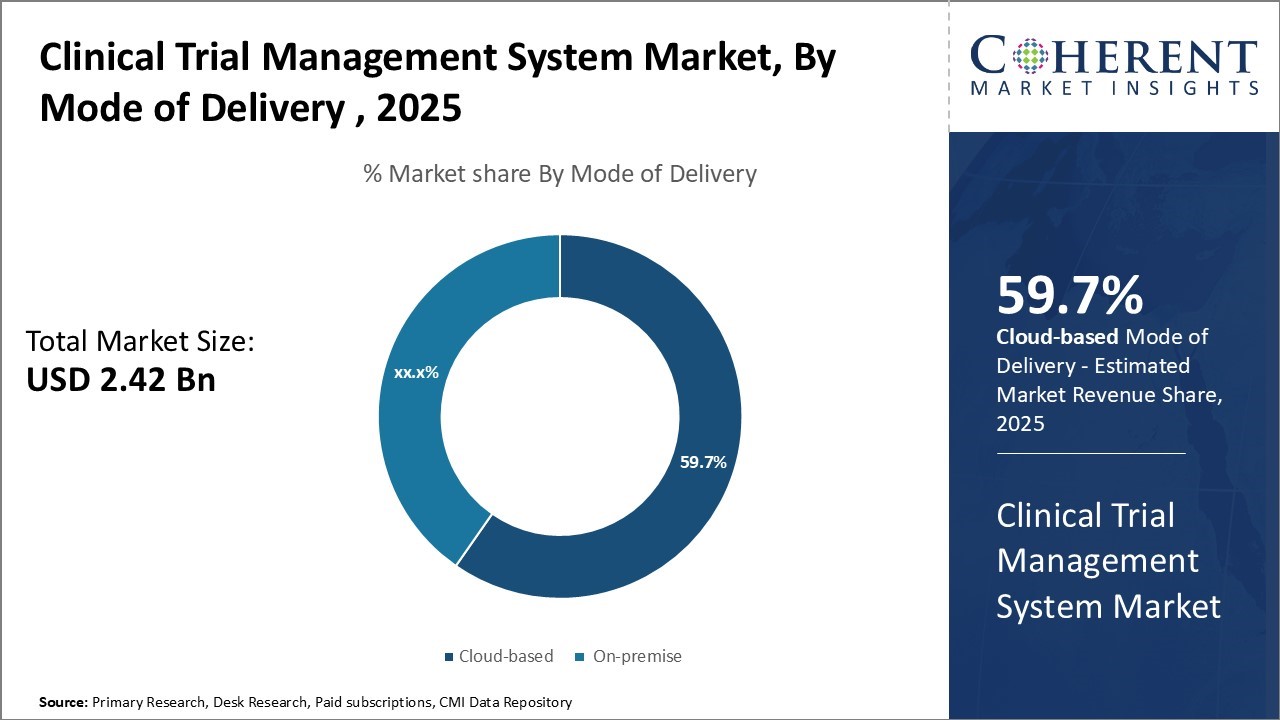
治験管理システム市場は評価されると推定されます米ドル 2.42 Bn 2025年、到達見込み米ドル 6.47 Bn 2032年までに、化合物の年間成長率を示す15.1%のCAGR2025年~2032年
キーテイクアウト
- 配信モードによって、オンプレミスは、データセキュリティとプライバシーの懸念として、2025年に59.7%の著名なシェアを獲得しました。
- コンポーネントによって、ソフトウェアは、臨床試験の複雑性を高めるために、2025年に70.6%の推定シェアで全体的な市場を支配します。
- エンドユーザーによるバイオ医薬品 企業は、その増加数の臨床試験に40.5%の最大の市場シェアを保持します。
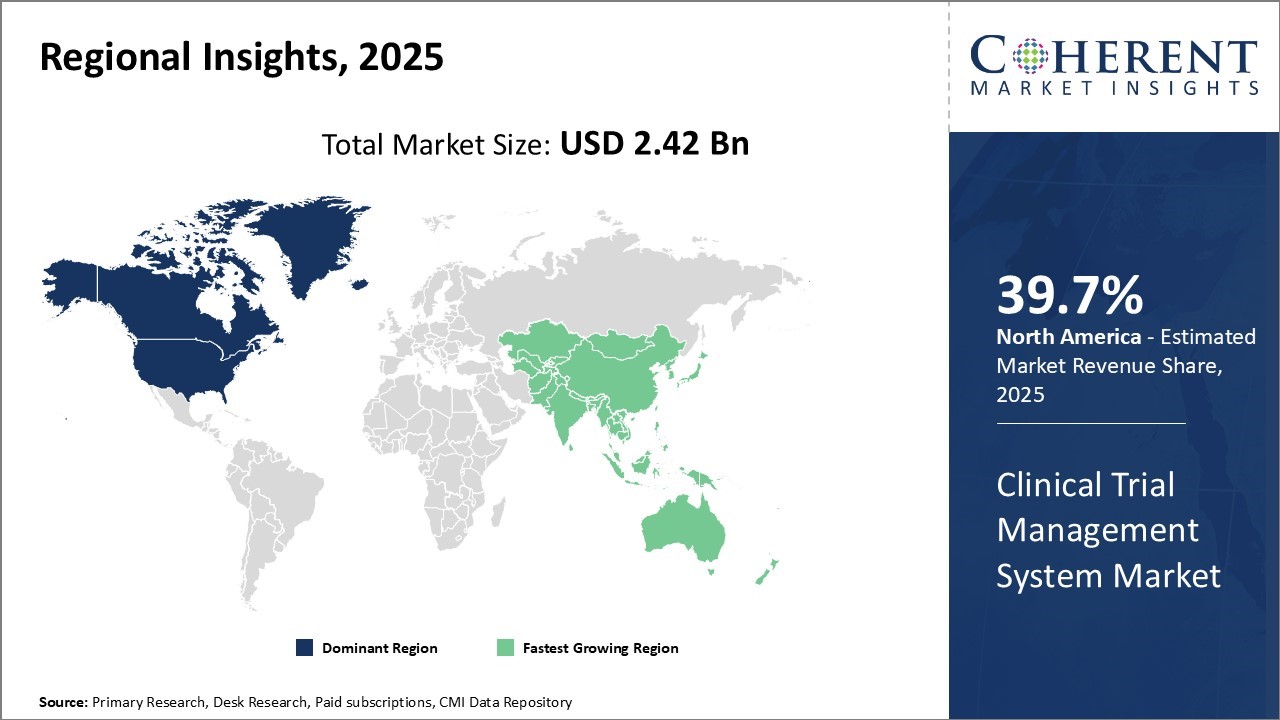
- 地域別、北米は、技術の発展とAIの統合として、2025年に39.7%の著名なシェアを獲得しました。
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
市場概観
臨床試験管理システム市場は、予測期間にわたって重要な成長を目撃することが期待されます。 世界中で実施されている臨床試験の数が年単位で増加しています。 また、医薬品やバイオテクノロジーの研究開発の普及が進んでおり、新たな医薬品分子の開発にも貢献しています。 さらに、臨床試験のアウトソーシングを増加させることで、治験管理システムの採用が増加し、コンプライアンスを維持し、試験の効率性が向上し、市場拡大を支援します。 費用追跡、タイムリーなレポート生成、監視性能の表示器、および冗長性を減らすなどの手動処理上のCTMSソフトウェアによって提供されるさまざまな利点は、これらのシステムのための要求をさらに運転しています。
現在のイベントとその影響 治験管理システム市場
現在のイベント | 説明とその影響 |
EUの臨床試験規則の完全な実装と規制調和 |
|
分散型臨床試験規制終了と市場変革 |
|
米国政府治験インフラ整備への取り組み |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
エンドユーザーフィードバックとアンメットは、 治験管理システム市場
- 複雑なユーザー インターフェイスおよび貧しいユーザビリティ: 臨床試験コーディネーターと現場のスタッフは、CTMSプラットフォームが直感的なインターフェイスを持っていることをよく報告し、広範なトレーニングを必要とする。 エンドユーザーは、シンプルなダッシュボードを探し、一般的なタスクを数回クリックするだけで、よりユーザーフレンドリーなナビゲーションで生産性を向上させ、トライアルのセットアップと実行中に運用遅延を削減します。
- 他のシステムとの限られた統合: ユーザーは、CTMS と EHR、EDC、ラボプラットフォームなどのシステムとの間の統合を頻繁に強調します。 相互運用性の欠如は、データの入力を複製し、エラーを増加させます。 エンドユーザーは、データフローを改善し、管理上の負担を軽減し、システム全体のデータの一貫性を維持するためにシームレスな接続を望んでいます。
- 柔軟性のあるカスタマイズ オプション: 多くのスポンサーとクロスは、現在のCTMSプラットフォームは、独自のワークフローやプロトコル要件に対応する柔軟性がないと述べています。 設定可能なモジュール、カスタマイズ可能なフォーム、および適応可能なワークフローを要求します。これは、特定の治療領域または試行フェーズと組み合わせて、コストリーなIT介入を必要としません。
臨床試験管理における人工知能(AI)の役割
AIは、データの処理を合理化し、精度を向上させることで、臨床試験データ管理システムにおいて重要な役割を果たしています。 これは、電子健康記録のようなソースから構造化され、構造化されていないデータの抽出と統合を自動化し、手動のエラーを減らす。 AI搭載のツールは、データをクリーンかつ検証し、分析のための高品質を保証します。 また、AIは、参加者のマッチングにより、より効率的に試用基準を強化し、患者様の採用を強化します。 自然言語処理(NLP)は、非構造の臨床メモから貴重な洞察を抽出するのに役立ちます。
2025年4月、AI主導のライフサイエンス分析ソリューションであるAxtria Inc.は、LUCCID(LLMベースの非構造臨床コンセプトの特定)を発売しました。 このGenAI搭載ソリューションは、電子健康記録(EHR)から非構造化データの抽出と処理を変換します。 構造化されたデータを処理するFHIR ベースの EHR-to-EDC システムを補完する設計, LUCCID は、手動で非構造の臨床試験データを抽出する主要な課題に対処します。, すべての試験情報の 80% を構成する.
治験管理システム市場 洞察、配信モードによる - オンプレミスは、その市場へのオウイングの最高のシェアに貢献 カスタマイズと統合のニーズ
オンプレミスは、最高のシェアに貢献することが期待されます59.7%(税抜き)で 2025. オンプレミスのCTMSは、エンドユーザの広範な運用ニーズとデータベースによって広くカスタマイズされている統合システムを提供します。 これは、他の内部のレガシーシステムとCTMSの統合を可能にし、治療領域や試験の複雑さに固有のカスタマイズされた機能を備えています。 大規模な製薬とCROは、グローバルな試験、調査員のエンゲージメント、ラボサンプル管理、サプライチェーンの調整、安全データ分析などの管理に関わる、非常に複雑な運用ワークフローを持っています。 オンプレミスのCTMSは、集中化されたプラットフォームを提供し、複雑な試験のすべての側面を監督します。 カスタマイズされたインターフェイス、役割ベースのアクセス、LIMS、EDCおよび他の内部アプリとの統合は継ぎ目が無いデータ交換を保障します。 全試験データへのアクセスを一元化し、統合することで効率性を高めます。 また、オンプレミスシステムは、機密性の高い患者データを組織に管理し、より高いデータセキュリティを実現します。
治験管理システム市場 インサイト、コンポーネントによる - ソフトウェアは、その市場へのオウイングの最高のシェアに貢献します リアルタイムのデータアクセスと分析の必要性
ソフトウェアセグメントは、最大の市場シェアに貢献することが期待されます70.6%で 2025. 現在、CTMSソフトウェアパッケージは、サイト選定や契約、患者登録追跡、ラボデータ統合、サプライチェーン管理、安全報告など、幅広い機能を備えています。 ファーマとクロスは、密接なエクセルシートとレガシーシステムを排除し、一元化された「ペーパーレスオフィス」ソリューションを提供するカスタマイズ可能なCTMSプラットフォームを好むようになりました。 統合ソフトウェアスイートは、サイトランダム化と支払い、ラボサンプルコーディング、ドキュメントの承認、供給注文、および統合されたECDキャプチャeCRFデータのための機能を備えた単一のプラットフォーム上で、グローバルな試験を監督するのに役立ちます。 これは、単一の共同スペースで臨床操作、モニター、およびデータ管理者の合理化された活動を持っています。 ニッチ治療領域とバイオマーカーベースの試験に焦点を当てた専門CTMSプロバイダーの上昇は、統合ソリューションの利用可能なスイートをさらに拡大しました。
例えば、2024年11月には、SlopeとLabConnectは、臨床試験業界に役立つ双方向アプリケーションプログラミングインターフェース(API)の統合を導入しました。
治験管理システム市場 エンドユーザーによるインサイト - バイオ医薬品 企業は、その市場へのオウイングの最高のシェアに貢献します 規制遵守とデータの完全性の必要性
Biopharmaceuticalの企業の区分は2025年に40.5%の全体的な臨床試験の管理システムの市場での最も高い共有に寄与すると期待されます。 Biopharmaは複数の生物的moieties、まれ/orphanの徴候およびbiomarker主導の混合物を含むパイプラインを絶えず拡大しました。 このような複雑な分子の巧妙な開発と商品化は、堅牢な試験計画フレームワーク、グローバル調査ネットワーク、および細心のサプライチェーンの調整が必要です。 バイオファーマに適したCTMSは、世界中の何百ものサイトを横断して、新しいバイオマーカー、特殊なCROエンゲージメント、ラボサンプルマッピングを含むプロトコルをカスタマイズできます。 弊社のスケーラブルなグローバルトライアルネットワークは、翻訳、決済、コールドチェーンのコンプライアンス、リアルタイムの安全レポートなどの機能によって効率的に管理されています。
例えば、2025年4月、Veeva Systemsは、SiteVault eISFとSiteVault eConsentと統合する研究拠点のための臨床試験管理システムであるVeeva SiteVault CTMSを発表しました。 このようなイノベーションは、臨床試験管理システム市場収益を増大しています。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカ 治験管理システム市場 トレンド
北米は39.7%の最大のシェアを獲得しました。 北米のバイオ医薬品会社とCROは、クラウドベースのプラットフォームを採用し、AIを統合して試験効率を高め、分散型試験モデルを組み込むことで、臨床試験管理システム(CTMS)市場の成長を促進しています。 規制要件を満たし、リアルタイムのデータ監視を有効にするための高度なCTMSソリューションに積極的に投資しています。
政府は、臨床研究をサポートし、スポンサーと研究拠点間のコラボレーションを強化し、世界的な臨床開発における北米のリーダーシップを強化しています。 例えば、より高速で信頼性の高い臨床試験を行うための「アンチクロ」として知られるLindus Healthは、その包括的な契約研究組織(CRO)と、眼科臨床試験の実行をサポートする技術ソリューションを開始しました。 また、世界中で臨床試験の4%を占めるカナダのアカウントで、臨床試験サイト数で4位を獲得しています。 治験の生産性をG7に導き、集団規模の試験数で測定します。 2023年、カナダは、新しい臨床試験の総数と4分の4の合計で3分の1をグローバルにランク付けし、臨床試験管理システム市場シェアをさらに加速しました。
アジアパシフィック 治験管理システム市場 トレンド
アジア・パシフィック地域では、CTMSプラットフォームをAIと機械学習で強化し、プロトコルの最適化、採用の成功の予測、データの不規則性の特定に活用しています。 モバイルアプリやリモート監視ツールを活用し、分散型およびハイブリッドトライアルを実施。 スポンサーは、フェーズIIIの採用を加速するために、地域の大規模で多様な人口と低コストを活用しています。 その結果、世界規模の製薬会社やCROは、CTMSの採用を推進するインド、中国、東南アジアなどの国々への調達試験がますます進んでいます。 例えば、グローバルITサービス、コンサルティング、ビジネスソリューションプロバイダーのタタタコンサルティングサービス(TCS)は、革新的なSaaSプラットフォームであるConnected Clinical Trials(CCT)を開始しました。 このプラットフォームは、製薬企業が臨床試験における患者の関与を変革し、臨床供給プロセスの効率性と説明性を高めるのに役立ちます。
アメリカ合衆国 治験管理システム市場 トレンド
米国では、CTMS プロバイダーは、高度な技術を統合し、患者の登録を予測し、試験プロトコルを精製し、異常をリアルタイムで特定します。 定期的なプロセスを自動化し、データの正確さを改善し、スポンサーやクロスが試行をスピードアップし、操作を簡素化することができます。 トライアルチームは、CTMS対応のモバイルアプリ、リモート監視、およびCTMS対応のモバイルアプリを利用しています。 テレメディシン 分散型およびハイブリッド研究を行うためのツール。 これらの技術は、農村人口へのアクセスを拡大し、データ収集を強化し、試験参加者の負担を軽減します。
2024年1月、BSI ライフサイエンスは、クラウドベースの臨床試験管理システムを搭載した最新のクライアント、Ocular Therapeutixのデモを発表しました。
インド 治験管理システム市場 トレンド
インドの臨床試験管理システム(CTMS)市場は、臨床研究活動が拡大し、デジタルプラットフォームの採用が上昇し、グローバル製薬企業が関与を増加させるにつれて急速に進んでいます。 インドのクロスと研究所は、CTMSソリューションを積極的に採用し、試験監督を強化し、規制基準を満たし、マルチサイトの試験管理を合理化しています。 例えば、2025年3月では、 臨床段階の医療バイオテクノロジー会社であるNeOnc Technologies Holdings, Inc.は、先見フルサービス臨床研究機関(CRO)であるCBCC Global Research(CBCC)との戦略的パートナーシップを発表しました。 このコラボレーションは、開発段階の神経腫瘍学的治療の進歩を促進し、インドのNeOncの臨床試験能力を拡大します。 治験管理システム市場需要のさらなる増大
治験管理システム市場 ニュース
- 2025年4月、次世代医薬品開発研究・サービスのリーディングプロバイダーであるPrecision for Medicine(Precision for Medicine)が、戦略的コラボレーションを実現 パスタイデジタル病理学のグローバルリーダー。 共に、新しいAIベースの技術を開発し、PathAIの高度なデジタル病態学と分析能力を、医薬品の臨床試験とバイオスピーメン操作の精度に統合します。
- 2024年10月、Medableは、Google Cloud Marketplaceの臨床試験ソフトウェアソリューションを立ち上げました。 新しく導入されたMedable Studioを含む、Google CloudのインフラとAI機能をプラットフォームに統合することで、臨床試験ソリューションのパフォーマンスとスケーラビリティを高めます。
- 2024年9月、リンダスヘルスは、より迅速で信頼性の高い臨床試験を実施するための「アンチクロ」として知られ、包括的な契約研究機関(CRO)を立ち上げ、眼科臨床試験の実行をサポートするように設計された技術ソリューション。
マーケットレポートスコープ
臨床試験管理システム市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 2.42 Bn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 15.1%(税抜) | 2032年 価値の投射: | 米ドル 6.47 Bn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
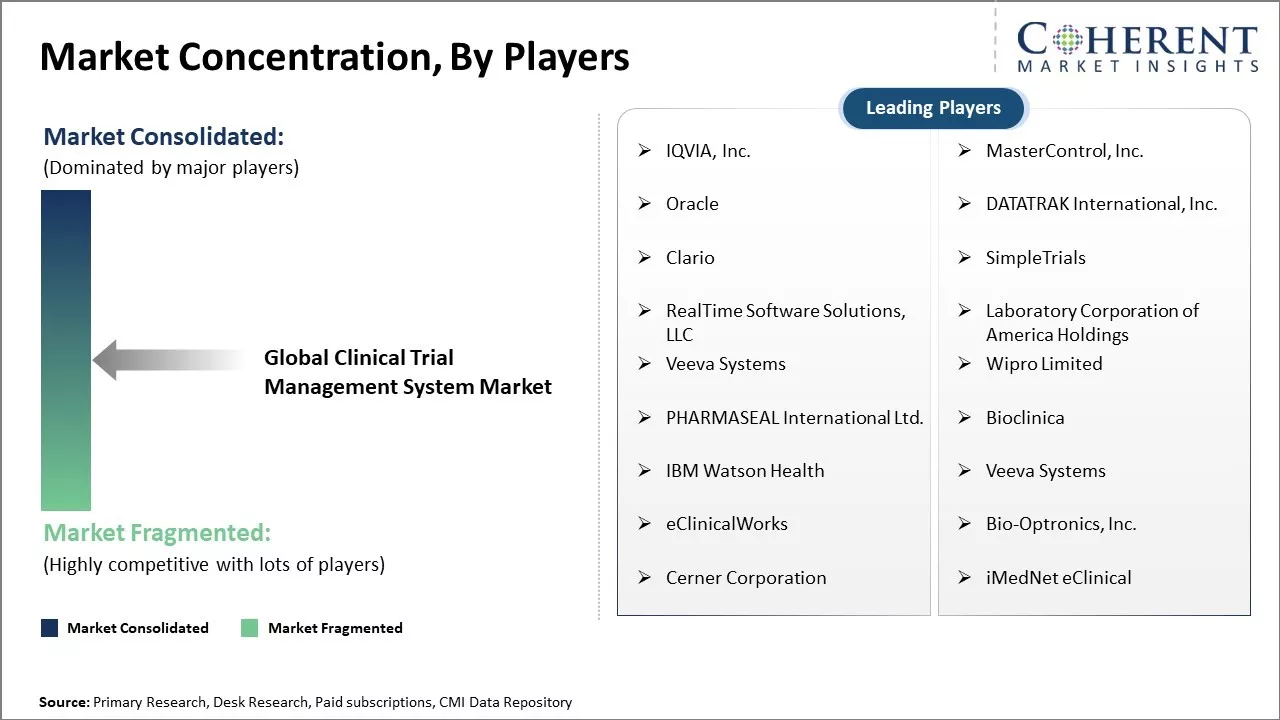
| 対象会社: | IQVIA, Inc., MasterControl, Inc., Oracle, DATATRAK(Oracle, DataTRAK), Inc.(MasterControl, Inc.), Oracle, DATATRAK(Oracle, DataTRAK), Inc.(MasterControl, Inc.), Oracle, DataTRAK(Oracle, DataTRAK), Inc.(MasterControl, Inc.), Oracle, DataTRAK(Oracle, DataTRAK), Oracle, DataTRAK(Oracle, DataTRAK), Inc.), IQVIA, Inc.(MasterControl, Inc.), Oracle, Oracle, DataTRAK(Oracle, DataTRAK), Inc.), Inc.) 国際、Inc.、Clario、SimpleTrials、RealTime Software Solutions、LLC、アメリカホールディングス、Veeva Systems、Wipro Limited、PHARMASEALインターナショナル株式会社、Bioclinica、IBM Watson Health、Veeva Systems、eClinicalWorks、Bio-Optronics、Inc、Cerner Corporation、およびiMedNet eClinical | ||
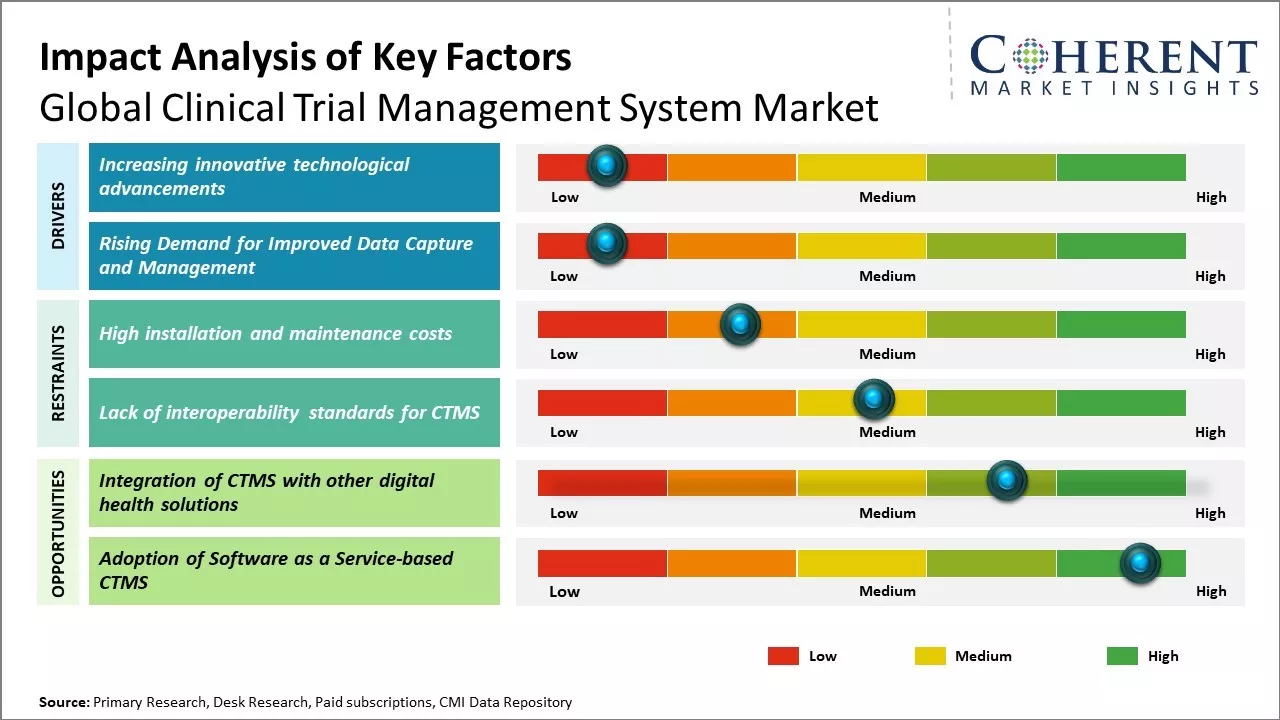
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
治験管理システム市場 トレンド
- クラウドベースとSaaS CTMSソリューションの採用
組織は、クラウドベースおよびSaaS CTMSプラットフォームへの移行が進んでおり、集中的なアクセスを可能にし、インフラコストを削減し、リモートワーク環境をサポートします。 これらのソリューションは、スポンサー、クロス、およびリサーチサイト間でリアルタイムコラボレーションを提供し、地理的に分散したチーム間でのデータアクセシビリティを向上させます。 クラウドベースのCTMSは、より高速な実装、システムスケーラビリティ、および簡素化されたアップグレードを容易にし、グローバルまたはマルチサイトトライアルを実施する企業にとって魅力的な選択肢となっています。
- 分散型およびハイブリッドトライアルのライジング要求
分散型およびハイブリッド臨床試験モデルに対する成長したシフトは、CTMSの設計と機能性を著しく影響しています。 スポンサーとクロスは、テレメディシン、ウェアラブルデバイス、リモートデータ収集ツールとシームレスに統合するプラットフォームを必要としています。 この傾向は、特にリモートまたは保存されていない場所で、より大きな患者のアクセシビリティと参加のためのより広いプッシュを反映しています。また、デジタル監視と仮想サイト相互作用によるデータのタイムラインと試験効率を改善します。
アナリストオピニオン(エキスパートオピニオン)
- CTMS市場は、臨床試験設計と実行における変革シフトにより、増分改善により、より少なく駆動される、ピボタル交差点にあります。 分散型臨床試験(DCTs)の急激な取り組みは、従来のCTMSプラットフォームの制限を明らかにし、リアルタイムのデータ統合とリモート患者管理に歴史的に苦労しています。 最近のTutfts Center for Drug Development Reportによると、分散型試験は最大30%の患者の採用タイムラインを削減できますが、複雑なリモートワークフローを扱うことができる堅牢でアジャイルなCTMSソリューションによってサポートされる場合に限ります。
- もう一つの見下ろす側面は、AIの役割であり、未来的なアドオンとしてではなく、運用意思決定を変革するコア機能です。 ベンダーは、AIを組み込んで患者のドロップアウトを予測し、サイトの選択を最適化し、プロトコルの修正を予測することは、既に測定可能な利点を配信しています。 例えば、IBM Watson Healthのような企業が展開するAI主導の患者様採用モデルは、20〜25%の登録率を報告し、データ主導の精度がもはやオプションではなく、重要でないと宣言しています。
- しかし、市場における急速なイノベーションは、ユーザビリティが犠牲になれば、エンドユーザーを占有するリスクを加速します。 アプライド・クリニカル・トライアルを含む複数の業界調査からのフィードバックは、一貫して複雑なユーザー・インタフェースを主要な痛みのポイントとして挙げ、採用を遅くし、ROIを減少させます。 プロバイダーは、現場や地域にさまざまなデジタルリテラシーレベルに対応する、直感的でロールベースのデザインで最先端のテクノロジーをバランス良くする必要があります。
- これとは別に、規制の複雑さは重要な障壁です。 電子記録やEMAの新しい臨床試験規制に関するFDAのガイダンスのような進化したフレームワークでは、CTMSベンダーは、チェックボックスではなく、動的機能としてコンプライアンスを埋め込む必要があります。 規制シフトを予測する適応可能なプラットフォームの提供に成功する人々は、ますます高度にフラグメントされたグローバルな風景をナビゲートするスポンサーのための巨大な値のロックを解除します。
市場区分
- 配信インサイトモード(Revenue、USD Bn、2020 - 2032)
- クラウドベース
- オンプレミス
- コンポーネントの洞察(Revenue、USD Bn、2020 - 2032)
- ソフトウェア
- サービス
- エンドユーザーインサイト(Revenue、USD Bn、2020 - 2032)
- ヘルスケア企業
- バイオ医薬品会社
- 臨床研究機関
- 学術・研究所
- その他
- 地域洞察(Revenue、USD Bn、2020 - 2032)
- 北アメリカ
- アメリカ
- カナダ
- ラテンアメリカ
- ブラジル
- アルゼンチン
- メキシコ
- ラテンアメリカの残り
- ヨーロッパ
- ドイツ
- アメリカ
- スペイン
- フランス
- イタリア
- ロシア
- ヨーロッパの残り
- アジアパシフィック
- 中国・中国
- インド
- ジャパンジャパン
- オーストラリア
- 韓国
- アセアン
- アジアパシフィック
- 中東
- GCCについて 国土交通
- イスラエル
- 中東の残り
- アフリカ
- 南アフリカ
- 北アフリカ
- 中央アフリカ
- キープレーヤーの洞察
- IQVIA株式会社
- マスターコントロール株式会社
- オラクル
- データトラック 株式会社インターナショナル
- クラリオ
- シンプルトライアル
- リアルタイムソフトウェアソリューション, LLC
- アメリカホールディングス株式会社
- Veevaシステム
- ウィプロ株式会社
- ファーマシール 株式会社インターナショナル
- バイオクリニカ
- IBM Watson 健康
- eClinicalワークショップ
- バイオオプトロニクス株式会社
- サーナー株式会社
- iMedNet電子臨床
著者について
Komal Dighe は、市場調査とコンサルティングで 8 年以上の経験を持つ経営コンサルタントです。彼女は、ヘルステック コンサルティング レポートで高品質の洞察とソリューションを管理および提供することに優れています。彼女の専門知識は、一次調査と二次調査の両方の実施、クライアントの要件への効果的な対応、市場の推定と予測に優れています。彼女の包括的なアプローチにより、クライアントは徹底的かつ正確な分析を受けられるため、情報に基づいた意思決定を行い、市場の機会を活用できます。
独占トレンドレポートで戦略を変革:
よくある質問