américain des produits biopharmaceutiques non oncologiques Marché- Insights
Les produits biologiques peuvent être définis comme des molécules dérivées de cellules vivantes telles que des microorganismes, des plantes ou des cellules animales et utilisées dans le traitement, le diagnostic ou la prévention des maladies. La plupart des molécules biologiques sont de très grandes molécules complexes ou un mélange de molécules.
Les produits biopharmaceutiques font partie d'une catégorie plus large d'agents thérapeutiques appelés produits biologiques. Les produits biopharmaceutiques sont les substances développées dans les systèmes vivants à l'aide de la biotechnologie et sont utilisées dans des applications thérapeutiques et diagnostiques. Les produits biopharmaceutiques non oncologiques sont les médicaments utilisés dans le traitement de diverses maladies plutôt que le cancer tels que la polyarthrite rhumatoïde, le rhumatisme psoriasique, la sclérose en plaques, l'hémophilie, la dégénérescence maculaire liée à l'âge, l'ostéoporose, etc.
Augmentation des lancements, des approbations et du pipeline robuste de nouveaux produits biopharmaceutiques pour les indications non oncologiques
On s'attend à ce que les approbations fréquentes, les lancements et le pipeline robuste de nouveaux produits biopharmaceutiques non oncologiques pour diverses indications sur le marché américain appuient de façon significative la croissance du marché américain des produits biopharmaceutiques non oncologiques.
Par exemple, en septembre 2018, Eli Lilly and Company a reçu l'approbation de la Food and Drug Administration (FDA) des États-Unis pour son injection d'Emgality (galcanezumab-gnlm) de 120 mg, pour le traitement préventif de la migraine chez les adultes.
En février 2018, Novartis a annoncé que la Food and Drug Administration (FDA) des États-Unis a approuvé une mise à jour de l'étiquette de son Cosentyx (secukinumab), le premier inhibiteur de l'interleukin-17A (IL-17A) approuvé pour traiter le psoriasis en plaques modéré à sévère.
En juillet 2018, Amgen Inc. et UCB Inc. ont présenté à nouveau la demande de licence de produits biologiques (BLA) à la Food and Drug Administration (FDA) des États-Unis pour EVENITY (romosozumab), un anticorps monoclonal expérimental pour le traitement de l'ostéoporose chez les femmes ménopausées à haut risque de fracture.
La taille du marché des produits biopharmaceutiques non oncologiques aux États-Unis a été évaluée à 116,0 $US. Bn en 2018 et devrait être témoin d'un TCAC de 10,2% au cours de la période de prévision (2018-2026).
Graphique 1. Part du marché des produits biopharmaceutiques non oncologiques aux États-Unis (%), par type de produit, 2018-2026
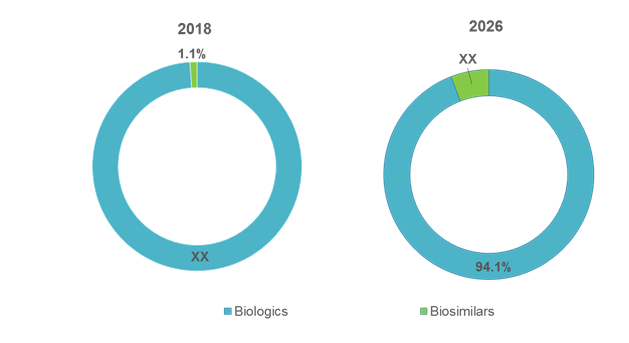
Pour en savoir plus sur ce rapport, demander un exemplaire
Source: Analyse cohérente des perspectives du marché (2018)
L'augmentation des fusions et des collaborations entre les principaux acteurs pour le développement de nouveaux produits biopharmaceutiques non oncologiques devrait soutenir la croissance du marché
Les principaux acteurs du marché sont impliqués dans des fusions stratégiques et des collaborations pour le développement de nouveaux produits biopharmaceutiques et pour les commercialiser aux États-Unis. De telles fusions stratégiques et collaborations entre les principaux acteurs sont censées soutenir le développement de nouveaux produits, ce qui devrait à son tour alimenter la croissance du marché américain des produits biopharmaceutiques non-oncologiques au cours de la période de prévision.
Par exemple, en 2017, Sanofi S.A. et son unité de gestion des vaccins Sanofi Pasteur ont collaboré avec MedImmune, le bras mondial de recherche et développement en biologie d'AstraZeneca Plc., pour le développement et la commercialisation d'un anticorps monoclonal, à savoir MEDI8897, pour la prévention de la maladie associée au virus respiratoire syncytial (VRS) chez les nouveau-nés et les nourrissons.
Le prix élevé des produits biologiques de marque devrait être un facteur important ayant une incidence négative sur son adoption.
Selon le rapport publié par l'Association for Accessible Medicines en 2018, le traitement annuel avec Humira est assorti d'un prix de liste de 38 000 $ US, et selon le rapport publié par I-Mak.org, entre 2012 et 2016, les dépenses moyennes pour Humira par personne aux États-Unis sont passées de 16 000 $ US à 33 000 $.
Tableau 1. Revenus des principales marques biopharmaceutiques non oncologiques aux États-Unis
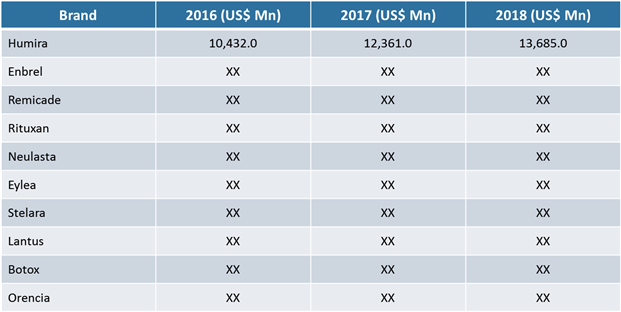
Pour en savoir plus sur ce rapport, demander un exemplaire
Source: Analyse cohérente des perspectives du marché (2018)
Possibilités de marché
Dans un passé récent, divers produits biologiques comme Humira et Remicade ont perdu leur brevet sur le marché américain. De plus, divers autres produits biologiques à revenu élevé devraient perdre leurs brevets dans un avenir proche.
La perte de brevets sur le marché américain offre une opportunité lucrative à d'autres acteurs pour le développement de ses biosimilaires. Par conséquent, les principaux acteurs du marché se concentrent sur le lancement et le développement de biosimilaires de produits biologiques sur le marché à un prix abordable.
Par exemple, en 2017, Merck & Co., Inc. a lancé RENFLEXIS (infliximab-abda), un biosimilaire du médicament biologique d'origine Remicade (infliximab) de Janssen Biotech, Inc. Selon l'entreprise, RENFLEXIS est introduit aux États-Unis à un prix de liste (coût d'acquisition global) de 753,39 $US, ce qui représente une réduction de 35 % par rapport au prix de liste actuel de Remicade, qui est son produit de référence.
Défis du marché
Haute R-D Investissements L'élaboration d'un produit biopharmaceutique IV/injectable nécessite une infrastructure sophistiquée, des scientifiques qualifiés et des investissements importants en ressources. La mise au point d'un produit biopharmaceutique nécessite une vaste recherche clinique et plusieurs phases d'essais, ce qui est un processus long et coûteux. Ces facteurs constituent des obstacles importants à l'entrée sur le marché des nouveaux acteurs.
Vente et commercialisation : Le marché américain des produits biopharmaceutiques non oncologiques a établi des acteurs du marché avec une solide équipe de vente et de commercialisation. La présence d'acteurs aussi forts dans le pays crée un grand défi pour les nouveaux joueurs d'entrer sur le marché et de soutenir contre ces grands joueurs.
Acceptation du médecin : L'acceptation par les médecins de produits de remplacement bien établis peut être un défi, en particulier parmi les indications pour lesquelles de nombreux produits sont disponibles et les produits de remplacement ne présentent pas un profil d'innocuité élevé ou amélioré et/ou un coût moindre.
Les principaux acteurs du marché américain des produits biopharmaceutiques non encologiques sont Sanofi S.A., Pfizer, Inc., Johnson & Johnson, Novartis International AG, Amgen, Inc., Eli Lilly and Company, AbbVie Inc., Bristol-Myers Squibb Company, F. Hoffmann-La Roche AG, Novo Nordisk A/S, GlaxoSmithKline plc., UCB Pharma, Teva Pharmaceutical Industries Ltd., Takeda Pharmaceutical Company Ltd, AstraZeneca Plc, Mylan N.V., LEO Pharma A/S, Boehringer Ingelheim GmbH, Alexion Pharmaceuticals Inc., Merck & Co., Inc., Elusys Therapeutics, Inc., Swedish Orphan Biovitrum AB, Samsung Bioepis NL B.V., Biogen Inc. et Theratechnologies Inc.
Partager
Vous n'avez pas envie de lire le rapport dans votre langue locale ? Trouvez votre langue préférée :
Transformez votre stratégie avec des rapports de tendances exclusifs :
Rejoindre des milliers d'entreprises à travers le monde engagées dans le making the Excellent Business Solutions..
Voir tous nos clients