Les tests et la certification des instruments médicaux mondiaux marché a été évalué à9 687 700 dollars des États-Unisen 2022 et devrait atteindre une valeur de13 550,8 millions de dollars des États-Unispar2030à unTCAC de 4,3 % entre2023 et 2030. Essais et certification des instruments médicaux Le marché connaît une forte croissance en raison de l'accent accru mis sur les essais et la certification des instruments médicaux et des règlements gouvernementaux rigoureux. En outre, l'apparition de COVID-19 et l'augmentation de l'utilisation de l'IA et de l'IoT dans les dispositifs médicaux devraient stimuler la croissance du marché. Toutefois, des facteurs tels que la diversité des règlements et l'éclosion de COVID-19 devraient entraver la croissance du marché.
Marché mondial des essais et de la certification d'instruments médicaux: Perspectives régionales
D'après la géographie, les essais et la certification des instruments médicaux mondiaux Le marché est segmenté en Amérique du Nord, en Europe, en Asie-Pacifique, en Amérique latine et au Moyen-Orient et en Afrique.
Parmi les régions, on s'attend à ce que l'Amérique du Nord gagne la plus forte part du marché au cours de la période de prévision en raison de la réglementation rigoureuse du gouvernement, de l'éclosion de COVID-19 et de la demande croissante de vérification et de validation des instruments médicaux. Par exemple, la Food and Drug Administration (FDA) est chargée de réglementer les matériels médicaux aux États-Unis. La FDA réglemente les dispositifs médicaux pour en assurer la sûreté et l'efficacité et élabore et exécute le programme national visant à contrôler les expositions inutiles à des produits électroniques émettant des rayonnements ionisants et non ionisants et à assurer leur utilisation sûre et efficace.
L'Europe et l'Asie-Pacifique devraient également être témoins d'une forte croissance des tests et des certifications mondiaux d'instruments médicaux marché en raison de l'éclosion de COVID-19, de l'accent accru mis sur la qualité des instruments médicaux et de la stricte réglementation gouvernementale dans ces régions. Par exemple, les autorités compétentes, les organismes notifiés et les représentants autorisés participent tous au processus de marquage CE. Les dispositifs médicaux sont réglementés au niveau des États membres de l'UE, mais l'Agence européenne des médicaments (EMA) participe au processus de réglementation. Les fabricants peuvent placer la marque CE sur un appareil médical après avoir passé une évaluation de la conformité.
Graphique 1. Part du marché mondial des essais et de la certification des instruments médicaux (%), par région, 2023
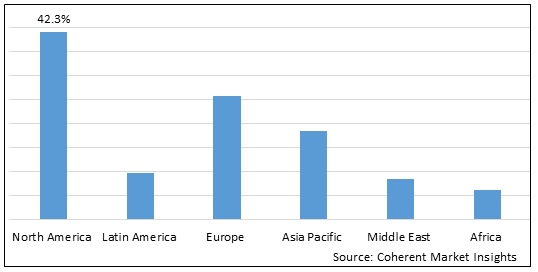
To learn more about this report, request sample copy
Conducteurs du marché des essais et de la certification d'instruments médicaux mondiaux :
L'accent est mis sur tests médicaux pour accroître la croissance du marché
L'un des principaux facteurs susceptibles d'accroître la croissance des tests et de la certification des instruments médicaux mondiaux Au cours de la période de prévision, l'accent est mis sur les essais et la certification des instruments médicaux. Par exemple, en janvier 2022, TÜV SÜD a prévu d'étendre ses installations de services médicaux et de santé à New Brighton, au Minnesota. Un nouveau laboratoire offrira une solution d'essai de bout en bout pour tous les dispositifs médicaux et fournira une gamme d'essais biologiques et chimiques des dispositifs médicaux qui complètent les capacités actuelles d'essai actif des dispositifs médicaux.
Réglementations gouvernementales strictes pour soutenir la croissance du marché
Un autre facteur qui est à l'origine de la croissance des tests et de la certification des instruments médicaux mondiaux Le marché est la réglementation gouvernementale stricte dans le monde entier. Par exemple, les directives normalisées pour les instruments médicaux varient d'un pays à l'autre et il est obligatoire pour les fabricants de suivre ces directives pour la commercialisation ou la vente de leurs produits médicaux dans le pays. Par exemple, les États-Unis suivent les lignes directrices de la Food and Drug Administration (FDA), l'Europe examine l'approbation de la conformité Europëenne (CE), le Canada a besoin de l'enregistrement de Santé Canada et l'Inde a besoin de l'approbation de la Central Drugs Standard Control Organisation (CDSCO).
Marché mondial des essais et de la certification d'instruments médicaux Possibilités :
On s'attend à ce que l'éclosion de COVID-19 offre des possibilités de croissance importantes aux acteurs du dépistage et de la certification des instruments médicaux mondiaux. marché. Par exemple, l'épidémie de COVID-19 a accru la demande de services de test et de certification des instruments médicaux dans le monde entier. En 2020, la Food and Drug Administration (FDA) des États-Unis a émis des autorisations d'utilisation d'urgence (UCE) pour les dispositifs médicaux permettant de diagnostiquer le COVID-19 ainsi que l'équipement de protection individuelle (EPI) nécessaire pour protéger les fournisseurs de soins de santé et les patients. Les tests médicaux et la certification se poursuivent et ont pris une phase rapide pendant la situation COVID 19.
Augmentation de l ' utilisation Intelligence artificielle (IA) et Internet des objets (IdO) dans les dispositifs médicaux devrait offrir des possibilités de croissance importantes pour les acteurs dans le test et la certification des dispositifs médicaux mondiaux marché. Par exemple, le déploiement de technologies de pointe, comme l'IA et l'IoT, ainsi que l'accent mis sur la surveillance en temps réel des patients, ont créé un écosystème complexe pour les dispositifs médicaux. Pour obtenir une autorisation de mise en marché, ces appareils doivent subir des essais méthodiques et doivent se conformer à des règlements rigoureux. Par conséquent, les acteurs du marché ou les fabricants investissent fortement pour tester leurs appareils et recevoir une autorisation de mise en marché.
Mise à l'essai des instruments médicaux et certification Couverture du rapport de marché
| Couverture du rapport | Détails | ||
|---|---|---|---|
| Année de base: | 2022 | Taille du marché en 2023: | 10 073,4 dollars des États-Unis Mn |
| Données historiques pour : | 2017 à 2021 | Période de prévision: | 2023 à 2030 |
| Période de prévision 2023 à 2030 TCAC: | 4,3% | 2030 Projection de valeur : | 13 550,8 millions de dollars des États-Unis |
| Géographies couvertes: |
| ||
| Segments couverts: |
| ||
| Sociétés concernées: | Medistri SA, BSI Group, Ente Certificazione Macchine, GMED, IMQ Group SRL, TOXIKON, TÜV SÜD, WuXi AppTec, Pace Analytical Services LLC, Gateway Analytical LLC, Boston Analytical, Bureau Veritas, UL LLC, TUV Rheinland, SGS SA, Intertek Group PLC, Eurofins Scientific, Element Materials Technology, Dekra Testing and Certification GmbH, et l'Institut pour les tests et la certification Inc., entre autres. | ||
| Facteurs de croissance : |
| ||
| Restrictions et défis : |
| ||
Uncover Macros and Micros Vetted on 75+ Parameters: Get Instant Access to Report
Essais et certification des instruments médicaux mondiaux Tendances du marché :
Nécessité test/certification des instruments médicaux est une tendance récente
Les instruments médicaux sont réglementés par diverses autorités de réglementation du monde entier. C'est principalement parce que les utilisateurs finaux de ces appareils attendent d'excellentes performances, sécurité et efficacité de ces appareils. Par conséquent, il est impératif que les fabricants mettent en œuvre correctement une stratégie d'essai des instruments médicaux, ce qui rend l'instrument efficace et facilite le processus de production. Cette tendance devrait se poursuivre au cours de la période de prévision, ce qui stimulera la croissance du marché.
Sous-traitance de essais et certification est une autre tendance
La demande de services d ' externalisation des services d ' essai à des fournisseurs tiers augmente avec un rythme rapide en raison de la forte intensité en capital des essais internes. Ainsi, plusieurs fabricants dans le monde entier ou des acteurs sous-traitent de plus en plus les services d'essais, car des réglementations strictes rendent coûteux la réalisation d'essais internes et aident ainsi ces entreprises à réduire le coût global des essais. Cette tendance devrait également se poursuivre au cours de la période de prévision, ce qui stimulera la croissance du marché.
Marché mondial des essais et de la certification d'instruments médicaux Restrictions:
Diversité des réglementations visant à entraver la croissance du marché
L'un des principaux facteurs susceptibles d'entraver la croissance des tests et des certifications des instruments médicaux mondiaux le marché est la diversité des réglementations ou des règles et réglementations strictes. Les lignes directrices normalisées pour les instruments médicaux varient d'un pays à l'autre, ce qui est obligatoire pour les fabricants de suivre, de commercialiser ou de vendre leurs produits dans le pays. Les règlements sont différents dans chaque pays. Par conséquent, pour les fabricants d'instruments médicaux, il est très crucial d'enregistrer et/ou de recevoir les directives réglementaires de ce pays.
L'épidémie de COVID-19 pour freiner la croissance du marché
Un autre facteur qui entrave la croissance des tests et de la certification des instruments médicaux mondiaux Le marché est le foyer de COVID-19. La pandémie a accru la demande de services de tests et de certification des instruments médicaux. Bien qu'il y ait des exemptions et des leviers dans la réglementation, les tests/certifications médicaux se poursuivent et ont pris une phase rapide pendant la pandémie. Cependant, la pandémie a eu un léger impact sur le marché, car les essais d'autres dispositifs médicaux, qui ne sont pas émergents, ont été suspendus.
Graphique 2. Part du marché mondial des essais et de la certification des instruments médicaux (%), par type de service, 2023
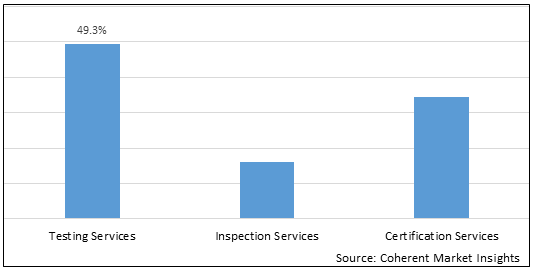
To learn more about this report, request sample copy
Essais et certification des instruments médicaux mondiaux Marché Segmentation:
Les tests et la certification des instruments médicaux mondiaux Le rapport de marché est divisé en type de service, type d'approvisionnement, classe d'appareils, technologie et géographie.
Basé sur les services Type, le marché est segmenté en Services d'essais, Services d'inspection et Services de certification. Dont: Services d'essais Segment devrait dominer les essais et la certification des instruments médicaux le marché au cours de la période de prévision, ce qui est attribuable à l'augmentation de la demande de dispositifs médicaux sûrs et efficaces.
Services d'inspection Segment On s'attend également à une croissance importante dans un proche avenir, en raison des règles et règlements rigoureux. Services d'inspection contribuer à réduire les coûts, minimiser les risques et fournir la qualité attendue.
Sur la base Type d'approvisionnement, le marché est segmenté en interne et externalisé. D'où, externalisé Segment On s'attend à ce que le marché domine au cours de la période de prévision, ce qui est attribuable à la tendance croissante à sous-traiter les services d'essai d'instruments médicaux.
Sur la base Classe de périphérique, le marché est segmenté en classes I, II et III. D'où, Classe I Segment On s'attend à ce que le marché domine au cours de la période de prévision, ce qui est attribuable à la demande croissante d'instruments médicaux de classe I. En fonction des risques associés à l'utilisation d'un instrument médical, ces instruments sont classés dans la classe I, la classe II ou la classe III. La classification dépend du niveau de risque associé à l'instrument.
Classe II Segment On s'attend également à une croissance importante dans un avenir proche, en raison de la demande croissante d'instruments médicaux de classe II.
Sur la base Technologie, le marché est segmenté en instrument médical actif, instrument médical actif, instrument médical non actif, instrument médical de diagnostic in vitro, instrument médical ophtalmique, instrument médical orthopédique et dentaire, instrument médical vasculaire et autres technologies. D'où, Dispositif médical actif Segment On s'attend à ce que le marché domine au cours de la période de prévision, ce qui est attribuable à la hausse de la demande de dispositifs médicaux actifs pour implants. En tant que l'une des catégories d'instruments les plus à risque, les AIM sont soumis à des contrôles réglementaires rigoureux avant de pouvoir atteindre les marchés mondiaux.
Segment des instruments médicaux diagnostiques in vitro On s'attend également à une croissance importante dans un avenir proche, ce qui est dû à une attention accrue accordée au diagnostic précoce (en raison de l'augmentation du fardeau des maladies mortelles dans le monde). Les instruments médicaux de diagnostic in vitro sont des tests utilisés sur des échantillons biologiques pour déterminer l'état de santé d'une personne.
Marché mondial des essais et de la certification d'instruments médicaux: Clé Faits nouveaux
En février 2021, Alfa Médical (AMG) prévoit d'investir 263,5 millions d'euros sur le marché au cours des cinq prochaines années, afin d'élargir le marché égyptien des soins de santé, notamment en augmentant le nombre de laboratoires, d'installations de production et de normes.
En février 2021, l'application de programmeur clinicien de neuromodulation de BSI et son application de contrôleur patient, pour une utilisation sur des appareils intelligents Apple personnels compatibles, au règlement sur les dispositifs médicaux (MDR) (UE 2017/745) via son corps notifié aux Pays-Bas (2797).
En avril 2021, TÜV SÜD a annoncé qu'elle s'était présentée à Medtec LIVE pour démontrer sa capacité à être un guichet unique pour les tests médicaux.
En octobre 2020, TÜV Rheinland a annoncé l'ouverture de ses laboratoires d'essais biomatériaux et de compatibilité électromagnétique (EMC) situés à Andhra Pradesh MedTech Zone (AMTZ), Visakhapatnam (Andhra Pradesh), en Inde.
Marché mondial des essais et de la certification d'instruments médicaux: Principales perspectives des entreprises
Les tests et la certification des instruments médicaux mondiaux Le marché est très concurrentiel. Ceci est attribué à la nécessité de tester et de certifier les instruments médicaux dans le monde entier, de sorte que les acteurs du marché se concentrent sur le lancement de nouveaux produits sur le marché.
Quelques-uns des principaux acteurs de l'essai et de la certification des instruments médicaux mondiaux marché sont Medistri SA, BSI Group, Ente Certificazione Macchine, GMED, IMQ Group SRL, TOXIKON, TÜV SÜD, WuXi AppTec, Pace Analytical Services LLC, Gateway Analytical LLC, Boston Analytical, Bureau Veritas, UL LLC, TUV Rheinland, SGS SA, Intertek Group PLC, Eurofins Scientific, Element Materials Technology, Dekra Testing and Certification GmbH, et l'Institut pour les tests et certification Inc., entre autres.
*Définition : Les tests et la certification des instruments médicaux sont nécessaires pour assurer la sécurité et l'efficacité des instruments médicaux. Les États-Unis suivent les lignes directrices de la Food & Drug Administration (FDA), le Canada a besoin de l'enregistrement de Santé Canada, l'Europe envisage l'approbation de Conformitè Europëenne (CE) et l'Inde a besoin de l'approbation de l'Organisation centrale de normalisation des médicaments (OCDS).
Share
About Author
Manisha Vibhute
Manisha Vibhute is a consultant with over 5 years of experience in market research and consulting. With a strong understanding of market dynamics, Manisha assists clients in developing effective market access strategies. She helps medical device companies navigate pricing, reimbursement, and regulatory pathways to ensure successful product launches.
Transform your Strategy with Exclusive Trending Reports :
Frequently Asked Questions
Joining thousands of companies around the world committed to making the Excellent Business Solutions.
View All Our Clients