US Non-oncology Biopharmaceuticals Market- Insights
Biologen können als Moleküle definiert werden, die von lebenden Zellen wie Mikroorganismen, Pflanzen oder Tierzellen abgeleitet werden und bei der Behandlung, Diagnose oder Prävention von Krankheiten verwendet werden. Die meisten biologen Moleküle sind sehr große, komplexe Moleküle oder Molekülgemische.
Biopharmazeutika sind Teil einer breiteren Kategorie von therapeutischen Mitteln namens Biologik. Biopharmazeutika sind die in lebenden Systemen mit Hilfe der Biotechnologie entwickelten Substanzen und werden in therapeutischen und diagnostischen Anwendungen eingesetzt. Nicht-onkologische Biopharmazeutika sind die Medikamente, die bei der Behandlung von verschiedenen Krankheiten verwendet werden, anstatt Krebs wie rheumatoide Arthritis, Psoriatic Arthritis, Multiple Sklerose, Hämophilie, altersbedingte Makuladegeneration, Osteoporose und andere.
Steigende Starts, Zulassungen und robuste Pipeline von neuartigen Biopharmazeutika für Nicht-onkologische Indikationen
Häufige Zulassungen, Starts und robuste Pipeline von neuartigen nicht-onkologischen Biopharmazeutika für verschiedene Indikationen auf dem US-Markt wird erwartet, dass das nicht-onkologische Biopharmazeutika-Marktwachstum deutlich unterstützt.
So erhielten Eli Lilly und das Unternehmen im September 2018 die Zulassung der US Food and Drug Administration (FDA) für ihre Emgality (Galcanezumab-gnlm) 120 mg Injektion zur präventiven Behandlung von Migräne bei Erwachsenen.
Im Februar 2018 kündigte Novartis an, dass die US Food and Drug Administration (FDA) ein Label-Update für ihren Cosentyx (secukinumab), den ersten Interleukin-17A (IL-17A) Inhibitor, der zur Behandlung von mittelschweren Plaque Psoriasis zugelassen wurde, genehmigt hat.
Im Juli 2018 haben Amgen Inc. und UCB Inc. die Biologics License Application (BLA) an die US Food and Drug Administration (FDA) für EVENITY (romosozumab) zurückgegeben, einen Untersuchungs-Monoklonalantikörper zur Behandlung von Osteoporose bei postmenopausalen Frauen mit hohem Bruchrisiko.
Die US-amerikanische nicht-onkologische Biopharmazeutika Marktgröße wurde mit US$ 116.0 bewertet Bn im Jahr 2018 und erwartet eine CAGR von 10,2% während der Prognosezeit (2018 – 2026).
Abbildung 1. US Non-oncology Biopharmaceuticals Marktanteil (%), Nach Produkttyp, 2018-2026
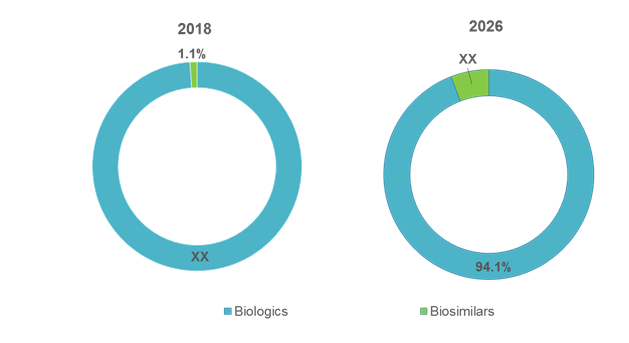
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Quelle: Coherent Market Insights Analysis (2018)
Zunehmende Fusionen und Kooperationen unter den Schlüsselakteuren für die Entwicklung neuartiger Biopharmazeutika der Nicht-Onkologie sollen das Marktwachstum unterstützen
Schlüsselakteure auf dem Markt sind an strategischen Fusionen und Kooperationen für die Entwicklung neuer biopharmazeutischer Produkte beteiligt und in den USA vermarktet. Solche strategischen Zusammenschlüsse und Kooperationen zwischen Schlüsselakteuren sollen die Entwicklung von neuartigen Produkten unterstützen, die wiederum erwartet werden, dass die US-amerikanischen nicht-onkologischen Biopharmazeutika über den Prognosezeitraum wachsen.
So kooperierte Sanofi S.A. und sein Impfstoff-Geschäftsbereich Sanofi Pasteur 2017 mit MedImmune, dem globalen Biologenforschungs- und Entwicklungsarm von AstraZeneca Plc., für die Entwicklung und Vermarktung eines monoklonalen Antikörpers, nämlich MEDI8897, zur Prävention von respiratorischen Syncytial Virus (RSV) in Neugeborenen und Säuglingen.
Der hohe Preis der Marken Biologik-Produkte wird voraussichtlich ein wesentlicher Faktor sein, der seine Annahme negativ beeinflusst.
Laut dem von der Association for Accessible Medicines im Jahr 2018 veröffentlichten Bericht kommt die jährliche Behandlung mit Humira mit einem Listenpreis von 38.000 US-Dollar, und nach dem Bericht von I-Mak.org, zwischen 2012 und 2016, die durchschnittlichen Ausgaben für Humira pro Person in US$ 16.000 auf US$ 33.000.
Tabelle 1. Umsatz der Top Non-oncology Biopharmazeutischen Marken in den USA
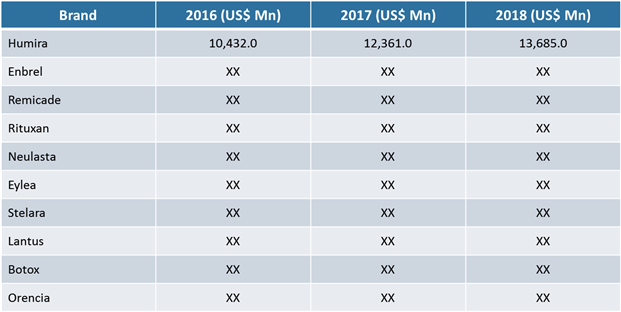
Um mehr über diesen Bericht zu erfahren, Beispielkopie anfordern
Quelle: Coherent Market Insights Analysis (2018)
Marktchance
In der jüngsten Vergangenheit verloren verschiedene Blockbuster-Biologen wie Humira und Remicade Patent im US-Markt. Darüber hinaus wird erwartet, dass in naher Zukunft verschiedene andere hochauflösende Biologen ihre Patente verlieren.
Der Verlust des Patents im US-Markt bietet anderen Akteuren eine lukrative Gelegenheit zur Entwicklung seiner Biosimilars. Daher konzentrieren sich die Schlüsselakteure auf die Markteinführung und Entwicklung von Biosimilars biologischer Produkte zu erschwinglichen Preisen.
So startete Merck & Co., Inc. im Jahr 2017 RENFLEXIS (infliximab-abda), eine Biosimilar der Urheber-Biologmedizin Remicade (infliximab) von Janssen Biotech, Inc. RENFLEXIS wird in den USA zu einem Listenpreis (Wholesaler Akquisitionskosten) von 753.39 US$ eingeführt. Dies entspricht einem Rabatt von 35 % auf den aktuellen Listenpreis von Remicade, dessen Referenzprodukt ist.
Marktherausforderungen
Hohe R&D Investitionen: Die Entwicklung eines IV/injizierbaren Biopharmazeutikums erfordert eine anspruchsvolle Infrastruktur, qualifizierte Wissenschaftler und bedeutende Ressourceninvestitionen. Die Entwicklung eines biopharmazeutischen Produktes erfordert umfangreiche klinische Forschung und mehrere Phasen von Versuchen, die ein langwieriges und teures Verfahren ist. Diese Faktoren sind wesentliche Hindernisse für den Einstieg in den Markt.
Vertrieb und Marketing: Der US-amerikanische Biopharmazeutika-Markt hat Marktteilnehmer mit starkem Vertriebs- und Marketingteam etabliert. Die Präsenz solcher starken Spieler im Land schafft eine große Herausforderung für neue Spieler, in den Markt zu kommen und gegen solche großen Spieler zu erhalten.
Physician Akzeptanz: Physicianische Akzeptanz von Ersatzstoffen für etablierte Produkte kann eine Herausforderung sein, insbesondere unter Hinweisen, für die zahlreiche Produkte verfügbar sind und Ersatzstoffe kein hohes/ besseres Sicherheitsprofil und/oder geringere Kosten aufweisen.
Zu den wichtigsten Akteuren im US-amerikanischen Biopharmazeutikum gehören Sanofi S.A., Pfizer, Inc., Johnson & Johnson, Novartis International AG, Amgen, Inc., Eli Lilly und Company, AbbVie Inc., Bristol-Myers Squibb Company, F. Hoffmann-La Roche AG, Novo Nordisk A/S, GlaxoSmithKline. Pharma A/S, Boehringer Ingelheim GmbH, Alexion Pharmaceuticals Inc., Merck & Co., Inc., Elusys Therapeutics, Inc., Swedish Orphan Biovitrum AB, Samsung Bioepis NL B.V., Biogen Inc., and Theratechnologies Inc.
Teilen
Vermissen Sie den Komfort, Berichte in Ihrer Landessprache lesen zu können? Finden Sie Ihre bevorzugte Sprache:
Verwandeln Sie Ihre Strategie mit exklusiven Trendberichten :
Wir schließen uns Tausenden von Unternehmen auf der ganzen Welt an, die sich der Aufgabe verschrieben haben,ng the Excellent Business Solutions..
Alle unsere Kunden anzeigen